Переливание крови, ее компонентов и кровезаменителей может осуществляться:
1. внутривенно (путем венепункции или венесекции);
2. внутриартериально;
3. внутрикостно.
Внутривенное переливание, как правило, дает меньше осложнений, хорошо переноситься больным. Является основным. Внутривенное вливание производится в одну из наиболее выраженных вен (чаще локтевую). При выборе вены для трансфузии предпочтение отдается венам верхней конечности. Вены нижней конечности используются реже в связи с большей опасностью тромбоза из-за замедления кровотока в них.
У детей раннего возраста чаще пунктируют вены головы (височная, лобная).
Во время длительных полостных операций и в порядке исключения при плохо выраженных венах допускается доступ к нужной вены путем венесекции. Для длительных трансфузий прибегают к катетеризации подключичной вены или большой подкожной вены бедра.
Внутриартериальное переливание крови производится по специальным показаниям, используется редко. Связано с тем, что внутриартериальное введение не превосходит, а во многих случаях уступает внутривенному.
Кровь вводится в обнаженную артерию (лучевую, плечевую, заднюю большеберцовую), в культю артерии в операционной, реже в другие артерии. Особенностью этого метода является необходимость создания и поддержания давления в системе для подачи препарата в сосудистое русло реципиента. В ампулу, из которой производится вливание, нагнетают воздух до давления 180 мм рт. ст., что обеспечивает потребности трансфузии. Давление во флаконе с трансфузионной средой, создаваемой при помощи резинового баллона, контролируется пружинным манометром от аппарата для измерения давления.
Есть интересные отечественные разработки систем для внутриартериального введения жидкостей. В.П. Сухоруков с соавторами (удостоверение на рационализаторское предложение №1 от 28 июня 1972 года, выданное Кировским научно-исследовательским институтом переливания крови) предложил систему, где помимо обычных частей имелся воздушный компенсатор и капельница с поплавком (рисунок 13).
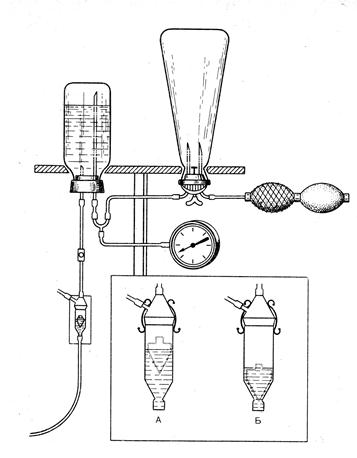
Рис. 13. Система для внутриартериального переливания
В качестве воздушного компенсатора в системе В.П. Сухорукова применяется литровая банка от аппарата Боброва. Воздушный компенсатор благодаря сжимаемости воздуха позволяет легко поддерживать избранное давление и регулировать скорость переливания. Особая конструкция капельницы, которая представляет собой стеклянную камеру с плавающим стеклянным поплавком, позволяет в завершающий момент нагнетания избежать опасности эмболии, так как поплавок опуститься на дно.
Внутрикостное переливание крови проводится в случаях плохо выраженных вен, при обширных ожогах, отморожениях. Также в клинической практике используется редко. Для внутрикостных переливаний используются гребень подвздошной кости, проксимальный метафиз большеберцовой. кости, наружный мыщелок бодренной кости, пяточная кость (наружная сторона). При внутрикостных вливаниях применяется игла с муфтой типа Кассирского или игла с мандреном. Иглу в кость вводят сверлящими движениями, предварительно обработав операционное поле (спирт, велтосепт) и обезболив (0,25-0,5% раствор новокаина). Ощущение "прокола" иглы свидетельствует о том, что она перфорировала кортикальный слой кости и находится в губчатом ее слое. Затем извлекают мандрен, аспирируют. костный мозг, вводят 5 мл 0,5% раствора новокаина и присоединяют к игле систему для переливания. Рекомендуется периодически промывать иглу 0,5% раствором новокаина. Детям раннего возраста внутрикостно кровь вводится шприцем емкостью 10-20 мл.
Трансфузию в костномозговое вещество нельзя производить под большим давлением (опасность эмболии).
§ 2. Обратное переливание
(аутологичные трансфузии)
Существуют следующие методы проведения аутологичных трансфузий:
1. предоперационная заготовка аутокрови или аутоэритроцитной массы или взвеси, позволяющая собрать за 3 – 4 недели до планового хирургического вмешательства 3 – 4 дозы (до 1000 – 1200 мл аутокрови консервированной или 600 – 700 мл аутоэритроцитной массы);
2. предоперационная нормоволемическая или гиперволемическая гемодилюция, предполагающая заготовку 1 – 2 доз крови (600 – 800 мл) непосредственно до операции или начала анестезии с обязательным восполнением временной кровопотери солевыми растворами и плазмозаменителями с поддержанием нормоволемии или гиперволемии;
3. интраоперационная реинфузия крови – сбор во время операции из операционной раны и полостей излившейся крови с обязательным последующим отмыванием и возвратом в русло крови реципиента аутокрови полостной, консервированной, фильтрованной для реинфузии. Такая же процедура возможна при использовании дренажной крови, получаемой в стерильных условиях при послеоперационном дренировании полостей тела.
Каждый из этих методов может применяться отдельно или в различных сочетаниях. Возможно одновременное или последовательное применение переливаний аутологичных компонентов крови с аллогенными.
Предоперационная заготовка аутокрови
Объем разовой кроводачи для лиц с массой тела более 50 кг не должен превышать 450 мл. При массе тела менее 50 кг объем кроводачи - не более 8 мл/кг массы тела. Лица с массой тела менее 10 кг к терапевтическому аутодонорству не допускаются. Количество антикоагулянтного раствора уменьшается пропорционально количеству эксфузируемой крови. Уровень гемоглобина у аутодонора перед каждой кроводачей не должен быть ниже 110 г/л, гематокрита - не ниже 33%.
Частота аутологичных кроводач определяется лечащим врачом и трансфузиологом. При этом следует учитывать, что объем плазмы и уровень общего белка и альбумина восстанавливается через 72 часа, т.е. последняя кроводача перед плановой операцией должна быть выполнена за 3 суток.
Большинство аутодоноров, особенно при заготовке более, чем одной дозы крови, должны получать таблетированные препараты железа. Известно, что скорость эритропоэза ограничена адекватным количеством железа в организме, которое равно примерно 2 г для женщин и 3 г для мужчин. Каждая донация 1 дозы крови снижает запасы железа на 200 мг (примерно, 1 мг на 1 мл эритроцитов). Прием препаратов железа начинают до первой кроводачи. В ряде случаев для ускорения образования эритроцитов целесообразно одновременное назначение эритропоэтина. Назначение препаратов железа и эритропоэтина аутодонору должно быть согласовано с лечащим врачом.
Хранение аутокрови или ее компонентов проводится по тем же правилам, что и для гомологичных компонентов крови.
Не допускаются к аутодонорству лица с установленным очагом инфекции (любым, необходима предварительная санация) или бактериемией, при верификации нестабильной стенокардии, стеноза аорты, серповидноклеточной анемии. Выявленная тромбоцитопения (количество тромбоцитов ниже 180 х 10(9)/л) также служит основанием для отвода от аутодонорства.
Положительное серологическое тестирование аутореципиента на ВИЧ, гепатит и сифилис является противопоказанием к использованию аутодонорства.
Частота побочных реакций при проведении заготовки аутокомпонентов крови аналогична общей донорской практике и составляет от 2 до 5% всех донаций. Чаще всего встречаются вазовагальные реакции на временную кровопотерю (обморок, головокружение, нарушение сердечного ритма, нерезкое снижение систолического артериального давления). Помещение, где проводится эксфузия крови у аутодоноров, должно быть оснащено для проведения мероприятий возможной интенсивной терапии, а персонал - соответствующим образом подготовлен.
Предтрансфузионный контроль аутологичной переносчиков газов крови, проведение проб на ее совместимость с реципиентом и биологической пробы подлежит выполнению врачом, непосредственно переливающим эту трансфузионную среду, как и в случае применения компонентов аллогенной крови, особенно если используются и донорские, и аутодонорские компоненты крови.
В целом, предоперационная заготовка аутокрови или ее компонентов не должна ухудшить состояние больного до операции.
В большинстве случаев программа аутодонорства предусматривает сбор, краткосрочное хранение и переливание цельной консервированной аутологичной крови и аутоэритроцитной массы или взвеси. Однако возможно аутодонорство плазмы, тромбоцитов.
Аутоплазма свежезамороженная, получаемая из аутологичной крови, может быть заготовлена в терапевтически значимых количествах (500 - 1000 мл) в плановых условиях и с успехом применена при отягощенном кесаревом сечении в акушерстве, в сердечно-сосудистой хирургии и ортопедии.
Аутологичный концентрат тромбоцитов и аутоплазма свежезамороженная могут быть использованы при операциях с искусственным кровообращением в сердечно-сосудистой хирургии, где нередко наблюдается тромбоцитопения в послеоперационном периоде. Заготовленный за 3 - 5 дней до операции аутотромбоцитный концентрат хранятся при комнатной температуре (20 - 24°С) в условиях постоянного перемешивания и переливаются во время операции или сразу после нее, что существенно уменьшает объем послеоперационной кровопотери.
Предоперационная гемодилюция
Достоинство подобного метода аутодонорства заключается в том, что во время операции пациент теряет кровь с меньшим содержанием эритроцитов, чем он имел до проведения гемодилюции. Последующая трансфузия несколькими часами ранее заготовленной цельной консервированной аутологичной крови, преимущественно после окончания основной хирургической кровопотери, позволяет быстро повысить концентрацию гемоглобина, коагуляционных факторов, уровень тромбоцитов и объем крови.
Гемодилюция может быть изоволемической, при которой сохраняется и поддерживается исходный (нормальный) объем циркулирующий крови, в котором лишь временно уменьшается объем и концентрация клеток крови. Возможна и гиперволемическая гемодилюция, при которой врач перед предстоящей массивной кровопотерей идет на увеличение внутрисосудистого циркулирующего объема крови выше нормы за счет избыточного переливания плазмозаменителей под контролем гемодинамики и центрального венозного давления, тем самым также снижая потерю эритроцитов во время операции.
Предоперационная гиперволемическая гемодилюция не показана больным с выраженной коронарной недостаточностью, тяжелыми нарушениями ритма сердца, гипертонией (систолическое АД более 180 мм рт.ст.), тяжелыми поражениями легких с респираторной недостаточностью, почек, печени, нарушениями в системе свертывания, при наличии очагов инфекции.
Больной должен быть заранее информирован о проведении предоперационной гемодилюции, на которую он дает свое согласие, фиксируемое в истории болезни (раздел 1 настоящей инструкции). Лечащий врач и трансфузиолог в истории болезни обосновывают необходимость проведения гемодилюции. Проводит предоперационную гемодилюцию трансфузиолог или специально подготовленный врач. Непосредственно перед началом процедуры измеряется и фиксируется АД, пульс, уровень гемоглобина и гематокрита. Пунктируются две вены - одна для эксфузии, другая для восполнения. При невозможности пункции второй вены эксфузия и восполнение чередуются.
Эксфузированный объем крови восполняется солевыми растворами (3 мл на каждый мл изъятой крови) или коллоидами (1 мл на каждый мл собираемой крови). Количество забираемой крови варьирует, но постгемодилюционный уровень гемоглобина не должен быть ниже 90 - 100 г/л, а уровень гематокрита - не менее 28%. Кровь собирается в стандартные пластикатные контейнеры для крови, содержащие гемоконсервант. Ведется протокол гемодилюции, в котором фиксируется состояние больного, объем эксфузируемой крови, объем восполнения, состояние гемодинамики, время начала и окончания процедуры.
Контейнер с цельной консервированной аутологичной кровью или тщательно маркируется: день, час, фамилия больного, название среды; если контейнеров несколько, то их порядковый номер. Интервал между эксфузией и реинфузией не должен быть более 6 часов, в противном случае контейнеры с кровью должны быть помещены в холодильник с температурой 4°С. Из операционной контейнеры с цельной консервированной аутологичной кровью при проведении предоперационной гемодилюции не выносятся.
Переливание цельной консервированной аутологичной крови начинается, как правило, после окончания этапа операции, связанного с наибольшей кровопотерей. Доза аутокрови, заготовленная последней, переливается первой. Переливается аутокровь через стандартные системы для переливания с фильтром.
Нормоволемическая гемодилюция проводится или до введения больного в наркоз или после вводного наркоза, но до начала операции. В последнем случае аутокровь забирается оксигенированной, поскольку искусственная вентиляция легких, проводимая во время наркоза в режиме умеренной гипервентиляции, способствует повышению содержания кислорода в венозной крови. Во время основного наркоза и операции необходим контроль гемодинамических показателей, почасового диуреза, газов крови с целью поддержания нормальной оксигенации тканей и нормоволемии, обеспечивающей адекватную перфузию органов.
Гиперволемическая гемодилюция проводится по тем же принципам, что и нормоволемическая, но при этом поддерживают уровень гематокрита в пределах 23 - 25%, используя для замещения эксфузируемой аутокрови растворы гидрооксиэтилкрахмала или 5 - 10% альбумина.
Интраоперационная реинфузия крови
Реинфузия крови, теряемой во время операции, предполагает аспирацию такой крови из операционной раны или полостей тела стерильным отсосом в стерильную емкость с последующим отмыванием, а затем возврат реципиенту во время операции или в срок, не превышающий 6 часов после начала сбора. Применение интраоперационной реинфузии крови показано только при тех обстоятельствах, когда предполагаемая кровопотеря превышает 20% объема циркулирующей крови, что наблюдается в сердечно-сосудистой хирургии, при разрыве внематочной беременности, в ортопедической хирургии, в травматологии.
Противопоказана интраоперационная реинфузия крови при ее бактериальном загрязнении, попадании амниотической жидкости, при отсутствии возможности отмывания излившейся во время операции крови.
Излившаяся в полости тела кровь отличается по своему составу от циркулирующей крови. В ней снижено содержание тромбоцитов, фибриногена, 2,3-дифосфоглицерата, высок уровень свободного гемоглобина, имеются продукты деградации фибриногена. В какой-то степени эти недостатки нивелируются в процессе обязательного отмывания эритроцитов перед реинфузией.
Фильтрование излившейся крови через несколько слоев марли в настоящее время недопустимы. Созданы специальные приборы для проведения интраоперационного сбора и отмывания крови, теряемой во время операции.
Как пример, приводим принцип действия аппарата для реинфузии «CELL SAVER 5».

Рис. 14. Аппарат для реинфузии «CELL SAVER 5»
Теряемая во время операции кровь собирается отсосом, затем смешивается с антикоагулянтом и поступает в резервуар, где отфильтровываются мелкие кусочки тканей, сгустки крови и другие макроструктуры. Из резервуара с помощью периcтaльтического насоса кровь попадает во вращающийся колокол. Эритроциты связываются в центрифуге центробежными силами, в то время, как плазма выносится из колокола, вымывая свободный гемоглобин, антикоагулянт, активированный фактор свертывания (АСТ), активизированные тромбоциты. Как только гемакрит крови, содержащийся в колоколе, достигает 55%, туда начинает поступать физиологический раствор, промывая эритроциты.
Эффективность промывки составляет более 95%, количество эритроцитов более 98% от собранных. По окончании цикла промывки концентрированная суспензия эритроцитов в физиологическом растворе поступает в мешок для реинфузии. Аппарат имеет высокую скорость работы. Например: время одного цикла с использованием типовых скоростей помпы при 1200 мл собранной крови в резервуаре с Ht=10-20% составляет 3 мин. Результатом является 225 мл взвези эритроцитов в физиологическом растворе в которой содержится 137мл чистых эритроцитов.
Аппарат также позволяет проводить предоперационную секвестрацию крови пациента на эритроцитную массу и плазму, обогащенную тромбоцитами в полуавтоматическом режиме.
§ 3. Особенности переливания
некоторых компонентов крови
В заключении главы необходимо более подробно остановиться на особенностях переливания некоторых компонентов крови (свежезамороженной плазмы и лейкоцитного концентрата).
Особенности переливания плазмы Свежезамороженной
Переливание плазмы свежезамороженной осуществляется через стандартную систему для переливания крови с фильтром, в зависимости от клинических показаний – струйно или капельно, при остром ДВС-синдроме с выраженным геморрагическим синдромом – струйно. Запрещается переливание плазмы свежезамороженной нескольким больным из одного контейнера или бутылки.
При переливании плазмы свежезамороженной необходимо выполнение биологической пробы (аналогичной при переливании переносчиков газов крови). Первые несколько минут после начала инфузии плазмы свежезамороженной, когда в циркуляцию реципиента поступило еще небольшое количество переливаемого объема, являются решающими для возникновения возможных анафилактических, аллергических и других реакций.
Объем переливаемой плазма свежезамороженная зависит от клинических показаний. При кровотечении, связанном с ДВС-синдромом показано введение не менее 1000 мл плазмы свежезамороженной одномоментно под контролем гемодинамических показателей и центрального венозного давления. Нередко необходимо повторное введение таких же объемов плазмы свежезамороженной под динамическим контролем коагулограммы и клинической картины. В этом состоянии неэффективно введение небольших количеств (300 – 400 мл) плазмы.
При острой массивной кровопотере (более 30% объема циркулирующей крови, для взрослых – более 1500 мл), сопровождающейся развитием острого ДВС-синдрома, количество переливаемой плазмы свежезамороженной должно составлять не менее 25 - 30% всего объема трансфузионных сред, назначаемых для восполнения кровопотери, т.е. не менее 800 – 1000 мл.
При хроническом ДВС-синдроме, как правило, сочетают переливание плазмы свежезамороженной с назначением прямых антикоагулянтов и антиагрегантов (необходим коагулологический контроль, являющийся критерием адекватности проводимой терапии). В этой клинической ситуации объем однократно переливаемой плазмы свежезамороженной – не менее 600 мл.
При тяжелых заболеваниях печени, сопровождающихся резким снижением уровня плазменных факторов свертывания и развившейся кровоточивостью или угрозой кровотечения во время операции, показано переливание плазмы свежезамороженной из расчета 15 мл/кг массы тела с последующим, через 4 – 8 часов, повторным переливанием плазмы в меньшем объеме (5 – 10 мл/кг).
Непосредственно перед переливанием плазму свежезамороженную оттаивают в водяной бане при температуре 37°С. В оттаянной плазме возможно появление хлопьев фибрина, что не препятствует ее использованию с помощью стандартных устройств для внутривенного переливания с фильтром.
Возможность длительного хранения плазмы свежезамороженной позволяет накапливать ее от одного донора с целью реализации принципа "один донор – один реципиент", что позволяет резко снизить антигенную нагрузку на реципиента.
Наиболее тяжелым риском при переливании плазмы свежезамороженной, является возможность передачи вирусных и бактериальных инфекций. Именно поэтому сегодня уделяется большое внимание методам вирусной инактивации плазмы свежезамороженной (карантинизация плазмы в течение 3 - 6 месяцев, обработка детергентом и др.).
Кроме того, потенциально возможны иммунологические реакции, связанные с наличием антител в плазме донора и реципиента. Наиболее тяжелая из них - анафилактический шок, клинически проявляющийся ознобом, гипотонией, бронхоспазмом, загрудинными болями. Как правило, подобная реакция обусловлена дефицитом IgA у реципиента. В этих случаях требуется прекращение переливания плазмы, введение адреналина и преднизолона. При жизненной необходимости продолжения терапии с помощью переливания плазмы свежезамороженной возможно назначение антигистаминных и кортикостероидных препаратов за 1 час до начала инфузии и повторное их введение во время переливания.
Особенности переливания лейкоцитного концентрата
Лейкоциты переливаются, по возможности, сразу, но не позднее 24 часов после получения. Для достижения терапевтического эффекта переливания лейкоцитов должны быть ежедневными, не менее 4 – 6 дней подряд при условии отсутствия восстановления гранулоцитопоэза или побочных реакций. Переливается концентрат лейкоцитов через обычное устройство для внутривенного переливания крови и ее компонентов с фильтром. Предтрансфузионное тестирование лейкоцитного концентрата аналогично таковому при переливании переносчиков газов крови. Совместимость по системам АВ0 и Rh обязательна. Совместимость по гистолейкоцитарным антигенам (HLA) обеспечивает лучший ответ на трансфузию, особенно у больных с выявленными антителами системы HLA. Объем лейкоцитного концентрата обычно находится в пределах 200 – 400 мл, в педиатрической практике он должен быть уменьшен с целью избежания волемической перегрузки.
 2015-01-21
2015-01-21 1249
1249
