Лекция 3
Ферменты. Строение, механизм действия, классификация.
Энергия активации. Катализаторы
Рассмотрим популяцию молекул D, находящихся в ограниченном замкнутом пространстве. В такой популяции индивидуальные молекулы при постоянной температуре сильно различаются по количеству содержащейся (внутренней) в них энергии:
1) молекулы с высокой энергией (Еmax), незначительное количество;
2) молекулы со средним значением энергии (Еmid), большинство молекул;
3) молекулы с низкой энергией (Еmin), незначительное количество.
Химическая реакция X→Y (CO2 + H2O → H2CO3) протекает потому, что в любой момент времени некоторая доля молекул D обладает б о льшей внутренней энергией (Еmax) по сравнению с другими молекулами данной популяции, и этой энергии оказывается достаточно для достижения ими вершины энергетического барьера и перехода в активную форму, называемую активным состоянием: (Рис. 3.1):
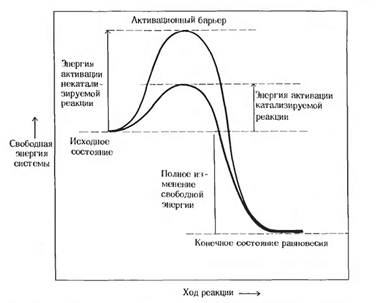
Рис. 3.1. Катализаторы снижают энергию активации (энергетический, или активационный, барьер) химических реакций, не влияя при этом на полное изменение свободной энергии в ходе реакции.
Энергией активации называется количество энергии необходимое для того, чтобы все молекулы вещества при определённой температуре перешли в активированное состояние, соответствующее вершине активационного барьера.
В ходе реакции молекулы приобретают энергию, достаточную для их активации, и оказываются в переходном состоянии; далее происходит образование продуктов.
При графическом изображении (Рис. 3.1) энергия активации (Еа) – это высота энергетического барьера, которая должна быть преодолена молекулами для осуществления химической реакции.
Достижение переходного состояния реагирующими молекулами (субстрата) возможно двумя путями:
1) придать реагирующим молекулам избыточную энергию за счёт увеличения температуры;
2) снизить энергию активации соответствующей реакции.
 2015-01-21
2015-01-21 413
413







