Описание установки.
 Для измерения объема водорода, выделившегося в результате взаимодействия металла с серной кислотой, используют эвдиометр (рисунок 2.1.).
Для измерения объема водорода, выделившегося в результате взаимодействия металла с серной кислотой, используют эвдиометр (рисунок 2.1.).
Резервуар Р и бюретка Б соединены с резиновой трубкой и заполнены водой. Бюретка закрыта пробкой с отводной трубкой, соединяющей бюретку и реакционную пробирку П. Если в пробирке проводить реакцию Me c кислотой, то выделившийся при этом водород будет увеличивать давление паров в бюретке и вытеснять воду из бюретки в резервуар Р в объеме, равном выделившемуся водороду.
План эксперимента.
1. Заполните водой резервуар Р и бюретку Б, так чтобы уровень воды в бюретке при закреплении резервуара Р на штативе в верхнем положении был ниже нулевого деления бюретки Р. Пробирка П при этом должна быть снята с пробки.
2. Налейте в пробирку 4-5 мл серной кислоты.
3. Получите у преподавателя взвешенную с точностью 0,0001г порцию металла (навеска металла) в кульке из фильтрованной бумаги.
4. Запишите в таблицу 2.1. массу металла (m).
5. Откройте кулек, отогнув уголок фильтрованной бумаги, смочите его дистиллированной водой с помощью стеклянной палочки, коснувшись бумаги смоченной водой палочкой. Приклейте мокрый уголок кулька к стенке пробирки и с помощью палочки установите кулек над поверхностью кислоты на расстоянии 1-1,5 см. закройте пробирку пробкой с трубкой, соединяющей ее с бюреткой.
6. Проверьте герметичность прибора, подняв сосуд Р на 10-15см выше уровня воды в бюретке, если по истечении 30с. уровень воды в бюретке останется постоянным, прибор герметичен. В противном случае проверить надежность всех соединений, плотнее закрыть пробками бюретку Б и пробирку П.
7. Верните резервуар Р в исходное положение, чтобы вода в бюретке и резервуаре была на одинаковом уровне.
8. Определите уровень воды в бюретке (h1), отметив положение на шкале бюретки нижней границы мениска жидкости.
При определении положения мениска жидкости уровень глаз и мениска над поверхностью стола должны совпадать.
9. Стряхните осторожно пробирку, чтобы кулек упал в кислоту, прикрепите пробирку резиновым кольцом к штативу и оставьте в покое до полного растворения металла и охлаждения пробирки до комнатной температуры.
10. Запишите показания барометра, термометра. Найдите в справочнике величину 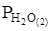 , соответствующую измеренной температуре и занесите в таблицу. Рассчитайте
, соответствующую измеренной температуре и занесите в таблицу. Рассчитайте 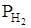 ,
, 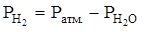 .
.
11. Вернитесь к опытной установке и, убедившись, что реакция закончилась и пробирка не горячая, совместите уровни воды в бюретке и резервуаре; опуская резервуар P, определите уровень воды в бюретке (h2), и запишите в таблицу.
12. Рассчитайте объем выделившегося водорода Vt, как h2-h1.
13. Вычислите 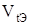 по формуле (2.2).
по формуле (2.2).
Примечание. Заносите значения измеренных и рассчитанных величин в соответствии с точностью их измерений и расчетов, руководствуясь методическими указаниями.
 2014-10-30
2014-10-30 633
633








