Полученные экспериментальные данные изменения температуры системы в процессе эксперимента сводят в таблицу.
По данным, приведенным в таблице, строят график изменения температуры системы от времени (рис. 2).
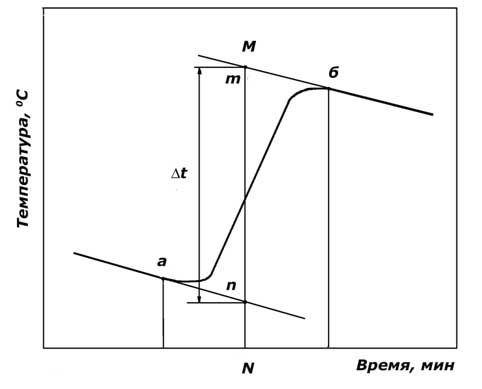
Рис. 3.1 ‑ Изменение температуры системы до начала, в процессе и после завершения химической реакции
При точном выполнении приведенных указаний температура раствора до начала и после завершения химической реакции изменяется прямолинейно. Поэтому через точки, отвечающие этим периодам, проводят прямые линии. Последнюю точку равномерного изменения температуры до начала реакции а
(рис. 3.1) и первую точку равномерного изменения температуры после завершения реакции б (рис. 3.1) проектируют на ось абсцисс. Расстояние между проекциями точек а и б делят пополам, а затем через среднюю точку отрезка а1 б1 проводят ординату NM.
Отрезок МК между точками пересечения ординаты NM с продолжениями прямых равномерного изменения дает истинное значение Δ t, которое измеряют на графике.
Теплоемкость всей системы определяют по формуле
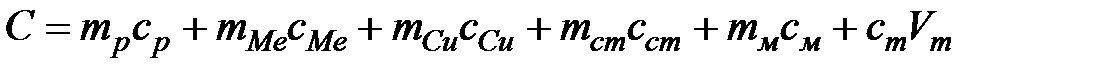 , (3.1)
, (3.1)
где mp – масса раствора, кг;
cр – удельная теплоемкость 0,125Н раствора CuSO4
(cр = 4,021·103 Дж/кг·К), Дж/кг·К;
mМе –масса металла, оставшегося после реакции, кг;
cМе – удельная теплоемкость металла, оставшегося после реакции, Дж/кг·К;
mCu ‑ масса меди, выделившейся в результате реакции, кг;
cCu ‑ удельная теплоемкость меди (cCu = 0,393·103 Дж/кг·К), Дж/кг К;
V - объем погруженной части термометра (4·10-6 м3), м3;
0,46·106 – удельная теплоемкость погружаемой части ртутного термометра, Дж/м3·К.
Массу металла оставшегося после реакции находят по избытку либо недостатку веществ, участвующих в химической реакции.
Теплоту, выделившуюся в системе в результате реакции, находят по формуле (3.2)
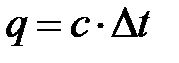 . (3.2)
. (3.2)
Тепловой эффект реакции, отнесенный к 1 мелю прореагировавшего компоненте, вычисляют по уравнению (3.3)
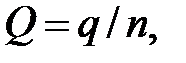 (3.3)
(3.3)
где Q - число молей СиSО4, содержащихся в 250 см3 0,125 Н водного раствора.
 2014-10-30
2014-10-30 322
322








