1. Рассчитать теоретическое содержание меди в образце сульфата меди (%) и содержание меди (%) по данным электрогравиметрического определения.
2. Рассчитать количество электричества (Кл), затраченное на проведение электролиза, теоретическое количество электричества и выход по току.
3. Рассчитать относительную ошибку электрогравиметрического определения меди по формуле
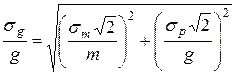 , , |
где sg – абсолютная погрешность массы определяемого вещества; sm – абсолютная погрешность массы пробы (сульфата меди); sp – абсо-лютная погрешность массы весовой формы (меди); g – масса меди, г; m – массса навески пробы, г. Принять sm = sp = 0,0002 г.
Контрольные вопросы
1. В чем сущность электрогравиметрического определения металлов? Обсудите достоинства и недостатки метода.
2. Принципиальная схема установки для электрогравиметрии.
3. Какие требования предъявляются к электродам в этом методе аннализа? Какие химические процессы происходят на катоде и аноде при электролизе растворов CuSO4, KCl, Ni(NO3)2?
4. Напишите уравнение закона Фарадея. Как рассчитать электро-химический эквивалент?
5. Какие металлы не восстанавливаются на катоде из водных раство-ров? Изобразите диаграмму устойчивости воды в координатах «потенциал – рН».
6. Для чего к анализируемому раствору добавляют азотную и серную кислоты? Как рассчитывается процентное содержание меди в исходном кристаллогидрате?
7. Объясните расхождение экспериментального и теоретического содержания меди в кристаллогидрате. Рассчитайте содержание кристалли-зационной воды в моль H2O на моль кристаллогидрата.
8. Как учитывают явления поляризации и перенапряжения в электро-гравиметрии? На чем основан выбор рабочего напряжения и силы тока в данном методе анализа?
9. Объясните ход кривой зависимости тока от времени при электро-лизе раствора сульфата меди при контролируемом потенциале (рис. 2.2).
10. В чем сущность кулонометрического метода анализа?
11. Обсудите принципиальную схему инверсионного анализа с предварительным электролитическим концентрированием.
 2015-01-30
2015-01-30 1149
1149
