| Вещество | Δ G 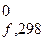 кДж/моль
кДж/моль
| Δ H 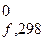 кДж/моль
кДж/моль
| S 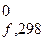 Дж/моль∙К
Дж/моль∙К
|
| Al2(SO4)3 (к) | -3101 | -3442,2 | 239,2 |
| Al2O3 (к) | -1580 | -1674 | 50,94 |
| N2 (г) | 191,5 | ||
| NH3 (г) | -16,7 | -46,9 | 192,5 |
| NH4NO3 (к) | -183,8 | -365,4 | 151,0 |
| NO (г) | 86,7 | 90,37 | 210,6 |
| N2O (г) | 103,6 | 81,5 | 220,0 |
| O2 (г) | 205,0 | ||
| Р (к) | -13,8 | -18,4 | 22,8 |
| PbS (к) | -92,7 | -94,8 | 91,2 |
| PbO (к) | -188,5 | -217,8 | 69,45 |
| S (к) | 31,9 | ||
| SO2 (г) | -300,4 | -296,9 | 248,1 |
| SO3 (г) | -370,4 | -395,2 | 256,23 |
| C (графит) | 5,74 | ||
| C (алмаз) | 2,866 | 1,897 | 2,38 |
| CO (г) | -138,4 | -110,5 | 197,4 |
| CO2 (г) | -394,4 | -396,3 | 213,6 |
| CH4 (г) | -50,5 | -74,85 | 186,19 |
| CH3OH (ж) | -166,1 | -238,6 | 126,8 |
| C2H5OH (ж) | -174,8 | -277,6 | 160,4 |
| CaC2 (к) | -67,8 | -62,7 | 70,3 |
| CaO (к) | -604,2 | -635,1 | 39,70 |
| CaCO3 (к) | -1128,8 | -1206 | 92,90 |
| CaCl2 (к) | -750,2 | -785,8 | 113,8 |
| Cl2 (г) | 223,0 | ||
| Cl2O (г) | 93,0 | 75,7 | 266,2 |
| Fe (к) | 27,15 | ||
| FeO (к) | -244,3 | -263,7 | 58,79 |
| Fe2O3 (к) | -741,5 | -821,32 | 89,92 |
| Fe3O4 (к) | -1014,2 | -1117,1 | 146,2 |
| H2 (г) | 130,6 | ||
| Окончание прилож. 2 | |||
| H2O (ж) | -237,2 | -285,84 | 70,1 |
| H2O (г) | -228,4 | -241,84 | 188,8 |
| H2S (г) | -33,3 | -20,15 | 205,64 |
| HCl (г) | -95,27 | -92,30 | 186,7 |
| HCl (ж) | -131,2 | -167,5 | 55,2 |
| HI (г) | 1,3 | 25,4 | 206,3 |
| HPO3 (ж) | -902,9 | -982,4 | 150,6 |
| I2 (г) | -690,3 | -805,0 | 156,9 |
| MgO (к) | 32,55 | ||
| MgCO3 (к) | -833,8 | -824,7 | 63,14 |
| ZnO (к) | -318,2 | -349,0 | 43,5 |
| ZnS (к) | -239,8 | -201 | 57,7 |
ПРИЛОЖЕНИЕ 3
Стандартные электродные потенциалы электрохимических систем
| Электрохимическая система | 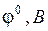
|
MnO2 + 4H+ + 2  = Mn2+ + 2H2O = Mn2+ + 2H2O
| 1,23 |
MnO  + 8H+ + 5 + 8H+ + 5  = Mn2+ + 4H2O = Mn2+ + 4H2O 
| 1,52 |
NO 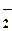 + 2H+ + + 2H+ +  = NO (г) + H2O = NO (г) + H2O
| 1,0 |
I2 + 2  = 2I = 2I 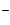
| 0,5355 |
MnO2 + 4H+ + 2  = Mn2+ + 2H2O = Mn2+ + 2H2O
| 1,23 |
S2- - 2  = S0 = S0
| -0,48 |
Cr2O 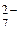 + 14H+ + 6 + 14H+ + 6  = 2Cr3+ + 7H2O = 2Cr3+ + 7H2O
| 1,33 |
Fe2+ -  = Fe3+ = Fe3+
| 0,771 |
ClO   + 6H+ + 6 + 6H+ + 6  = Cl = Cl  + 3H2O + 3H2O
| 1,45 |
SO 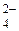 + 8H+ + 8 + 8H+ + 8  = S2- + 4H2O = S2- + 4H2O
| 0,149 |
SO2 + 2H2O - 2  = SO = SO  + 4H+ + 4H+
| 0,138 |
NO  + 2H+ + + 2H+ +  = NO2 (г) + H2O = NO2 (г) + H2O
| 0,80 |
NO  + 4H+ + 3 + 4H+ + 3  = NO (г) + 2H2O = NO (г) + 2H2O
| 0,957 |
2Br 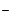 - 2 - 2  = Br2 = Br2
| 1,07 |
MnO  + 1 + 1  = MnO = MnO 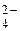
| 0,564 |
2Cl 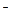 - 2 - 2  = Cl2 = Cl2
| 1,359 |
NO  + 3H+ + 2 + 3H+ + 2  = HNO2 + H2O = HNO2 + H2O
| 0,960 |
PbO2 + 4H+ + 2  = Pb2+ + 2H2O = Pb2+ + 2H2O
| 1,682 |
2IO  + 12H+ + 10 + 12H+ + 10  = I2 + 6H2O = I2 + 6H2O
| 1,195 |
Ti4+ +  = Ti3+ = Ti3+
| -0,04 |
Pb2+ + 2  = Pb0 = Pb0
| -0,126 |
Cr3+ + 3  = Cr0 = Cr0
| -0,744 |
Mn2+ + 2  = Mn0 = Mn0
| -1,180 |
Co2+ + 2  = Co0 = Co0
| -0,277 |
Fe2+ + 2  = Fe0 = Fe0
| -0,44 |
Cd2+ + 2  = Cd0 = Cd0
| -0,4029 |
Cu2+ + 2  = Cu0 = Cu0
| 0,337 |
Sn2+ + 2  = Sn0 (белый) = Sn0 (белый)
| -0,136 |
Au3+ + 3  = Au0 = Au0
| 1,498 |
| Окончание прилож. 3 | |
Mg2+ + 2  = Mg0 = Mg0
| -2,363 |
Zn2+ + 2  = Zn0 = Zn0
| -0,763 |
Al3+ + 3  = Al0 = Al0
| -1,662 |
Ag+ +  = Ag0 = Ag0
| 0,799 |
Sb3+ + 3  = Sb0 = Sb0
| 0,24 |
Pd2+ + 2  = Pd0 = Pd0
| 0,987 |
Sn4+ + 2  = Sn2+ = Sn2+
| 0,009 |
Cr2+ + 2  = Cr0 = Cr0
| -0,913 |
Ni2+ + 2  = Ni0 = Ni0
| -0,25 |
In3+ + 3  = In0 = In0
| -0,343 |
Fe3+ + 3  = Fe0 = Fe0
| -0,036 |
2H+ + 2  = H2 = H2
| |
Li+ +  = Li0 = Li0
| -3,045 |
 2014-10-30
2014-10-30 413
413







