5.1.1 Момент импульса электрона в атоме (правило отбора стационарных орбит)
mu r = n 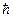 ,
,
где n = 1,2,3, … 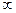 . – главное квантовое число.
. – главное квантовое число.
5.1.2 Радиус n -ой стационарной орбиты атома водорода
rn = a1 n2,
где а1 – радиус первой боровской орбиты (радиус Бора)
5.1.3 Скорость электрона на п – ой орбите
uп = u1 / п,
где u1 – скорость электрона на первой орбите
5.1.4 Энергия ионизации атома водорода
Еi = R h c,
где R = 1,10.107 м-1 – постоянная Ридберга
5.1.5 Энергия электрона в атоме водорода
Еn = Е1 / п2
где Е1 – энергия электрона на первом энергетическом уровне
5.1.6 Энергия, излучаемая или поглощаемая атомом (второй постулат Бора)
e = 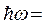
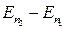 или e = Еi (
или e = Еi (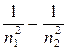 )
)
5.1.7 Сериальная формула для спектральных линий, излучаемых или поглощаемых атомом водорода или водородоподобными ионами с зарядом ядра Z при переходе с одного стационарного уровня с главным квантовым числом n 2 на другой стационарный уровень с главным квантовым числом n 1
n = Z 2Rc 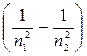 или
или 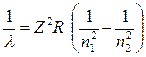
5.1.8 Коротковолновая граница сплошного рентгеновского спектра
λmin=hc / | e |U
5.1.9 Закон Мозли
а) в общем случае
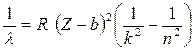
б) для К α – линий
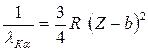
5.1.10 Энергия фотона К α – линии рентгеновского излучения
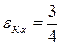 Еi (Z b)2
Еi (Z b)2
 2015-01-30
2015-01-30 474
474








