5.2.1 Задача 1. Электрон в ионе Li++ перешел с четвертого энергетического уровня на второй. Определить энергию испущенного при этом фотона.
| Дано: Z =3 n 2=4 n 1=2 | Решение: Для определения энергии фотона воспользуемся сериальной формулой для водородоподобных ионов: 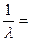 RZ 2 RZ 2 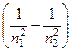 , (5.1) , (5.1) |
| e -? |
где l - длина волны фотона; R – постоянная Ридберга; Z – заряд ядра в относительных единицах; n 1 – номер орбиты, на которую перешел электрон; n 2 - номер орбиты, с которой перешел электрон (n 1 и n 2 – главные квантовые числа).
Энергия фотона e выражается формулой
e = hn =h 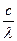 .
.
Умножив обе части формулы (5.1) на hc, получим:
e =R hcZ2 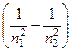 ,
,
Так как. Rhc есть энергия ионизации Еi атома водорода, то
e = Еi Z2 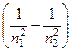 . (5.2)
. (5.2)
Подставим числовые значения и произведем расчеты. Еi возьмем из справочной табл. 1 во внесистемной единице: Еi= 13,6 эВ.
e = 13,6×32 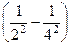 = 22,95 эВ.
= 22,95 эВ.
Ответ: e =22,95 эВ.
5.2.2 Задача 2. Используя теорию Бора для атома водорода, определить радиус ближайшей к ядру орбиты (первый боровский радиус) и скорость движения электрона по этой орбите.
| Дано: n = 1 Z = 1 | Решение: В атоме на электрон со стороны ядра действует кулоновская сила притяжения, которая играет роль центростремительной силы: 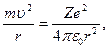 (5.3) (5.3) |
| r l-? υ l-? |
где m и e соответственно масса и заряд электрона, Ze – заряд ядра, υ и r –
скорость движения электрона по орбите и радиус орбиты, ε0 – электрическая постоянная.
Из множества орбит, удовлетворяющих уравнению (5.3), выберем стационарные орбиты. Для этого воспользуемся правилом квантования (отбора) орбит:
mυr = nћ, (5.4)
где п – главное квантовое число, в теории Бора соответствует номеру
стационарной орбиты; ћ= h / 2π – приведённая постоянная Планка.
По условию задачи Z = 1, п= 1 и уравнения (5.3) и (5.4) примут вид:
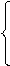
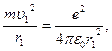
mυ1 r1 = ћ (5.5)
Решая систему уравнений (5.5), получим:
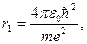 (5.6)
(5.6)
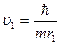 . (5.7)
. (5.7)
Проверим единицы r1 и υ1:
[ r1 ] = 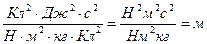 ,
,
[ υ1 ] = 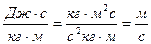 .
.
Единицы r1 и υ1 верны, следовательно, верны и формулы (5.6) и (5.7). Подставим числовые значения и произведём расчёты:
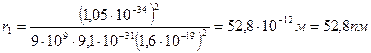
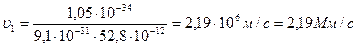
Ответ: r1 = 52,8пм; υ1 = 2,19 Мм/с.
5.2.3 Задача 3. Определить длину волны λКα энергию εКα фотона Кα – линии рентгеновского спектра, излучаемого вольфрамом при бомбардировке его быстрыми электронами.
Дано: k = 1 n = 2 Z =74 | Решение: При бомбардировке вольфрама быстрыми электронами возникает характеристическое рентгеновское излучение, имеющее линейчатый спектр. Быстрые электроны, проникая внутрь электронной оболочки атома, выбивают электроны, принадлежащие электронным слоям. Если за пределы атома выбивается один из двух электронов ближайшей к ядру К – оболочки, то на освободившееся место переходит один из электронов вышележащих слоёв (L, M, N). | |||
| λКα -? εКα -? |
При этом возникает соответствующая линия К – серии. Наиболее интенсивная линия этой серии Кα возникает при переходе электрона из L - слоя
(п = 2) в К – слой (k = 1). Поэтому длина волны этой линии в соответствии с законом Мозли определится по формуле:
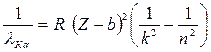 =
= 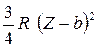 , (5.8)
, (5.8)
где R = 1,1. 107 м-1 – постоянная Ридберга, Z = 74 – атомный номер вольфрама, b- постоянная экранирования (для К – серии b = 1). Из формулы (5.8)
получим:
λКα = 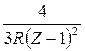 .
.
Подставим числовые значения и произведём расчёт:
λКα = 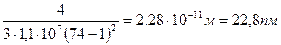
Энергию фотона α – серии определим по формуле:
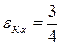 Еi (Z - b)2, (5.9)
Еi (Z - b)2, (5.9)
где Еi – энергия ионизации атома водорода, Еi = 2,18.10-18 Дж (см. табл. 1). Подставим в формулу (5.9) числовые значения и произведём расчёт:
εКα = 0,75 . 2,18 . 10-18 (74 - 1)2 = 8,713.10-15Дж = 54,5 кэВ
Ответ: λКα = 22,8 пм, εКα = 54,5 кэВ.
 2015-01-30
2015-01-30 3639
3639

