491. Что такое водородный показатель (рН)? Числовые значения рН в кислом, щелочном и нейтральном растворах. Вычислите рН 0,1н. раствора хлороводородной кислоты.
492. Что называется произведением растворимости? Вычислите 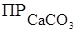 , зная, что растворимость этой соли при данной температуре равна 0,013 г/л.
, зная, что растворимость этой соли при данной температуре равна 0,013 г/л.
493. Как влияет введение сильного электролита, содержащего одноименный ион, на растворимость малорастворимого электролита? Во сколько раз изменится растворимость сульфата бария в присутствии 0,1М раствора сульфата калия, если 
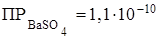 ?
?
494. Какие растворы называются буферными? Приведите примеры буферных растворов. Почему рН буферных растворов практически не изменяется при добавлении к ним небольших количеств сильных кислот или щелочей?
Определите рН аммонийного буферного раствора, если известен состав этого буфера: 0,1М NH4OH; 0,1М NH4Cl. Как изменится рН, если к 1 л буферного раствора добавить 0,001 моль хлороводородной кислоты и если разбавить буферный раствор в 5 раз?
495. Сформулируйте условия образования осадков. Получится ли осадок сульфата кальция при смешении равных объемов 0,01 М растворов CaCl2 и Na2SO4, если ПР 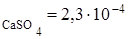 ?
?
496. Сформулируйте условия растворения осадков. Выпадет ли осадок сульфата стронция при смешении равных объемов 0,005 М растворов SrCl2 и K2SO4, если 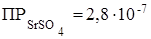 ?
?
497. Сформулируйте условия образования осадков. Образуется ли осадок оксалата кальция (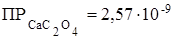 ) при смешении равных объемов 0,01М растворов CaCl2 и Na2C2O4?
) при смешении равных объемов 0,01М растворов CaCl2 и Na2C2O4?
498. Сформулируйте правило растворения осадков. Образуется ли осадок сульфата бария при смешении равных объемов 0,0005М растворов BaCl2 и K2SO4, если 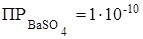 ?
?
499. Сформулируйте понятие произведения растворимости. Вычислите произведение растворимости карбоната магния при комнатной температуре, если растворимость его в этих условиях равна 0,01 г в 100 мл раствора.
500. Как влияет добавление сильного электролита, содержащего одноименный ион на растворимость осадка? Произведение растворимости сульфата серебра Ag2SO4 равно 7×10-5. Рассчитайте растворимость соли и выразите ее в молях на литр и в граммах на литр.
501. Напишите выражения произведения растворимости для BaSO4, Ca3(PO4)2, Ag2CrO4. Вычислите произведение растворимости CaSO4, если 1л насыщенного раствора его содержит 1,5×10-2 моль соли.
502. Напишите выражение для константы диссоциации воды. Что показывает ионное произведение воды? Каково его численное значение? Определите характер среды растворов, если: а) [H+] = 10-9 моль/л; б) рН = 4; в) [OH-] = 10-6моль/л; г) рОН = 12
503. Какие растворы называются буферными? Приведите примеры буферных растворов. Почему рН буферных растворов не зависит от разбавления? Определите рН ацетатного буферного раствора, если известен состав этого буфера: 1М CH3COOH; 0,1M CH3COONa. Как изменится рН, если к 1 л буферного раствора добавить 0,01 моль хлороводородной кислоты и если разбавить буферный раствор в 20 раз?
504. Сформулируйте правило произведения растворимости. Вычислите произведение растворимости BaCrO4, если в 1 л насыщенного раствора его содержится 3,9×10-3 г хромата бария.
505. Как измеряют рН раствора в ходе анализа? Приведите примеры индикаторов. Вычислите рН 0,05 М раствора хлороводородной кислоты.
506. Напишите выражение произведения растворимости для сульфита кальция. Рассчитайте растворимость CaSO3 в воде и в 0,2 М растворе Na2SO3, если 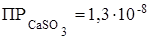 .
.
507. Как влияет введение сильного электролита, содержащего одноименный ион, на растворимость малорастворимого электролита? Во сколько раз изменится растворимость оксалата кальция CaC2O4 в присутствии 0,01 моль Na2С2O4 в 1 л раствора, если 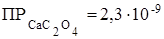 .
.
508. Сформулируйте условия образования и растворения осадков. Вычислите произведение растворимости Mg(OH)2, если в 1 л насыщенного раствора его содержится 6,4×10-3 г гидроксида магния.
509. Как изменится концентрация ионов водорода в растворе уксусной кислоты CH3COOH при добавлении ацетата натрия NaCH3COO? Вычислите концентрацию катионов водорода [H+] и рН 0,1М раствора уксусной кислоты, если K 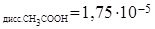 .
.
510. Как изменится концентрация ионов ОН - в растворе гидроксида аммония при добавлении хлорида аммония? Вычислите концентрацию гидроксид-ионов [OH - ] и рОН 0,2М раствора гидроксида аммония, если K 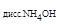 =1,75×10-5.
=1,75×10-5.
 2015-01-30
2015-01-30 914
914








