Идеа́льный газ – это модель газа в которой 1)собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда. 2)между молекулаи газа отсутствуют силы взаимодействия 3)столкновение молекул газа между собой и со стенками сосуда абсолютно упругие.
Уравнение состояния идеального газа — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид: 
, где:
p — давление,
Vμ — молярный объём,
T — абсолютная температура,
R — универсальная газовая постоянная.
Так как, 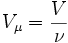 где ν — количество вещества, а, где m — масса, μ — молярная масса, уравнение состояния можно записать:
где ν — количество вещества, а, где m — масса, μ — молярная масса, уравнение состояния можно записать:
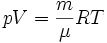 Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Уравнение можно записать в виде:
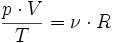

Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
— закон Бойля — Мариотта 
— закон Гей-Люссака 
— закон Шарля 
 2015-01-30
2015-01-30 581
581








