§ Уравнение состояния идеального газа
Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона) связывает давление (р), объём (V) и температуру (T) идеального газа произвольной массы (m), в данном состоянии идеального газа.
 ,
,
где M – молярная масса, R – универсальная газовая постоянная.
§ Уравнение Клапейрона
Переход данной массы идеального газа из одного состояния в другое подчиняется соотношению
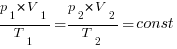
§ Закон Бойля-Мариотта (изотермический процесс)
Для газа данной массы при переходе из одного состояния в другое при постоянной температуре (T) произведение давления (р) газа на его объём (V) не меняется.
 , (при T=const)
, (при T=const)
§ Закон Гей-Люссака (изобарный процесс)
Для газа данной массы при переходе из одного состояния в другое при постоянном давлении (р) отношение объёма (V) к абсолютной температуре (T) есть величина постоянная для всех газовых состояний.
 , (при p=const)
, (при p=const)
§ Закон Шарля (изохорный процесс)
Для газа данной массы при переходе из одного состояния в другое при постоянном объёме (V) отношение давления (р) к абсолютной температуре (T) есть величина постоянная для всех газовых состояний.
 , (при p=const)
, (при p=const)
§ Закон Дальтона
Для разреженных (идеальных) газов давление (р) смеси равно сумме парциальных давлений (р1, р2,… рn) компонентов смеси.

СИ: Па
 2015-01-30
2015-01-30 410
410








