Коллоидный раствор можно получить обменной реакцией. Рассмотрим образование иодида серебра при сливании разбавленных растворов нитрата серебра и иодида калия:
AgNO3 + KI = AgI + KNO3,
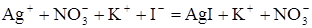 .
.
Если иодид калия и нитрат серебра взяты в эквивалентных количествах, частицы AgI растут, достигая размеров, превосходящих размеры коллоидных частиц, и быстро выпадают в осадок. Если же реакцию проводят с разбавленными растворами, то осадок не выпадает, а образуется коллоидный раствор иодида серебра. Основную массу мицеллы составляет ядро – мельчайший кристаллик иодида серебра, состоящий из большого числа молекул: m(AgI).
Полученное ядро является носителем свободной поверхностной энергии, поэтому на его поверхности идет адсорбционный процесс. Согласно правилу Пескова – Фаянса, на поверхности ядра мицеллы адсорбируются ионы, имеющиеся в составе ядра, т.е. адсорбируются ионы, находящиеся в избытке. Если получать раствор при избытке иодида калия, то адсорбироваться будут ионы иода. Ионы иода достраивают кристаллическую решетку ядра, образуя адсорбционный слой, и придают ядру отрицательный заряд: m[AgI]nI־. Эти ионы, адсорбирующиеся на поверхности ядра и придающие ему заряд, называются потенциалопределяющими ионами.
В растворе находятся также ионы противоположные по знаку потенциалопределяющим ионам, их называют противоионами. В данном случае это катионы К+, которые электростатически притягиваются потенциалопределяющими ионами адсорбционного слоя, образуя гранулу:
{ m [AgI] n I־ (n – x)K+}x־
г р а н у л а
В адсорбционном слое гранулы преобладают потенциалопределяющие ионы I־, число которых можно обозначить n, а количество противоионов K+– (n - x). Оставшаяся часть противоионов образует диффузный слой ионов. Ядро с адсорбционным и диффузным слоями называется мицеллой:
{ m [AgI] n I־ (n - x)K+}x־ x K+
м и ц е л л а
Если получать золь иодида серебра при избытке нитрата серебра, т.е. при избытке Ag+, то коллоидная частица благодаря адсорбции ионов Ag+ на поверхности ядра получит положительный заряд.
{ m [AgI] n Ag+(n - x)NO3}x+ x NO3 (гранула положительна)
{ m [AgI] n I־(n - x)K+}x־ x K+ (гранула отрицательна)
Числа m, n, x в зависимости от условий приготовления золей могут меняться в широких пределах, т.е. мицелла не имеет строго определенного состава.
Таким образом, мицелла – электрически нейтральная коллоидная частица, способная к самостоятельному существованию. Она определяет все основные свойства коллоидной системы. Состоит мицелла из ядра кристаллического или аморфного строения, адсорбционного (неподвижного относительно частицы) и диффузного (подвижного) слоев. При пропускании постоянного тока через коллоидный раствор к электродам движутся не мицеллы, которые электронейтральны, а только гранулы.
Золь — высокодисперсный коллоидный раствор. Размер частиц дисперсной фазы 10-9 — 10-6м.
Золи обладают рядом специфических свойств, которые подробно изучает коллоидная химия. Золи в зависимости от размеров частиц могут иметь различную окраску, а у истинных растворов она одинаковая. Например, золи золота могут быть синими, фиолетовыми, вишневыми, рубиново-красными.
В отличие от истинных растворов для золей характерен эффект Тиндаля, т. е. рассеяние света коллоидными частицами. При пропускании через золь пучка света появляется светлый конус, видимый в затемненном помещении. Так можно распознать, является данный раствор коллоидным или истинным.
Для осаждения золя необходимо, чтобы его частицы соединились в более крупные агрегаты. Соединение частиц в более крупные агрегаты называется коагуляцией, а осаждение их под влиянием силы тяжести — седиментацией.
Обычно коагуляция происходит при прибавлении к золю: 1) электролита,2) другого золя, частицы которого имеют противоположный заряд, и 3) при нагревании.
При определенных условиях коагуляция золей приводит к образованию студенистой массы, называемойгелем. В этом случае вся масса коллоидных частиц, связывая растворитель, переходит в своеобразное полужидкое-полутвердое состояние. От гелей следует отличать студни — растворы высокомолекулярных веществ в низкомолекулярных жидкостях (системы гомогенные). Их можно получить при набухании твердых полимеров в определенных жидкостях.
Значение золей исключительно велико, так как они более распространены, чем истинные растворы.
Наличие одноименного заряда у всех частиц золя является фактором его устойчивости. Заряд препятствует слипанию и укрупнению коллоидных частиц, т.е. коагуляции. Стабильность (устойчивость) коллоидных частиц объясняется тем, что на поверхности ядер адсорбируется определенный вид потенциалопределяющих ионов. Те электролиты, ионы которых являются потенциалопределяющими, следует считать стабилизаторами, а ионы, которые адсорбируются поверхностью ядер, - стабилизирующими ионами. При этом на ядре адсорбируются те ионы стабилизатора, которые содержат элементы, общие с ядром.
 2015-01-30
2015-01-30 1665
1665
