1. Внутреннее строение и физические свойства атомов, молекул и их более сложных объединений
2. Понятие о теории Бора.
3. Химическая связь
4. Энергетические уровни атомов
5. Энергетические уровни молекул
6. Основные направлений исследований атомов и молекул
7. Экспериментальные методы при изучении атомов и молекул
перерыв - 10 мин
Методы обучения и преподавания:
- разбор и обсуждение основных вопросов
- решение типовых и ситуационных задач
- тестирование
- исправления ошибок
Методы контроля формируемых на занятии компетенций:
- - тестирование на компьютере (студент должен ответить на «тест», содержащий в себе минимальные знания и навыки – основные определения, теоретические вопросы данной темы);
- проверка правильности решенных задач
Самостоятельная работа студентов - 30 мин
· Объяснить содержания и находить пути решения поставленных задач
· Преобразовывать формул и перевести единицу измерения физических величин
Задачи для решения:
1. Длительность возбужденного состояния атома водорода соответствует примерно
10-8с. Чему равна неопределенность 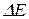 энергетического уровня при этом?
энергетического уровня при этом?
2. Найдите энергию и момент импульса электрона в атоме водорода, соответствующие состоянию 1s, 2s, 2p.
3. Найдите проекции момента импульса электрона на направление индукции магнитного поля, соответствующие 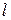 =2.
=2.
4. Найти ридберговскую поправку для 3Р-терма атома натрия, первый потенциал возбуждения которого 2,1В, а энергия связи валентного электрона в основном 3S-состоянии 5,14эВ.
5.Найти энергию связи валентного электрона в основном состоянии атома лития, если известно, что длина волны головной линии резкой серии 813нм и коротковолновой границы этой серии 350нм.
 2015-01-07
2015-01-07 687
687








