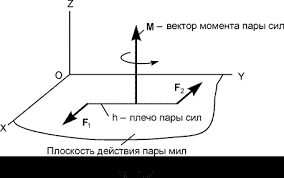
Расчёт состоит из следующих этапов:
1) расчёт константы равновесия в стандартных условиях;
2) пересчёт значений константы равновесия к заданным условиям;
3) определение равновесных концентраций веществ.
1. На первом этапе в методе расчёта, основанном на использовании стандартных термодинамических величин, применяют два исходных уравнения:
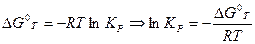
и 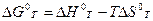 .
.
Расчёт 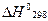 и
и 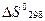 проводят по известным соотношениям следствий из закона Гесса:
проводят по известным соотношениям следствий из закона Гесса:
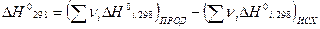 .
.
Аналогично рассчитываем 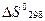 .
.
По величине и знаку 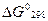 судят о возможности полученных продуктов реакции из исходных веществ в стандартных условиях.
судят о возможности полученных продуктов реакции из исходных веществ в стандартных условиях.
2. На втором этапе переходит от значения 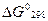 к
к 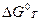 , используя уравнение Кирхгофа:
, используя уравнение Кирхгофа:
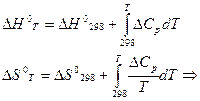
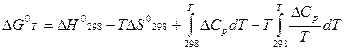 .
.
После подстановки степенного ряда зависимости 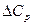 = f(T), интегрирования и преобразований, получаем уравнение вида:
= f(T), интегрирования и преобразований, получаем уравнение вида:
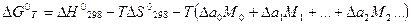 ,
,
где М0, М1, М2 – функции Темкина-Шварцмана, приведённые в соответствующих таблицах справочника физико-химических величин.
Константу равновесия можно рассчитать для стандартных условий, используя уравнение
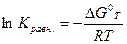
и пересчитать для температуры, используя уравнение изобары или изохоры химических реакций.
Определение константы равновесия с помощью температурных функций Тёмкина-Шварцмана называется методом Тёмкина-Шварцмана по имени составителей таблиц. В результате второй стадии рассчитано 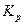 , известно общее давление.
, известно общее давление.
3. На третьей стадии определяем состав равновесной смеси в моль или молярных долях.
Пример: Определить состав равновесной смеси при взаимодействии этилена и хлорводорода.
 2014-05-17
2014-05-17 5948
5948