Если в систему, состоящую из двух взаимно нерастворимых и химически не взаимодействующих жидкостей, ввести третий компонент, способный растворяться в этих жидкостях, то он, растворяясь в них, распределяется между ними совершенно определенным образом. В результате образуется трехкомпонентная двухфазная система. Первая фаза (I) представляет собой раствор третьего компонента в первой жидкости, а вторая фаза (II) – во второй.
Закон распределения третьего компонента между двумя несмешивающимися фазами можно вывести из условия равновесия в гетерогенной системе. Этим условием является равенство химических потенциалов каждого компонента во всех фазах, образующих данную систему.
Для третьего компонента в двухфазной системе условие равновесия между фазами I и II выражается равенством:
| μ3I = μ3II. | (1) |
Подставим в равенство уравнение связи химического потенциала i-того компонента системы с его концентрацией С, считая растворы разбавленными
| μi = μi0 + RTlnCi, | (2) |
где μi - химический потенциал i-того компонента; μi0 -стандартный химический потенциал i-того компонента, равный μi при единичной концентрации i-того компонента Ci; R – универсальная газовая постоянная; Т – абсолютная температура.
После подстановки равенство (1) принимает вид:
| μ30,I + RTlnC3I = μ30,II + RTlnC3II | (3) |
или
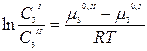 | (4) |
Правая часть уравнения (4) является величиной постоянной, если температура постоянная. Отсюда
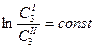
при T = const и, следовательно
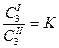 | (5) |
где К – коэффициент или константа распределения.
Таким образом, закон распределения читается так: отношение концентрации третьего компонента в двух равновесных жидких фазах (I и II) при постоянной температуре является величиной постоянной, не зависящей от количества введенного в систему третьего компонента (при условии, что образовавшиеся растворы можно считать разбавленными).
Если количество введенного третьего компонента достаточно велико и образовавшиеся при его растворении растворы нельзя считать разбавленными (идеальными), то закон распределения записывают аналогично, но вместо равновесных концентраций нужно поставить активности, то есть
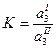 | (6) |
Соотношения (5) и (6) справедливы, если третье вещество при растворении в I и II растворителях не диссоциирует и не ассоциирует, то есть не изменяет своего молекулярного состояния. Если же последнее происходит, то закон распределения записывают в виде
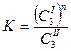 | (7) |
где 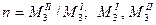 – средняя молекулярная масса третьего вещества в I и II растворителях соответственно.
– средняя молекулярная масса третьего вещества в I и II растворителях соответственно.
 2014-05-17
2014-05-17 4471
4471








