1. Найдите молярную массу эквивалента двух металлов по следующим экспериментальным данным: навеска первого металла массой 2.0000 г. и навеска второго массой 1.0582 г. образуют оксиды массой, соответственно равной 2.5036 и 2.0000 г.
2. Олово образует два оксида. Первый содержит 78.8%, второй - 88.2% олова. Вычислите молярные массы эквивалентов олова в этих соединениях.
3. Мышьяк образует два оксида с массовыми долями мышьяка 0.652 и
0.758. Определите молярные массы эквивалентов мышьяка в этих оксидах.
4. Элемент образует гидрид с массовой долей водорода 0.887. Вычислите молярную массу эквивалента элемента.
5. В оксиде металла 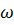 (0) = 0.286. В его же соединении со фтором
(0) = 0.286. В его же соединении со фтором 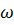 (F) = 0.487. Определите молярную массу эквивалента фтора.
(F) = 0.487. Определите молярную массу эквивалента фтора.
6. При горении фосфора в недостатке кислорода на 6.2 г фосфора расходуется 3.36 л кислорода, а в избытке 5.60 л. Рассчитайте 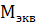 фосфора в полученных соединениях. Как относятся эквиваленты друг к другу?
фосфора в полученных соединениях. Как относятся эквиваленты друг к другу?
7. Одно и то же количество металла соединяется с 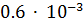 кг кислорода и
кг кислорода и 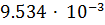 кг галогена. Рассчитайте молярную массу эквивалента металла.
кг галогена. Рассчитайте молярную массу эквивалента металла.
8. На восстановление 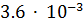 кг оксида металла израсходовано
кг оксида металла израсходовано 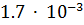
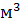 водорода (н.у.). Рассчитайте молярную массу эквивалента металла.
водорода (н.у.). Рассчитайте молярную массу эквивалента металла.
9. Анализом установлено, что массовая доля углерода в соединении с водородом составляет 0.75. Какова молярная масса эквивалента углерода и его валентность?
10. Чему равен при н.у. молярный объем эквивалента водорода? Вычислите молярную массу эквивалента металла, если на восстановление 1.017г его оксида израсходовалось 0.28 л водорода (н.у.).
11. При растворении в кислоте металла массой 11.9 г выделился водород объемом 2.24 л (н.у.). Чему равны 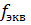 и
и 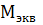 для этого металла?
для этого металла?
12. Металл массой 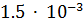 кг вытесняет из раствора никель массой
кг вытесняет из раствора никель массой 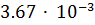 кг, а из раствора кислоты - водород объемом 1
кг, а из раствора кислоты - водород объемом 1 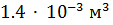 (н.у.). Определите молярную массу эквивалента никеля.
(н.у.). Определите молярную массу эквивалента никеля.
13. Кальций массой 0.69 г и цинк массой 1.13 г вытесняют из кислоты одинаковые количества водорода. Определите молярную массу эквивалента цинка, зная, что молярная масса эквивалента кальция 20 г/моль.
14. Алюминий массой 0.752 г при взаимодействии с кислотой вытеснил водород объемом 0.936 л (н.у.). Определите молярный объем эквивалента водорода. Молярная масса эквивалента алюминия 8.99 г/моль.
15. На нейтрализацию 245 г 10% раствора 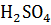 пошло 20 г NaOH. Вычислите молярную массу эквивалента серной кислоты.
пошло 20 г NaOH. Вычислите молярную массу эквивалента серной кислоты.
16. Вычислить 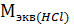 , если известно, что при полном взаимодействии цинка с 66.4 мл 20 % раствора соляной кислоты расходуется 13 г цинка, а то же количество цинка, в свою очередь, реагируя с кислородом, дает 16.2 г оксида цинка.
, если известно, что при полном взаимодействии цинка с 66.4 мл 20 % раствора соляной кислоты расходуется 13 г цинка, а то же количество цинка, в свою очередь, реагируя с кислородом, дает 16.2 г оксида цинка.
17. В лаборатории имеются два различных хлорида железа. Их анализ показал, что в одной соли содержится 34.5 % железа, в другой - 44.1%. Определите молярные массы эквивалента железа в этих соединениях, если известно, что 2.24 л (н.у.) хлора соединяются с 2.24 л (н.у.) водорода. Как относятся 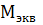 друг к другу?
друг к другу?
18. Определите 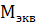 алюминия и количество выделившегося газа, если известно, что для растворения 5.4 г алюминия потребовалось 99.6 мл 20-% раствора соляной кислоты.
алюминия и количество выделившегося газа, если известно, что для растворения 5.4 г алюминия потребовалось 99.6 мл 20-% раствора соляной кислоты.
19. На нейтрализацию 0.943 г фосфористой кислоты 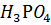 израсходовано 1.291 г КОН. Вычислите эквивалент, молярную массу эквивалента, основность кислоты. На основании расчета напишите уравнение реакции.
израсходовано 1.291 г КОН. Вычислите эквивалент, молярную массу эквивалента, основность кислоты. На основании расчета напишите уравнение реакции.
20. Из 3.85 г нитрата металла получено 1.60 г его гидроксида. Вычислите молярную массу эквивалента металла.
21. Из 1.35 г оксида металла получается 3.15 г его нитрата. Вычислите молярную массу эквивалента этого металла.
22. Для растворения 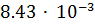 кг металла потребовалось 0.147 кг раствора с массовой долей
кг металла потребовалось 0.147 кг раствора с массовой долей 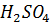 0.05. Рассчитайте молярную массу эквивалента металла и объем выделившегося водорода (н.у.).
0.05. Рассчитайте молярную массу эквивалента металла и объем выделившегося водорода (н.у.).
23. Какая масса цинка потребуется для вытеснения меди из раствора, содержащего 0.1 молярной массы эквивалента 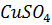
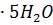 .
.
24. Избытком хлороводородной (соляной) кислоты подействовали на растворы:
а) гидрокарбоната кальция;
б) хлорида гидроксоалюминия.
Напишите уравнения реакций этих веществ с НСl и определите их молярные массы эквивалентов.
25. Напишите уравнения реакций 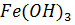 с хлороводородной кислотой прикоторых образуются следующие соединения железа:
с хлороводородной кислотой прикоторых образуются следующие соединения железа:
а) хлорид дигидроксожелеза (III);
б) хлорид гидроксожелеза (III);
в) хлорид железа(III).
Вычислить фактор эквивалентности и молярную массу эквивалента 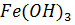 в каждой из этих реакций.
в каждой из этих реакций.
 2015-01-13
2015-01-13 1351
1351








