1. Кристаллическая сода 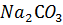
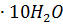 какой массы потребуется для приготовления раствора объемом 12 л, если его:
какой массы потребуется для приготовления раствора объемом 12 л, если его:
а) молярная концентрация равна 0.2 моль/л;
б) эквивалентная концентрация равна 0.2 моль/л?
2. Медный купорос 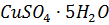 какой массы потребуется для приготовления раствора объемом 2 л, содержащего
какой массы потребуется для приготовления раствора объемом 2 л, содержащего 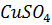 количеством вещества 0.5 моль? Какова молярная концентрация полученного раствора?
количеством вещества 0.5 моль? Какова молярная концентрация полученного раствора?
3. Чему равны массы хлорида бария безводного и кристаллогидрата 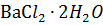 , которые надо взять для приготовления раствора(
, которые надо взять для приготовления раствора(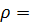 1.072г
1.072г 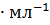 ) объемом 1.5 л, в котором
) объемом 1.5 л, в котором 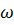 (
(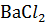 ) = 0.08? Какой объем воды потребуется в том и другом случае?
) = 0.08? Какой объем воды потребуется в том и другом случае?
4. Какие массы безводного сульфата меди и медного купороса потребуются для приготовления раствора (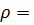 1.084 г
1.084 г 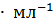 ) объемом 1 л, для которого
) объемом 1 л, для которого 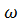 (
(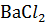 ) = 0.08?
) = 0.08?
5. Определите эквивалентную концентрацию 8-процентного раствора гидроксида натрия (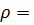 1.092 г
1.092 г 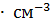 ).
).
6. Определите нормальную концентрацию 10-процентного раствора серной кислоты (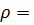 1.07 г
1.07 г 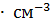 ).
).
7. Сколько миллилитров 96-процентного (по массе) раствора 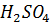
(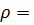 1.84 г
1.84 г 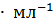 ) нужно взять для приготовления 1 л 0.25Н раствора?
) нужно взять для приготовления 1 л 0.25Н раствора?
8. Плотность 40-процентного (по массе) раствора 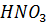 равна 1.25 г
равна 1.25 г 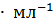
Рассчитать молярность, моляльность этого раствора.
9. Вычислите массовую долю 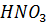 в растворе и моляльность 8Н раствора
в растворе и моляльность 8Н раствора 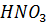 , плотность которого равна 1246 г
, плотность которого равна 1246 г 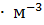 .
.
10. Какой объем раствора гидроксида калия с массовой долей КОН 24% (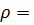 1218 г
1218 г 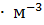 ) можно приготовить из 125 л раствора гидроксида калия с массовой долей КОН 0.48 (
) можно приготовить из 125 л раствора гидроксида калия с массовой долей КОН 0.48 (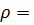 1510 г
1510 г 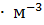 )?
)?
11. Определите эквивалентную концентрацию, моляльность и массовую долю 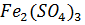 в растворе, если плотность раствора равна 1000 г
в растворе, если плотность раствора равна 1000 г 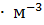 .
.
12. Какой объем 5Н раствора NaOH можно приготовить из 4 л раствора гидроксида натрия с массовой долей NaOH 0.50 (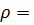 1510 г
1510 г 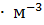 )?
)?
13. Плотность 15-процентного (по массе) раствора 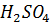 равна 1105 г
равна 1105 г 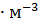 . Вычислите нормальность, молярность, моляльностъ раствора.
. Вычислите нормальность, молярность, моляльностъ раствора.
14. Из 3 л раствора с массовой долей КОН 0.50 и плотностью 1.09 г 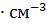 нужно приготовить раствор с массовой долей КОН 0.10 (
нужно приготовить раствор с массовой долей КОН 0.10 (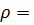 1.09 г
1.09 г 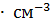 ). Сколько воды нужно взять для приготовления указанного раствора?
). Сколько воды нужно взять для приготовления указанного раствора?
15. Из 5 л раствора гидроксида калия с массовой долей КОН 0.50 и плотностью 1538 г 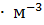 надо приготовить раствор с массовой долей КОН 0.18. Какой объем воды надо взять?
надо приготовить раствор с массовой долей КОН 0.18. Какой объем воды надо взять?
16. Какой объем раствора серной кислоты с массовой долей 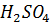 0.96 (
0.96 (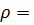 1835 г
1835 г 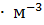 ) нужно взять для приготовления 5 л 0.5Н раствора
) нужно взять для приготовления 5 л 0.5Н раствора 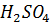 ?
?
17. Какой объем 50-процентного раствора КОН (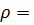 1.538 г
1.538 г 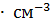 ) требуется для приготовления 3 л 6-процентного раствора
) требуется для приготовления 3 л 6-процентного раствора 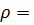 1.048 г
1.048 г 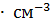 )?
)?
18. Какой объем 0.1Н 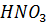 можно приготовить из 0.7 л раствора азотной кислоты с массовой долей 30% (
можно приготовить из 0.7 л раствора азотной кислоты с массовой долей 30% (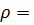 1180 г
1180 г 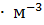 )?
)?
19. К 100 мл 96-процентной (по массе) 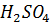 (
(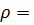 I.84 г
I.84 г 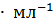 ) прибавили 400 мл воды. Получился раствор плотностью 1.220 г
) прибавили 400 мл воды. Получился раствор плотностью 1.220 г 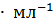 . Вычислить его эквивалентную концентрацию и массовую долю
. Вычислить его эквивалентную концентрацию и массовую долю 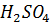 .
.
20. Сколько миллилитров концентрированной соляной кислоты (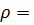 1.19 г
1.19 г 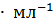 ), содержащей 38% (масс.) НСl, нужно взять для приготовления в 2 Н раствора?
), содержащей 38% (масс.) НСl, нужно взять для приготовления в 2 Н раствора?
21. Смешаны 0.8 л 1.5 Н NаOH и 0.4 л 0.6 Н NaOH. Какова эквивалентная концентрация полученною раствора?
22. Водный раствор содержит 577 г 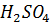 в 1 л. Плотность раствора 1335 г
в 1 л. Плотность раствора 1335 г 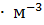 . Вычислите массовую долю
. Вычислите массовую долю 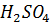 в растворе, а также эквивалентную концентрацию раствора.
в растворе, а также эквивалентную концентрацию раствора.
23. Определите молярную концентрацию и молярную концентрацию эквивалента 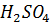 в растворе, в котором массовая дола
в растворе, в котором массовая дола 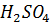 0.98, а
0.98, а 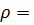 1.84 г
1.84 г 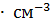 .
.
24. К 0.78 л раствора NaOH с массовой долей 0.20 и 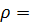 1.225 г
1.225 г 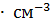 прибавили 0.14 л раствора с массовой долей NаОН 0.10 и
прибавили 0.14 л раствора с массовой долей NаОН 0.10 и 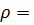 1.115 г
1.115 г 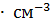 . Определите массовую долю NaOH в полученном растворе.
. Определите массовую долю NaOH в полученном растворе.
25. Какой объем раствора серной кислоты с массовой долей 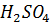 0.3 (
0.3 (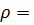 1219 г
1219 г 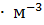 ) можно приготовить из 12 кг раствора серной кислоты с массовой долей
) можно приготовить из 12 кг раствора серной кислоты с массовой долей 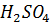 0.6.
0.6.
3. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА РАСТВОРОВ НЕЭЛЕКТРОЛИТОВ
 2015-01-13
2015-01-13 1701
1701
