3) пирамидалыќ
4) квадрат
5) октаэдрлiк
69. Келесi заттардыњ ќайсысына иондыќ кристалдыќ тор т‰з‰ тен:
1) цезий иодидi;
2) графит;
3) нафталин;
4) алмаз;
5) иод.
70. Келесi заттардыњ ќайсысына атомдыќ кристалдыќ тор т‰зу тєн:
1) аммоний нитраты;
2) алмаз;
3) иод;
4) натрий хлоридi;
5) натрий.
71. Химиялыќ элементтер ќай ќатарда электртерiстiлiгiнiњ µсу баѓытында орналаќан:
1) Si, P, Se, Br, Cl, O;
2) Si, P, Br, Se, Cl, O;
3) P, Si, Br, Se, Cl, O;
4) Br, P, Cl, Si, Se;
5) Si, P, Se, Cl, O, Br
72. Бериллий гидридi молекуласында бериллий атомыныњ валенттiк орбитальдары ќай тип бойынша гибридтелген:
Sp
2) sp2
3) sp3
4) d2sp3
5) d2sp2
73. Бериллий гидридi молекуласыныњ структурасы ќандай:
1) квадрат
2) жазыќ
3) тетраэдрлiк
4) октаэдрлiк
5) шар тєрiздi.
74. ВF3 молекуласында бор атомыныњ валенттiк орбитальдары ќай тип бойынша гибридтелген:
1) sp
2) sp2
3) sp3
4) d2sp3
5) d2sp
75. Келесi молекулалардыњ ќайсысы неѓ±рлым берiк:
1) Н2
2) О2
3) F2
4) Cl2
5) N2
76. Ќай молекуланыњ диполi неѓ±рлым жоѓары:
1) H2O
HF
3) HCl
4) HBr
5) H2S
77. Атомдыќ орбитальдары sp2-гибридизация к‰йiнде болѓанда молекуланыњ кењiстiктегi конфигурациясы ќандай болады:
1) сызыќтыќ
2) тетраэдрлiк
3) жазыќ квадрат
4) жазыќ тригональды
5) октаэдрлiк
78. Атомдыќ орбитальдардыњ ќандай гибридизациясы кезiнде молекула октаэдрлiк ќ±рылысты болады:
1) sp
2) dsp2
3) d2sp3
4) sp3
5) sp2
79. Ќазiргi кездегi атом ќ±рылысы теориясы ќайсысыныњ т‰сiнiктерiне негiзделген:
А) классикалыќ механика;
В) кванттыќ механика;
С) Бор теориясы;
Д) электродинамика;
Е) химиялыќ кинетика
80. Элемент атомдарыныњ кµрсетiлген сипаттамаларыныњ ќайсысы периодты т‰рде µзгередi:
1) атом ядросыныњ заряды
2) салыстырмалы атомдыќ масса
3) атомдаѓы энергетикалыќ дењгейлер саны
4) сыртќы энергетикалыќ дењгейдегi электрондар саны
5) электрондардыњ жалпы саны
81. Бiр период iшiнде элементтiњ реттiк нµмiрiнiњ µсуi єдетте ќай ќ±былыспен ќабат ж‰редi:
1) атом радиусыныњ тµмендеуi жєне атомныњ элекртерiстiлiгiнiњ артуы
2) атом радиусыныњ артуы жєне атомныњ элекртерiстiлiгiнiњ тµмендеуi
3) атом радиусыныњ жєне электртерiстiлiгiнiњ тµмендеуi
4) атом радиусыныњ жєне электртерiстiлiгiнiњ артуы
5) электртерiстiлiктiњ тµмендеуi
82. Ќай элемент атомы бiр электронды оњайыраќ бередi:
1) натрий, реттiк номерi 11;
2) магний, реттiк номерi 12;
3) алюминий, реттiк номерi 13;
4) кремний, реттiк номерi 14;
5) к‰кiрт, реттiк номерi 16.
83. Периодтыќ ж‰йенiњ IA тобы элементтерi атомдарында бiрдей болады:
1) сыртќы энергетикалыќ дењгейдегi электрондар саны
2) нейтрондар саны
3) барлыќ электрондар саны
4) электрондыќ ќабаттар саны
5) протондар саны
84. Элементтердiњ ќайсысы мемлекет ќ±рметiне аталѓан:
1) Sn;
2) Si;
3) Ra;
4) Ru;
6) CI.
85. Ќай ќатарда тек ауыспалы элементтер орналасќан:
1) реттiк номерi 11, 14, 22, 42;
2) реттiк номерi 13, 33, 54, 83;
3) реттiк номерi 24, 39, 74, 80;
4) реттiк номерi 19, 32, 51, 101;
5) реттiк номерi 19, 20, 21, 22.
86. VA тобыныњ ќай атомыныњ радиусы ењ ‰лкен:
1) азот;
2) фосфор;
3) мышьяк;
4) висмут;
5) сурьма.
87. Элементтердiњ ќай ќатары атом радиусыныњ µсуi баѓытында орналасќан:
1) О, S, Se, Te;
2) С, N, O, F;
3) Na, Mg, AI, Si;
4) J, Br, CI, F;
5) Sc, Te, V, Cr.
88. Mg – Ca – Sr – Ba ќатарында элементтердiiњ металдыќ сипаты:
1) азаяды
Артады
3) µзгермейдi
4) азаяды, содан кейiн артады
5) артады, содан кейiн тµмендейдi
89. Реттiк номерi артќан сайын IA тобы элементтерi гидроксидтерiнiњ негiздiк ќасиеттерi:
1) тµмендейдi
Артады
3) µзгермейдi
4) тµмендейдi, содан кейiн артады
5) артады, содан кейiн тµмендейдi
90. Ќай элементтер т‰зетiн жай заттардыњ физикалыќ жєне химиялыќ ќасиеттерi бойынша ±ќсастыѓы ‰лкен:
1) Li, S;
2) Be, CI;
3) F, CI;
4) Li, F;
5) Na, Sc.
91. Ќай элементтердiњ табиѓатта болуын Д.И. Менделеев болжап айтќан:
1) Cu, Sb, Bi;
2) AI, B, Si;
3) Sc, Ga, Ge;
4) Na, P, S.
5) Zn, Cd, Hg.
92. Периодтыќ ж‰йенiњ ‰лкен периодтарыныњ кiшi периодтардан айырмашылыѓы неде:
1) сiлтiлiк металдардыњ болуы;
2) инерттi газдардыњ болмауы;
3) d – жєне f – элементтердiњ болуы;
4) металл емес элементтердiњ болуы;
5) металдыќ ќасиет кµрсететiн элементтердiњ болуы.
93. Электрондыќ формуласы бойынша элементтiњ ќай периодта орналасатынын ќалай аныќтауѓа болады:
1) сыртќы энергетикалыќ дењгейдiњ бас квант саныныњ мєнi бойынша;
2) валенттiк электрондардыњ саны бойынша;
3) сыртќы энергетикалыќ дењгейдегi электрондар саны бойынша;
4) сыртќы энергетикалыќ дењгейдегi дењгейшелер саны бойынша;
5) соњѓы валенттiк электрон орналасќан дењгейше тањбасы бойынша.
94. Ќай элементтiњ иондану потенциалы неѓ±рлым аз:
Bi
2) Sb
3) As
4) P
5) N
95. ‡шiншi период элементi ќ±рамы Э2О3 жоѓары оксидiн т‰зедi. Осы элемент атомыныњ электрондыќ формуласы:
1) 1s22s22p1
2) 1s22s22p63s1
3) 1s22s22p63s23p1
4) 1s22s22p63s23p6
5) 1s22s22p3
96. Ќай химиялыќ элементтiњ гидроксидi неѓ±рлым айќын байќалатын негiздiк ќасиет кµрсетедi:
1) кальций;
2) магний;
3) алюминий;
4) калий;
5) бериллий
97. Атомныњ электрондыќ ќабаттарында электрондардыњ таралуы мынадай: 2.8.6. Д.И. Менделеевтiњ периодтыќ ж‰йесiнде б±л элемент ќай жерде орналасќан:
1) 6 период, 6 топ;
2) 3 период, 6 топ;
3) 2 период, 6 топ;
4) 3 период, 2 топ;
5) 2 период, 8 топ.
98. Элемент атомыныњ соњѓы электроныныњ кванттыќ сандары: n = 5, l = 1, m = -1, ms = - 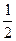 . Периодтыќ ж‰йеде б±л элемент ќай жерде орналасќан:
. Периодтыќ ж‰йеде б±л элемент ќай жерде орналасќан:
1) 5 период, 1 топ;
2) 5 период, 4 топтыњ негiзгi топшасы;
3) 4 период, 6 топ;
4) 5 период, 6 топтыњ негiзгi топшасы;
5) 5 период, 6 топтыњ ќосымша топшасы.
99. Химиялыќ элементтiњ жоѓары оксидiнiњ формуласы ЭО2 . Б±л элемент периодтыќ ж‰йенiњ ќай тобыныњ негiзгi топшасына жатады:
1) 1 топ
2) 2 топ
3) 3 топ
Топ
5) 6 топ
“Химиялыќ процестердiњ ж‰ру зањдылыќтары жєне энергетикасы”.
100. Егер жылдамдыќтыњ температуралыќ коэффициентi 2-ге тењ болса, онда температураны 300-ќа арттырѓанда реакция жылдамдыѓы неше есе кµбейедi:
1) 60;
2) 30;
3) 15;
4) 8;
5) 4.
101. Егер жылдамдыќтыњ температуралыќ коэффициентi 3-ке тењ болса, онда реакция жылдамдыѓы 27 есе азаю ‰шiн температураны неше градусќа тµмендету керек:
1) 27;
2) 30;
3) 3;
4) 81;
5) 9.
102. Y затыныњ концентрациясын 3 есе кµбейткенде X+2Y=Z реакциясыныњ жылдамдыѓы неше есе артады:
1) 2;
2) 3;
3) 6;
4) 9;
5) 12.
103. Ќысымда 2 есе арттырѓанда 2NO+O2 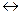 2NO2 ж‰йесiндегi тура реакцияныњ жылдамдыѓы керi реакцияныњ жылдамдыѓымен салыстырѓанда неше есе артыќ болады:
2NO2 ж‰йесiндегi тура реакцияныњ жылдамдыѓы керi реакцияныњ жылдамдыѓымен салыстырѓанда неше есе артыќ болады:
1) 2;
2) 4;
3) 3/2;
4) 0,5;
5) 2/3.
104. 2Cr+3Cl2 = 2CrCl3 ж‰йесi ‰шiн жылдамдыќтыњ д±рыс µрнегiн кµрсет:
1) v= k[Cr]2[Cl2]3
2) v= k[3Cl2]
3) v= k[2Cr][3Cl2]
4) v= k[Cl2]3
5) v= k [CrCl3]2
105. Ќай жаѓдайда реакция жылдамдыѓы єрекеттесушi заттардыњ екеуiнiњ де концентрациясына тєуелдi болады:
1) С + О2 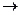 СО2
СО2
2) СО+О2 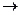 СО2
СО2
3) СО2 +С  СО
СО
4) Na +Cl2  2NaCl
2NaCl
5) S+O2  SO2
SO2
106. Егер NO концентрациясын 3 есе арттырса, 2NO+O2=2NO2 реакциясыныњ жылдамдыѓы ќалай µзгередi:
1) 27 есе артады
2) 27 есе азаяды
 2015-01-21
2015-01-21 488
488








