2) 4
3) 13
4) 20
5) 26
2. Элементтердiњ келесi массалыќ ‰лестерiне (%) сєйкес келетiн азот оксидiн кµрсету: азот - 36,84; оттегi – 63,16.
1) N2O
2) NO
3) N2O3
4) N2O5
5) NO2
3. 4 кг оттегiн алу ‰шiн судыњ ќандай массасын (кг) ыдырату ќажет:
1) 2,25;
2) 4,0;
3) 4,5;
4) 9;
5) 2
4. Бiрдей жаѓдайда массалары бiрдей етiп алынѓан газдардыњ ќайсысыныњ кµлемi ењ жоѓары болады:
1) SO2;
2) H2S;
3) O2;
4) CO2;
5) H2.
5. К‰кiрт (VI) оксидiндегi к‰кiрт эквивалентiнiњ мольдiк массасы (г/моль):
1) 2,6;
2) 5,3;
3) 10,6;
4) 13,3;
5) 20,0
6. Металдыњ 2 грамы оттегiнiњ 0,8 грамымен ќосылысады. Металл эквивалентiнiњ мольдiк массасы ќанша:
1. 40 г/моль
2. 10 г/моль
3. 16 г/моль
4. 1,6 г/моль
Г/моль
7. Егер газ ауадан 2,2 есе ауыр болса, онда оныњ салыстырмалы молекулалыќ массасы ќанша:
1) 26,1;
2) 58,0;
3) 63,8;
4) 64,0;
5) 32,0
8.Менделеев – Клапейрон тењдеуi ќайсы:
А) 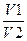 =
= 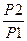
B) P = CRT
C) PV = 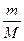 RT
RT
Д) 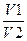 =
= 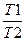
E) 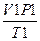 =
= 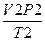
9.Басќа кез келген газ бойынша салыстырмалы тыѓыздыќ ќай ‰ш газ ‰шiн бiрдей болады:
А) CH4, SO2, Cl2
B) C2H4, CH4, F2
C) CO, Cl2, H2
Д ) CO, C2H4, N2
E) N2, CH4, H2
10.Тек ќышќылдыќ оксидтерден т±ратын ќатарды кµрсету:
1) Na2O; CaO; CO2
2) SO3; CuO; CrO3
3) Mn2O7; CuO; CrO3
4) SO3; CO2; P2O5
5) Na2O; H2O; CO2
11. Ќай ќатарда тек ќышќылдыќ оксидтер бар:
1) CO2; SiO2; MnO; CrO3
2) V2O5; CrO3; TeO3; Mn2O7
3) CuO; SO2; NiO; MnO
4) CaO; P2O3; Mn2O7; Cr2O3
5) Na2O; H2O; CuO; Mn2O7
12. К‰кiрт ќышќылын нейтралдау ‰шiн ќай зат ќолданыла алмайды:
1) натрий гидрокарбонаты;
2) магний оксидi;
3) гидроксомагний хлоридi;
4) натрий гидросульфаты;
5) натрий оксидi.
13. К‰кiрт ќышќылын нейтралдау ‰шiн ќай затты пайдалануѓа болады:
1) HNO3
2) Mg(OH)2
3) CH3OH
4) NaHSO4
5) NaCl
14. Шыны т‰тiк арќылы ерiтiндiлерге кµмiрќышќыл газы жiберiледi. Ќай заттыњ ерiтiндiсiнде µзгерiс болады:
1) КОН;
2) NaOH;
3) Ca(OH)2;
4) HCI;
5) HNO3.
15. Ќай металл гидроксидiн сєйкес оксидтi суда ерiту арќылы алуѓа болады:
1) Zn(OH)2;
2) Fe(OH)3;
3) KOH;
4) Pb(OH)2;
5) Cu(OH)2.
16. Ќай реакция жаѓдайында т±з т‰зiледi:
1) N2O5+SO3;
2) CO2+C;
3) CaO+K2O;
4) H2SO4+NH3;
5) SO2+S.
17. Ќай ќышќыл ќышќылдыќ т±здар т‰зе алады:
1) H3PO4;
2) CH3COOH;
3) HCrO2;
4) H3PO2;
5) HNO3.
18. Гидроксидтердiњ ќайсысы негiздiк т±здар т‰зе алады:
1) KOH;
2) Ba(OH)2;
3) NH4OH;
4) NaOH;
5) LiOH
19. 112 кг сµндiрiлмеген iзбес алу ‰шiн iзбестастыњ ќандай массасы (кг) ќажет:
1) 200;
2) 50;
3) 100;
4) 30;
5) 20.
20. Оксидтердiњ ќайсысы сумен єрекеттеседi:
1) NO;
2) CаO;
3) SiO2;
4) N2O;
5) CO.
21. Гидроксидтердiњ ќайсысы суда еридi:
1) Cu(OH)2;
2) Mg(OH)2;
3) Ba(OH)2;
4) Be(OH)2;
5) Fe(OH)2.
22. Калий фосфатын алу ‰шiн калий гидрофосфатына келесi заттардыњ ќайсысымен єсер ету керек:
1) KOH;
2) H2SO4;
3) KCI;
4) HCI;
5) HNO3.
23. Оксидтердiњ ќайсысы ќышќылдыќ оксид:
1)N2O;
2) NO;
3) Mn2O7;
4) CO;
5) ZnO.
24. Заттардыњ ќай ж±бы судаѓы ерiтiндiде бiр -бiрiмен єрекеттесе алады:
1) MgO жєне KOH;
2)Cu(OH)2 жєне ZnO;
3) AI2O3 жєне HCI;
4)Rb2O жєне NaOH;
5) CaO жєне K2O.
25. Ќай топта тек ќышќылдыќ т±здар бар:
1) KCI, CuOHCI, NaHSO4;
2) KAI(SO4)2, Na[AI(OH)4], Ca(HCO3)2;
3) CuS, NaHSO3, Cu(HS)2;
4) NaHCO3, Na2HPO4, NaH2PO4;
5) AIOHCI2, NaHCO3, NaCN.
26.. Ќай ќышќыл ќышќылдыќ т±з т‰збейдi:
1) H3PO4;
2) H3AsO4;
3) H3PO3;
4) HPO3;
5) H3AsO3.
27. Ќай жаѓдайда т±здыњ аталуы д±рыс емес:
1) Темiр (II) сульфаты
2) калий сульфаты
темiр (II) гидрохлоридi
4) мыс (I) хлоридi
5) аммоний сульфаты
28. Катиондарды ќышќылдыќ – негіздік анализ ж‰йесі бойынша неше топќа бµледі:
1. 3;
2. 4;
3. 5;
4. 7;
5. 6.
29. Массасы 10,8 г ‰швалеттi металды ауада ќыздырѓанда массасы 20,4 г металл оксидi т‰зiледi. Б±л ќандай металл:
1) хром Cr;
2) алюминий AI;
3) железо Fe;
4) скандий Sc;
5) натрий Na.
“Заттар ќ±рылысы жєне Д.И. Менделеевтiњ периодтыќ зањы”
30. Ќорѓасынныњ неѓ±рлым кµп тараѓан изотопы 207 Pb ядросында неше нейтрон бар:
1) 82;
2) 125;
3) 207;
4) 289;
5) 164.
31. Атомныњ ‰шiншi энергетикалыќ дењгейiнде n=3 неше электрон бола алады:
1) 2;
2) 8;
3) 18;
4) 32;
5) 50.
32. Атомныњ тµртiншi энергетикалыќ дењгейiнде n=4 неше дењгейше бар:
1) 1;
2) 2;
3) 3;
4) 4;
5) 5.
33. Вольфрам атомында электрондар неше энергетикалыќ дењгейге орналасады:
1) 5;
2) 6;
3) 7;
4) 8;
5) 9.
34. Осмий атомы ядросында неше протон бар:
1) 38;
2) 152;
3) 76;
4) 114;
5) 266.
35. Криптон атомы 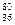 Kr ядросында ќанша протон жєне нейтрон бар:
Kr ядросында ќанша протон жєне нейтрон бар:
1) 80p жєне36n;
2) 36p жєне44е;
3) 36p жєне 80n;
4) 36p жєне44n;
5) 44p жєне44n;
36. Хром ионында 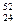 Cr3+ неше электрон бар:
Cr3+ неше электрон бар:
1) 21;
2) 24;
3) 27;
4) 52;
5) 28.
37. Ќ±рамында 18 электроны жєне 16 протоны бар ионныњ ядро заряды нешеге тењ:
1) +18;
2) –18;
3) +2;
4) –2;
5) +16.
38. 3s-орбитальда орналаса алатын электрондардыњ ењ жоѓары саны ќанша:
1) 1;
2) 2;
3) 6;
4) 8;
5) 12.
39. Ќай элемент атомыныњ электрондыќ конфигурациясы 1s22s22p63s23p64s1 болады:
1) K;
2) Ca;
3) Ba;
4) Na;
5) Cs.
40. Орбитальдар тањбаларыныњ ќайсысы д±рыс емес:
1) 2s,4f;
2) 2p,3d;
3) 1p,2d;
4) 1s,2p;
5) 3p,3d.
41. Бµлшектердiњ ќайсысыныњ электрондыќ конфигурациясы аргон атомы конфигурациясындай болады:
1) Ca2+;
2) K0;
3) Cl0;
4) Na+;
5) Na0.
42. Электронтартќыштыќ деп ненi атайды:.
1) ќозбаѓан атомнан электронды ‰зуге ќажеттi энергия;
2) берiлген элемент атомыныњ электрон тыѓыздыѓын µзiне ќарай тарту ќабiлетi;
3) электронныњ жоѓарыраќ энергетикалыќ дењгейлерге ауысуы;
4) электронныњ атомѓа немесе ионѓа ќосылуы кезiнде бµлiнетiн энергия;
5) химиялыќ байланыстыњ энергиясы.
43. Ядролыќ реакцияныњ 
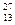 Al +
Al + 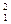 H
H 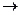
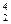 He + … нєтижесiнде ќай изотоп т‰зiледi:
He + … нєтижесiнде ќай изотоп т‰зiледi:
1) 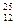 Mg;
Mg;
2) 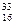 S;
S;
3) 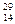 Si;
Si;
4) 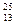 Al;
Al;
5) 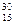 P.
P.
44. Сутек атомындаѓы электронныњ ќай ауысуы энергиясы минимал фотонныњ сiњiрiлуiн ќажет етедi:
1) 1s 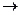 2p;
2p;
2) 1s  4d;
4d;
3) 2s 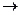 4s;
4s;
4) 2p 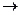 3s;
3s;
5) 2p 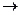 3p;
3p;
45. Ќай тењдеу электронныњ корпускулалыќ- толќындыќ табиѓатын сипаттайды:
1) 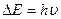 ;
;
2) 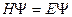 ;
;
3) 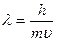 ;
;
4) 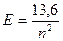 ;
;
5) E=mc2.
46. Барлыќ квант сандарыныњ (n, 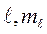 ,
, 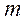 s) ќандай мєндерi калий атомыныњ валенттiк электроны ‰шiн м‰мкiн:
s) ќандай мєндерi калий атомыныњ валенттiк электроны ‰шiн м‰мкiн:
1) 4,1,-1,- 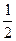 ;
;
2) 4,1,+1,+ 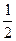 ;
;
3) 4,0,0,+ 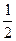 ;
;
4) 5,0,+1,+ 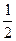 ;
;
5) 4,1,0,+ 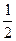 .
.
47. Негiзгi к‰йде валенттiк электрондарыныњ конфигурациясы... 4d25s2
болатын атомныњ ядро заряды ќандай:
1) 22;
2) 24;
3) 40;
4) 72;
5) 52
48. Бас квант саны n ненi аныќтайды:
А) электрон б±лттарыныњ формасын;
В ) электронныњ энергиясын;
С) электрон б±лтыныњ кењiстiктегi баѓытын;
Д) электронныњ µз осi бойынша айналу ќозѓалысын;
Е) электрон б±лтыныњ гибридтенуiн
49. Орбиталь квант саны l ненi аныќтайды:
А) электрон б±лттарыныњ формасын;
В) электронныњ энергиясын;
С) электрон б±лтыныњ кењiстiктегi баѓытын;
Д) электронныњ µз осi бойынша айналу ќозѓалысын;
Е) электрон б±лтыныњ гибридтенуiн
50. Магнит квант саны m ненi аныќтайды:
А) электрон б±лттарыныњ формасын;
В) электронныњ энергиясын;
С) электрон б±лтыныњ кењiстiктегi баѓытын;
Д) электронныњ µз осi бойынша айналу ќозѓалысын;
Е) электрон б±лтыныњ гибридтенуiн
51. Спин квант саны ms ненi аныќтайды:
А) электрон б±лттарыныњ формасын;
В) электронныњ энергиясын;
С) электрон б±лтыныњ кењiстiктегi баѓытын;
Д) электронныњ µз осi бойынша айналу ќозѓалысын;
Е) электрон б±лтыныњ гибридтенуiн
52. Радиоактивтi элементтiњ 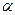 - ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
- ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
А) электрон;
В) позитрон;
С) гелий атомы ядросына бiрiккен екi протон мен екi нейтрон;
Д) екi протон;
Е) екi нейтрон
53. Радиоактивтi элементтiњ 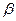 - - ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
- - ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
А) электрон;
В) позитрон;
С) гелий атомы ядросына бiрiккен екi протон мен екi нейтрон;
Д) екi протон;
Е) екi нейтрон
54. Радиоактивтi элементтiњ 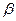 + - ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
+ - ыдырауы кезiнде оныњ атомы ядросынан ќай бµлшек ±шып шыѓады:
А) электрон;
В) позитрон;
С) гелий атомы ядросына бiрiккен екi протон мен екi нейтрон;
Д) екi протон;
Е) екi нейтрон
55. Атомдыќ орбитальдардыњ ќайсысында (n + l) ќосындысыныњ мєнi ењ тµмен болады:
А) 3d
В) 4s
С) 4p
Д) 5s
Е) 4f
56. Атомдыќ орбитальдардыњ ќайсысында (n + l) ќосындысыныњ мєнi ењ жоѓары болады:
А) 3d
В) 4s
С) 4p
Д) 5s
Е) 4f
57. Сыртќы 2р- дењгейшесiнде ‰ш электрон єр орбитальѓа бiр – бiрден орналасќанда азот атомы неѓ±рлым т±раќты болады. Б±л ќайсысыныњ мазм±нына сєйкес келедi:
А) Ењ кiшi энергия принципi;
В) Паули принципi;
С) Гунд ережесi;
Д) Клечковскийдiњ 1-шi ережесi;
Е) Клечковскийдiњ 2-шi ережесi.
58. Скандий атомыныњ 21 – шi электроны 4 р- дењгейшеге емес, 3d – дењгейшеге орналасады. Б±л ќайсысыныњ мазм±нына сєйкес келедi:
А) Ењ кiшi энергия принципi;
В) Паули принципi;
С) Гунд ережесi;
Д) Клечковскийдiњ 1-шi ережесi;
Е) Клечковскийдiњ 2-шi ережесi.
59. Калий атомыныњ 19-шы электроны 3d – дењгейшеге емес, 4s – дењгейшеге орналасады. Б±л ќайсысыныњ мазм±нына сєйкес келедi:
А) Ењ кiшi энергия принципi;
В) Паули принципi;
С) Гунд ережесi;
Д) Клечковскийдiњ 1-шi ережесi;
Е) Клечковскийдiњ 2-шi ережесi.
60. Сутек атомыныњ жалѓыз электроны негiзгi к‰йiнде 1-шi энергетикалыќ дењгейге орналасады. Б±л ќайсысыныњ мазм±нына сєйнес келедi:
А) Ењ кiшi энергия принципi;
В) Паули принципi;
С) Гунд ережесi;
Д) Клечковскийдiњ 1-шi ережесi;
Е) Клечковскийдiњ 2-шi ережесi.
61. Элемент атомдарыныњ 2-шi энергетикалыќ дењгейiнде ењ кµп дегенде 8 электрон орналаса алады. Б±л ќайсысыныњ мазм±нына сєйкес келедi:
А) Ењ кiшi энергия принципi;
В) Паули принципi;
С) Гунд ережесi;
Д) Клечковскийдiњ 1-шi ережесi;
Е) Клечковскийдiњ 2-шi ережесi.
62. Коваленттi байланыстыњ т‰зiлу механизмдерiнiњ бiрi:
1) радикалдыќ
Алмасу
3) молекулалыќ
4) иондыќ
5) тiзбектiк.
63. Полюстi коваленттi байланысы бар полюссiз молекула ќайсы:
1) N2
2) H2O
3) NH3
4) CCl4
5) CaO
64. Ќай заттыњ молекуласы полюстi емес:
1)НСI
2) CF4
3) NH3
4)H2S
5)HBr
65. Молекулардыњ LiF – BeF2-BF3- CF4-NF3-OF2-F2 ќатарында:
1) байланыстыњ сипаты µзгермейдi
2) байланыстыњ иондыќ сипаты артады
3) байланыстыњ коваленттi сипаты тµмендейдi
4) байланыстыњ коваленттi сипаты артады
5) жауаптыњ д±рыс варианты жоќ
66. Ќай ќосылыста атомдар арасында коваленттi байланыс донорлы-акцепторлы механизм
бойынша т‰зiледi:
1) KCl;
2) CCl4;
3) NH4C1;
4) NH3;
5) H2O.
67. Азот молекуласында байланыстыњ ќай т‰рi т‰зiледi:
1) тек 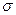 - байланыстар
- байланыстар
2) тек 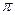 - байланыстар
- байланыстар
3) 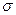 -жєне
-жєне 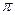 - байланыстар
- байланыстар
4) бiр байланыс
5) ќос байланыс
68. Метан молекуласыныњ структурасы:
1) жазыќ
 2015-01-21
2015-01-21 751
751







