Из формулировки второго начала термодинамики по Кельвину следует, что вечный двигатель второго рода — периодически действующий двигатель, совершающий работу за счет охлаждения одного источника теплоты,— невозможен. Для иллюстрации этого положения рассмотрим работу теплового двигателя (исторически второе начало термодинамики и возникло из анализа работы тепловых двигателей).
Принцип действия теплового двигателя приведен на рис. 85. От термостата (термодинамическая система, которая может обмениваться теплотой с телами без изменения температуры) с более высокой температурой 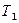 , называемого нагревателем, за цикл отнимается количество теплоты
, называемого нагревателем, за цикл отнимается количество теплоты 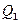 , а термостату с более низкой температурой
, а термостату с более низкой температурой 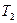 называемому холодильником, за цикл передается количество теплоты
называемому холодильником, за цикл передается количество теплоты 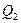 , при этом совершается работа
, при этом совершается работа 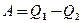 .
.
Чтобы термический коэффициент полезного действия теплового двигателя (56.2) был 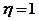 , должно быть выполнено условие
, должно быть выполнено условие 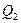 = 0, т. е. тепловой двигатель должен иметь один источник теплоты, а это невозможно. Так, французский физик и инженер Н. Л. С. Карно (1796—1832) показал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами, иначе это противоречило бы второму началу термодинамики.
= 0, т. е. тепловой двигатель должен иметь один источник теплоты, а это невозможно. Так, французский физик и инженер Н. Л. С. Карно (1796—1832) показал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами, иначе это противоречило бы второму началу термодинамики.
Двигатель второго рода, будь он возможен, был бы практически вечным. Охлаждение, например, воды океанов на 1° дало бы огромную энергию. Масса воды в мировом океане составляет примерно 1018 т, при охлаждении которой на 1° выделилось бы примерно 1024 Дж теплоты, что эквивалентно полному сжиганию 1014 т угля. Железнодорожный состав, нагруженный этим количеством угля, растянулся бы на расстояние 1010 км, что приблизительно совпадает с размерами Солнечной системы!
Рис. 85Рис. 86
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине, принцип действия которой представлен на рис. 86. Системой за цикл от термостата с более низкой температурой 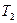 отнимается количество теплоты
отнимается количество теплоты 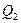 и отдается термостату с более высокой температурой
и отдается термостату с более высокой температурой 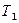 количество теплоты
количество теплоты 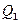 . Для кругового процесса, согласно (56.1), Q = A, но, по условию, Q =
. Для кругового процесса, согласно (56.1), Q = A, но, по условию, Q = 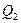 —
— 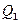 < 0, поэтому А <0 и
< 0, поэтому А <0 и 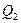 —
— 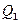 = —А, или
= —А, или 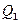 =
= 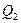 + А, т. е. количество теплоты
+ А, т. е. количество теплоты 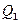 , отданное системой источнику теплоты при более высокой температуре
, отданное системой источнику теплоты при более высокой температуре 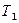 , больше количества теплоты
, больше количества теплоты 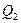 , полученного от источника теплоты при более низкой температуре
, полученного от источника теплоты при более низкой температуре 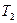 , на величину работы, совершенной над системой. Следовательно, без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать ее более нагретому. Это утверждение есть не что иное, как второе начало термодинамики в формулировке Клаузиуса.
, на величину работы, совершенной над системой. Следовательно, без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать ее более нагретому. Это утверждение есть не что иное, как второе начало термодинамики в формулировке Клаузиуса.
Однако второе начало термодинамики не следует представлять так, что оно совсем запрещает переход теплоты от менее нагретого тела к более нагретому. Ведь именно такой переход осуществляется в холодильной машине. Но при этом надо, помнить, что внешние силы совершают работу над системой, т. е. этот переход не является единственным результатом процесса.
Основываясь на втором начале термодинамики, Карно вывел теорему, носящую теперь его имя: из всех периодически действующих тепловых машин, имеющих одинаковые 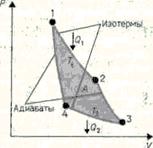
Рис. 87
температуры нагревателей (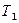 ) холодильников (
) холодильников (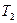 ), наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей (
), наибольшим к. п. д. обладают обратимые машины; при этом к. п. д. обратимых машин, работающих при одинаковых температурах нагревателей (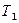 ) и холодильников (
) и холодильников (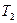 ), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами).
), равны друг другу и не зависят от природы рабочего тела (тела, совершающего круговой процесс и обменивающегося энергией с другими телами).
Карно теоретически проанализировал обратимый наиболее экономичный цикл, состоящий из двух изотерм и двух адиабат, называемый циклом Карно. Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Цикл Карно изображен на рис. 87, где изотермические расширение и сжатие заданы соответственно кривыми 1—2 и 3 — 4,а адиабатические расширение и сжатие — кривыми 2—3 и 4—1. При изотермическом процессе U = const, поэтому, согласно (54.4), количество теплоты 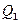 , полученное газом от нагревателя, равно работе расширения
, полученное газом от нагревателя, равно работе расширения 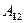 , совершаемой газом при переходе из состояния 1 в состояние 2:
, совершаемой газом при переходе из состояния 1 в состояние 2:

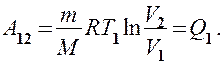 (59.1)
(59.1)
При адиабатическом расширении 2—3теплообмен с окружающей средой отсутствует и работа расширения 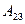 совершается за счет изменения внутренней энергии (см. (55.1) и (55.8)):
совершается за счет изменения внутренней энергии (см. (55.1) и (55.8)):
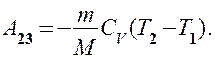
Количество теплоты 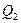 , отданное газом холодильнику при изотермическом сжатии, равно работе сжатия
, отданное газом холодильнику при изотермическом сжатии, равно работе сжатия 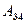 :
:
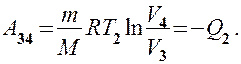 (59.2)
(59.2)
Работа адиабатического сжатия
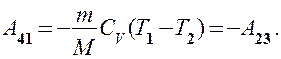
Работа, совершаемая в результате кругового процесса,
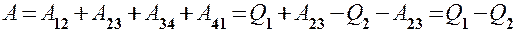
и, как можно показать, определяется площадью, выполненной в цвете на рис. 87.
Термический к.п.д. цикла Карно, согласно (56.2),
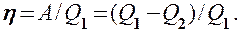
Применив уравнение (55.5) для адиабат 2—3 и 4—1, получим
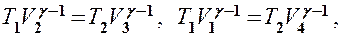
откуда
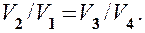 (59.3)
(59.3)
Подставляя (59.1) и (59.2) в формулу (56.2) и учитывая (59.3), получим
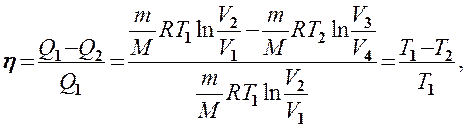 (59.4)
(59.4)
т. е. для цикла Карно к. п. д. действительно определяется только температурами нагревателя и холодильника. Для его повышения необходимо увеличивать разность температур нагревателя и холодильника. Например, при 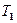 = 400 K и
= 400 K и 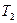 = 300 К
= 300 К 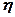 =0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то
=0,25. Если же температуру нагревателя повысить на 100 К, а температуру холодильника понизить на 50 К, то 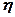 = 0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
= 0,5. К. п. д. всякого реального теплового двигателя из-за трения и неизбежных тепловых потерь гораздо меньше вычисленного для цикла Карно.
Обратный цикл Карно лежит в основе действия тепловых насосов. В отличие от холодильных машин тепловые насосы должны как можно больше тепловой энергии отдавать горячему телу, например системе отопления. Часть этой энергии отбирается от окружающей среды с более низкой температурой, а часть — получается за счет механической работы, производимой, например, компрессором.
Теорема Карно послужила основанием для установления термодинамической шкалы температур. Сравнив левую и правую части формулы (59.4), получим
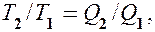 (59.5)
(59.5)
т. е. для сравнения температур 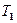 и
и 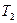 двух тел необходимо осуществить обратимый цикл Карно, в котором одно тело используется в качестве нагревателя, друroe — холодильника. Из равенства (59.5) видно, что отношение температур тел равно отношению отданного в этом цикле количества теплоты к полученному. Согласно теореме Карно, химический состав рабочего тела не влияет на результаты сравнения температур, поэтому такая термодинамическая шкала не связана со свойствами какого-то определенного термометрического тела. Отметим, что практически таким образом сравнивать температуры трудно, так как реальные термодинамические процессы, как уже указывалось, являются необратимыми.
двух тел необходимо осуществить обратимый цикл Карно, в котором одно тело используется в качестве нагревателя, друroe — холодильника. Из равенства (59.5) видно, что отношение температур тел равно отношению отданного в этом цикле количества теплоты к полученному. Согласно теореме Карно, химический состав рабочего тела не влияет на результаты сравнения температур, поэтому такая термодинамическая шкала не связана со свойствами какого-то определенного термометрического тела. Отметим, что практически таким образом сравнивать температуры трудно, так как реальные термодинамические процессы, как уже указывалось, являются необратимыми.
Контрольные вопросы
- В чем суть закона Больцмана о равнораспределении энергии по степеням свободы молекул? Почему колебательная степень свободы обладает вдвое большей энергией, чем поступательная и вращательная?
- Что такое внутренняя энергия идеального газа? Какими параметрами она определяется? В результате каких процессов может изменяться внутренняя энергия системы?
- Что такое теплоемкость газа? Какая из теплоемкостей — СV или Ср — больше и почему? Как объяснить температурную зависимость молярной теплоемкости водорода?
- Чему равна работа изобарного расширения моля идеального газа при нагревании на 1 К?
- Нагревается или охлаждается идеальный газ, если он расширяется при постоянном давлении?
- Температура газа в цилиндре постоянна. Запишите на основе первого начала термодинамики соотношение между сообщенным количеством теплоты и совершенной работой.
- Газ переходит из одного и того же начального состояния 1 в одно и то же конечное состояние 2 в результате следующих процессов: а) изотермического; б) изобарного; в) изохорного. Рассмотрев эти процессы графически, показать: 1) когда работа расширения максимальна; 2) когда газу сообщается максимальное количество теплоты.
- Газ переходит из одного и того же начального состояния 1 в одно и то же конечное состояние 2 в результате следующих процессов: а) изобарного процесса; б) последовательных изохорного и изотермического процессов. Рассмотрите эти переходы графически. Одинаковы или различны в обоих случаях: 1) изменение внутренней энергии? 2) затраченное количество теплоты?
- Почему адиабата более крута, чем изотерма?
- Как изменится температура газа при его адиабатическом сжатии?
- Показатель политропы п> 1. Нагревается или охлаждается идеальный газ при сжатии?
- Чем отличаются обратимые и необратимые процессы? Почему все реальные процессы необратимы?
- В каком направлении может изменяться энтропия замкнутой системы? незамкнутой системы?
- Дайте понятие энтропии (определение, размерность и математическое выражение энтропии для различных процессов).
- Изобразите в системе координат Т, S изотермический и адиабатический процессы. Возможен ли процесс, при котором теплота, взятая от нагревателя, полностью преобразуется в работу?
- Представив цикл Карно на диаграмме р, V графически, укажите, какой площадью определяется: 1) работа, совершенная над газом; 2) работа, совершенная самим расширяющимся газом.
- Представьте графически цикл Карно в переменных Т, S.
Задачи
9.1. Азот массой 1 кг находится при температуре 280 К. Определить: 1) внутреннюю энергию молекул азота; 2) среднюю кинетическую энергию вращательного движения молекул азота. Газ считать идеальным. [1) 208 кДж; 2) 83,1 кДж ]
9.2. Определить удельные теплоемкости 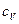 и
и 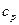 некоторого двухатомного газа, если плотность этого газа при нормальных условиях 1,43 кг/м3. [
некоторого двухатомного газа, если плотность этого газа при нормальных условиях 1,43 кг/м3. [ 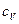 = 650 Дж/(кг×К),
= 650 Дж/(кг×К), 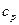 = 910 Дж/(кг×К)]
= 910 Дж/(кг×К)]
9.3. Водород массой 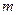 = 20 г был нагрет на
= 20 г был нагрет на 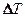 = 100 К при постоянном давлении. Определить: 1) количество теплоты Q, переданное газу; 2) приращение
= 100 К при постоянном давлении. Определить: 1) количество теплоты Q, переданное газу; 2) приращение 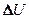 внутренней энергии газа; 3) работу A расширения. [1) 29,3 кДж; 2) 20,9 кДж; 3) 8,4 кДж ]
внутренней энергии газа; 3) работу A расширения. [1) 29,3 кДж; 2) 20,9 кДж; 3) 8,4 кДж ]
9.4. Кислород объемом 2 л находится под давлением 1 МПа. Определить, какое количество теплоты необходимо сообщить газу, чтобы увеличить его давление вдвое в результате изохорного процесса. [5 кДж ]
9.5. Некоторый газ массой 2 кг находится при температуре 300 К и под давлением 0,5 МПа. В результате изотермического сжатия давление газа увеличилось в три раза. Работа, затраченная на сжатие, A = – 1,37 кДж. Определить: 1) какой это газ; 2) первоначальный удельный объем газа. [1) гелий; 2) 1,25 м3/кг]
9.6. Двухатомный идеальный газ занимает объем V 1 = 1 л и находится под давлением 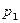 = 0,1 МПа. После адиабатического сжатия газ характеризуется объемом V 2 и давлением
= 0,1 МПа. После адиабатического сжатия газ характеризуется объемом V 2 и давлением 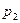 . В результате последующего изохорного процесса газ охлаждается до первоначальной температуры, а его давление
. В результате последующего изохорного процесса газ охлаждается до первоначальной температуры, а его давление 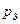 = 0,2 МПа. Определить: 1) объем V 2; 2) давление
= 0,2 МПа. Определить: 1) объем V 2; 2) давление 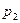 . Представить эти процессы графически. [ 1) 0,5 л; 2) 0,26 МПа ]
. Представить эти процессы графически. [ 1) 0,5 л; 2) 0,26 МПа ]
9.7. Идеальный газ количеством вещества n = 2 моль сначала изобарно нагрели так, что его объем увеличился в п =2 раза, а затем изохорно охладили так, что давление газа уменьшилось в п = 2 раза. Определить приращение энтропии в ходе указанных процессов. [11,5Дж/К]
9.8. Тепловая машина, совершая обратимый цикл Карно, за один цикл совершает работу 1 кДж. Температура нагревателя 400 К, а холодильника 300 К. Определить: I) к.п.д. машины; 2) количество теплоты, получаемое машиной от нагревателя за цикл; 3) количество теплоты, отданное холодильнику за цикл. [1) 25%; 2) 4 кДж; 3) 3 кДж ]
9.9. Идеальный газ совершает цикл Карно, термический к.п.д. которого равен 0,3. Определить работу изотермического сжатия газа, если работа изотермического расширения составляет 300 Дж. [–210 Дж]
 2015-01-21
2015-01-21 7638
7638