Идеальным газом называется воображаемый газ, молекулы которого представляют собой материальные точки, не имеющие собственного объема и не взаимодействующие между собой. Зависимость между основными термодинамическими параметрами такого газа определяется уравнением состояния идеального газа – уравнением Клапейрона-Менделеева:
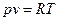 , (1)
, (1)
где 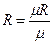
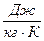 - газовая постоянная;
- газовая постоянная;
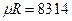
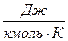 - универсальная газовая постоянная.
- универсальная газовая постоянная.
Реальные газы состоят из молекул, имеющих конечный собственный объем, между которыми действуют силы межмолекулярного взаимодействия (силы притяжения и отталкивания). Эти газы описываются уравнением (1) только при малых плотностях, когда среднее расстояние между центрами молекул сравнительно велико, и эти силы не проявляются. В более плотных реальных газах со значительно меньшим расстоянием между молекулами необходимо учитывать и эти силы, и собственный объем молекул. Поведение реальных газов качественно отражает уравнение Ван-дер-Ваальса:
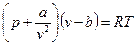 , (2)
, (2)
где 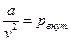 - называют внутренним давлением (для жидкостей оно велико), учитывает силы взаимодействия между молекулами;
- называют внутренним давлением (для жидкостей оно велико), учитывает силы взаимодействия между молекулами;
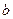 - учитывает собственный объем молекул - это наименьший объем, до которого можно сжать газ.
- учитывает собственный объем молекул - это наименьший объем, до которого можно сжать газ.
Для количественных расчетов уравнение (2) часто малопригодно, т.к. при высоких плотностях, а следовательно, при высоких давлениях параметры, рассчитанные по этому уравнению, расходятся с действительными (экспериментальными) значениями.
Уравнение Ван-дер-Ваальса можно представить в приведенных параметрах состояния. Если переменные p, v и T отнести к их значениям в критической точке 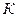 (далее в опыте Эндрюса эта точка будет рассмотрена подробнее), то можно получить приведенные значения объема
(далее в опыте Эндрюса эта точка будет рассмотрена подробнее), то можно получить приведенные значения объема 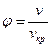 , давления
, давления 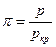 и температуры
и температуры 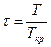 и записать так называемое приведенное уравнение состояния:
и записать так называемое приведенное уравнение состояния:
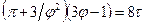 . (3)
. (3)
Состояния веществ, находящихся при одинаковых 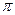 ,
, 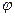 и
и 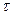 , называются соответственными состояниями.
, называются соответственными состояниями.
Уравнения типа (2) и (3) получаются в случае, если ограничиться рассмотрением только парных взаимодействий между молекулами, т.е. в группах по две молекулы. Поэтому эти уравнения применимы в области не очень высоких давлений.
С повышением давления необходимо учитывать образование устойчивых молекулярных образований из трех, четырех и более молекул, распад которых возможен только при подводе энергии извне, т.е. при нагревании. Такой газ можно рассматривать как «смесь» нескольких газов, частицами которых являются одиночные, двойные, тройные и т.д. группы молекул.
Уравнение состояния реальных газов формально можно записать в виде:
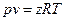 , (4)
, (4)
где z - коэффициент сжимаемости (для идеальных газов z = 1) - можно представить в виде вириального уравнения, учитывающего и взаимодействия более высокого порядка:
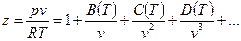 . (5)
. (5)
Правую часть этого уравнения можно рассматривать как разложение в ряд коэффициента z по степеням плотности 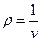 . Зависящие от температуры функции
. Зависящие от температуры функции 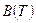 ,
, 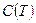 ,
, 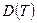 … выступают здесь как вириальные (от латинского vires - силы) коэффициенты, учитывающие соответственно парные, тройные, четверные и т.д. взаимодействия. Область справедливости вириального разложения ограничивается сходимостью рядов. Ряды расходятся при плотностях, соответствующих жидкому состоянию. Уравнение (5) оказывается справедливым для газов умеренной плотности.
… выступают здесь как вириальные (от латинского vires - силы) коэффициенты, учитывающие соответственно парные, тройные, четверные и т.д. взаимодействия. Область справедливости вириального разложения ограничивается сходимостью рядов. Ряды расходятся при плотностях, соответствующих жидкому состоянию. Уравнение (5) оказывается справедливым для газов умеренной плотности.
Второй вириальный коэффициент может быть определен по значениям потенциальной энергии взаимодействия - силам притяжения и отталкивания - двух молекул 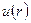 в зависимости от расстояния между ними:
в зависимости от расстояния между ними:
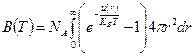 , (6)
, (6)
где NA - число Авогадро, NA = 6,022×1026 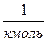 ;
;
КБ - постоянная Больцмана, КБ = 1,38×10-23 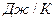 ;
;
кстати 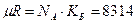
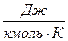 - универсальная газовая постоянная.
- универсальная газовая постоянная.
Определение последующих вириальных коэффициентов для газов достаточно большой плотности облегчается при наличии экспериментально полученных данных по теплофизическим свойствам этих газов (теплоемкость, вязкость, теплопроводность и т.п.).
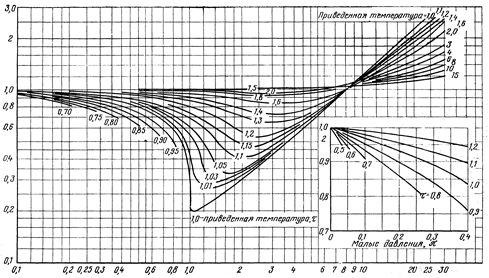
Коэффициент неидеальности z может быть найден также по зависимости 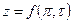 из
из 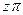 - диаграммы (рис.1).
- диаграммы (рис.1).
|
|
Рассчитанное значение 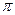 откладывается на соответствующей оси этой диаграммы и из этой точки проводится прямая, перпендикулярная оси
откладывается на соответствующей оси этой диаграммы и из этой точки проводится прямая, перпендикулярная оси 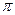 до пересечения с кривой, соответствующей рассчитанному значению t. Точка пересечения позволяет определить искомую величину коэффициента неидеальности на оси z.
до пересечения с кривой, соответствующей рассчитанному значению t. Точка пересечения позволяет определить искомую величину коэффициента неидеальности на оси z.
Точность расчетов в этом случае окажется такой же, как и по уравнению Ван-дер-Ваальса (2) или приведенному уравнению (3)
 2015-02-24
2015-02-24 465
465








