Метод основан на реакции между нитратами и фенолдисуль-фокислотой с образованием нитропроизводных фенола, которые со щелочами образуют окрашенные в желтый цвет соединения.
Обнаружение NО2-. На крахмальную бумагу последовательно наносят каплю 2 н. уксусной кислоты, каплю анализируемой воды и каплю 0,1н. иодида калия. В зависимости от количества присутствующего нитрита появляется синее пятно или кольцо йодкрахмального соединения.
В кислых растворах нитриты взаимодействуют с иодидами по уравнению:
2NO2- + 2J- + 4H+ 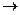 J2 + 2H2O + 2NO
J2 + 2H2O + 2NO
Чувствительность реакции: m = 0,005 мкг NO2-.
В присутствии нитритов чувствительная цветная реакция на нитраты с дифениламином не пригодна, поскольку нитриты дают подобную же реакцию. Поэтому, предварительно нужно удалить нитриты. Один из методов разрушения нитритов основан на реакции с аминосульфоновой кислотой (сульфаминовой кислотой):
NO2- + NН 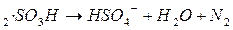
Обнаружение NО3-. В пробирку наливают 5 мл исследуемой воды, прибавляют 4 – 5 капель раствора дифениламина, встряхивают. При наличии нитратов раствор окрашивается в синий цвет. По интенсивности окрашивания приближенно судят об их содержании и необходимости количественного анализа.
Чувствительность реакции: m = 0,5 мкг NО3-.
 2015-02-24
2015-02-24 675
675








