Реагентные методы используют для очистки водных систем от солей жесткости (известково-содовый способ), ионов тяжелых металлов (нейтрализация, комплексообразование). При этом растворенные примеси из растворенного состояния переходят в нерастворимые соединения, которые в дальнейшем выделяют при осаждении.
В основе известково-содового способа очистки от солей жесткости лежат следующие обменные реакции:
CaSO4+Na2CO3→Na2SO4+CaCO3,
MgSO4+2NaOH→Mg(OH)2+Na2SO4,
CaSO4+2NaOH→Ca(OH)2+Na2SO4,
Ca(OH)2+Na2CO3→CaCO3+2NaOH,
CaCO3,e↔Cae2++CO3,e2-.
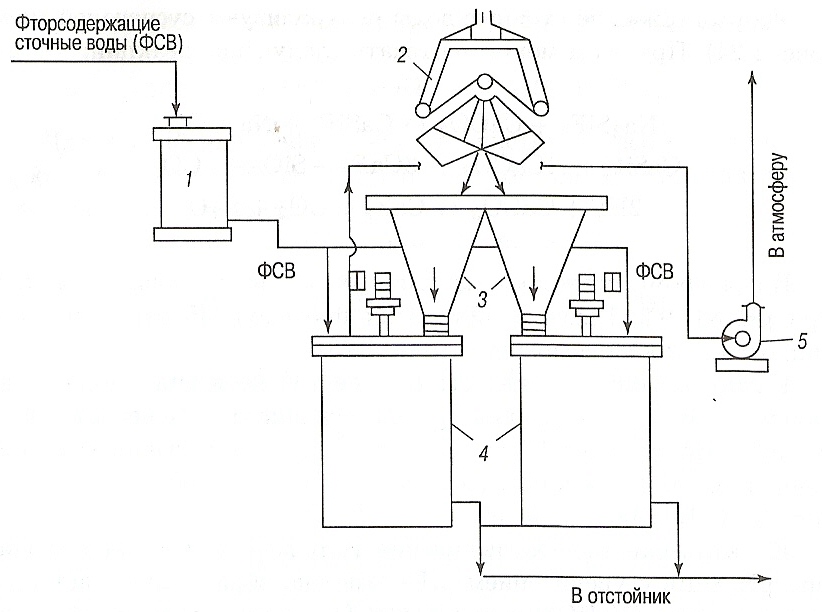
Рис. 1. Схема установки для нейтрализации сточных вод суспензией мела: 1-сборник-усреднитель; 2-грейферный кран; 3-бункеры; 4-реакторы; 5-вентилятор.
Растворенное соединение выпадает в осадок при условии
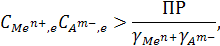
где 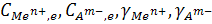 - соответсвенно концентрации ионов в момент равновесия и коэфиициенты их активности. Индекс e указывает на состояние равновесия.
- соответсвенно концентрации ионов в момент равновесия и коэфиициенты их активности. Индекс e указывает на состояние равновесия.
Для насыщенного раствора малорастворимой соли в воде
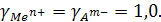
Пределы растворимости (ПР) некоторых соединений приедены ниже.
| Соединения | CaCO3 | ZnS | PbCO3 | CdS | CaF2 | FeS |
| ПР | 3,1*10-9 | 1,6*10-24 | 1,5*10-13 | 1*10-29 | 4*10-11 | 4*10-19 |
Фторсодержащие сточные воды нейтрализуют суспензией мела (рис. 1). При этом могут протекать следующие реакции:
Na2SiF6+CaCO3↔CaSiF6+Na2CO3,
CaSiF6+2CaCO3↔3CaF2+SiO2+2CO2,
2HF+CaCO3↔CaF2+CO2+H2O.
Ионы хрома осаждают из сточных вод известковым молотком при рН 8,0-9,5. Выше и ниже этих пределов рН растворимость гидроксида хрома возрастает (рис. 2).
Катионы свинца можно осадить не только в виде гидроксида свинца, но и в виде гидроксокарбоната свинца (в воде нерастворим) и карбоната свинца (ПР=1,5*10-13). Для
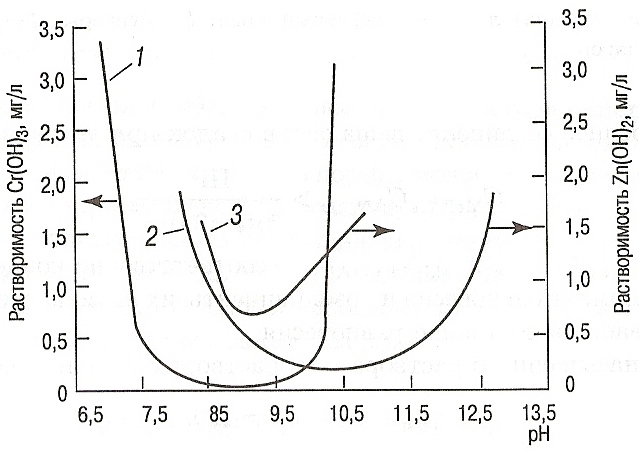 Рис. 2. Растворимость в воде гидроксидов хрома и цинка (в пересчете на Cr3+ и Zn2+) в зависимости от рН:
Рис. 2. Растворимость в воде гидроксидов хрома и цинка (в пересчете на Cr3+ и Zn2+) в зависимости от рН:
1-Cr(OH)3, подщелачивание известковым молоком;
2-Zn(OH)2, подщелачивание известковым молоком;
3- Zn(OH)2, подщелачивание карбонатом натрия.
осаждения катионов свинца можно применять известняк (CaCO3), необожженный доломит (CaCO3* MgCO3) и др.
Практически полное выпадение гидроксида меди происходит при рН 8-10, с увеличением рН возможно образование растворимых купритов (NaHCuO2 или NaCuCO2). Катионы меди (II) целесообразно осаждать в виде гидроксокарбоната, нерастворимого в воде:
2Cu2++CO32-+2OHàCu2(OH)2CO3↓.
Для повышение эффективности очистки целесообразно в сточную воду вводить более растворимые соединения кальция, например гидроксид кальция.
Нейтрализация кислоты протекает по реакции
H2SiF6+3Ca(OH)2↔3CaF2+SiO2+4H2O.
При этом возможны и другие обменные реакции:
Na2SiF6+Ca(OH)2↔CaSiF6+2NaOH,
Na2SiF6+3Ca(OH)2↔3CaF2+SiO2+2H2O+2NaOH,
CaSiF6+2Ca(OH)2↔3CaF2+SiO2+2H2O,
2HF+Ca(OH)2↔CaF2+2H2O.
В результате этих реакций соединения фтора переходят в труднорастворимый фторид кальция, растворимость которого в воде при 20оС составляет около 16 мг/л.
Приведенные обменные реакции протекают практически мгновенно. При этом образуются растворы электролитов, пересыщенные соединениями кальция. Начинается кристаллизация – образование и рост кристаллов солей кальция.
При выделении тяжелых металлов необходимо соблюдать оптимальные условия их осаждения. Например, для осаждения цинка карбонатом натрия требуется значительное количество реагента. Поэтому рекомендуется двухступенчатая очистка воды от цинка, предусматривающая предварительную нейтрализацию серной кислоты карбонатом натрия с последующим осаждением цинка гидроксидом натрия.
При глубокой очистке катионы цинка осаждаются в виде труднорастворимого сульфида ZnS. При осаждении цинка сульфитом натрия оптимальный рН составляет 2,5-3,5. ПРZnS=1,6*10-24.
Очистка от ионов кадмия производится подщелачиванием сточных вод до рН 10,5. Образующиеся мелкодисперсные частицы Cd(OH)2 можно выделить в осадок коагуляцией сульфатами алюминия или железа. Катионы кадмия можно осаждать в виде CdS, добавляя сульфид натрия. ПРCdS=1*10-29; pHопт≈4.
Для осаждения ртути и кадмия предложены такие реагенты, как ксантогенты, образующие нерастворимые комплексы с ионами ртути и кадмия.
Фосфор в сточных водах присутствует в виде растворимых соединений – орто- и метафосфатов, а также в виде комплексных неорганических фосфатов, например полифосфатов.
Для осаждения фосфатов сточные воды обрабатывают известковым молоком (рН 10-11) или сульфатом алюминия в щелочной среде.
Реагентный метод очистки должен обеспечить достаточно полное выделение растворимых примесей в виде нерастворимых осадков, быстрый отстой образовавшегося осадка и максимальное уплотнение шлама.
Очистка сточных вод с использованием химических реагентов имеет ряд особенностей. При прочих равных условиях эффективность процесса зависит от турбулентности в ядре потока, с увеличением которой возрастает вероятность дробления образующихся агрегатов.
Процесс очистки зависит как от режимных параметров (температура, порядок подачи и концентрация реагентов, концентрация малорастворимых солей в очищаемой воде), так и от присутствия затравочных кристаллов.
На примере карбоната кальция рассмотрены основные стадии роста кристаллов – внешняя диффузия и поверхностная реакция (рис. 3).
Массовая скорость кристаллизации:
- стадия внешней диффузии
Wr=β(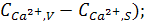 (1)
(1)
- стадия поверхностной реакции
Wr=kг(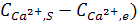 nρK, (2)
nρK, (2)
Kг=2,9*10-7exp 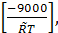 (3)
(3)
где β – коэффициент массоотдачи, м/с; kг – аррениусовская константа скорости роста кристалла, м/с; n – порядок реакции; ρК-плотность кристаллизующегося вещества, кг/м3.
В процессе кристаллизации карбоната кальция стадия внешне диффузии практически не оказывает сопротивления процессу (отсутствует диффузионное торможение) при высоких пересыщениях раствора (S=2-2,5). В этом случае скорость гетероген
Wr=kг(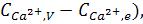
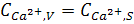 (4)
(4)
а линейная скорость роста кристалла
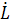 =kгSn, (5)
=kгSn, (5)
где S=(C0-Ce)/Ce – относительное пересыщение раствора.
По экспериментальным данным значение n приближается к 1,0.
М.А.Булатовым проведены исследования по интенсификации очистки раствора при производстве поваренной соли на Мозырском солеварочном комбинате. Исходные растворы получали методом подземного выщелачивания.
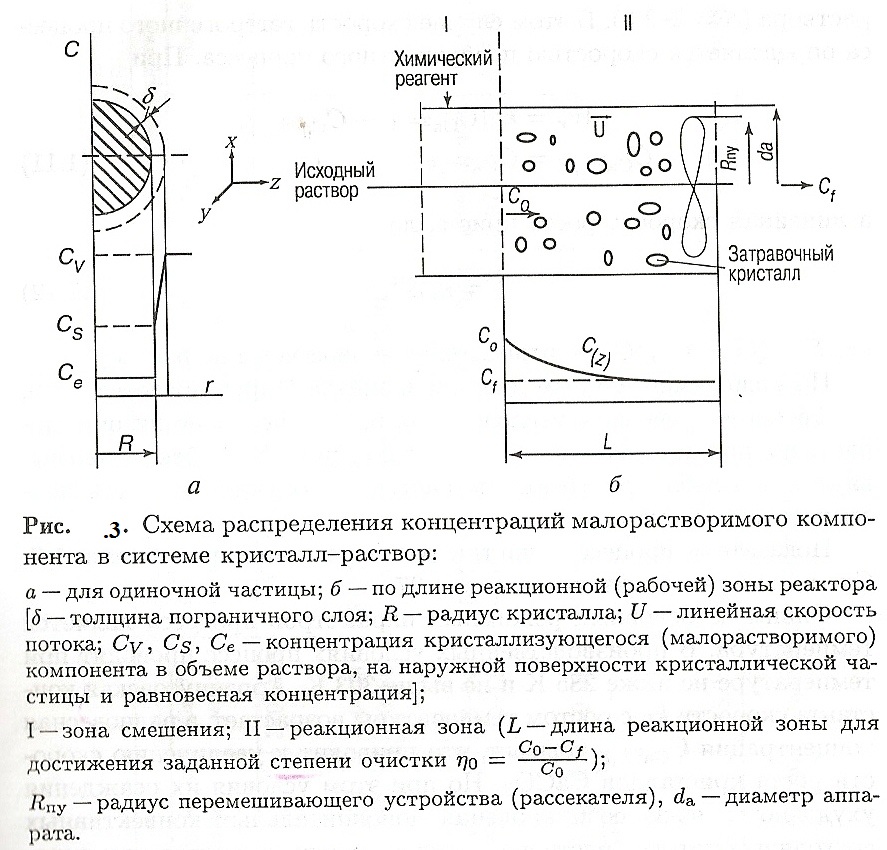
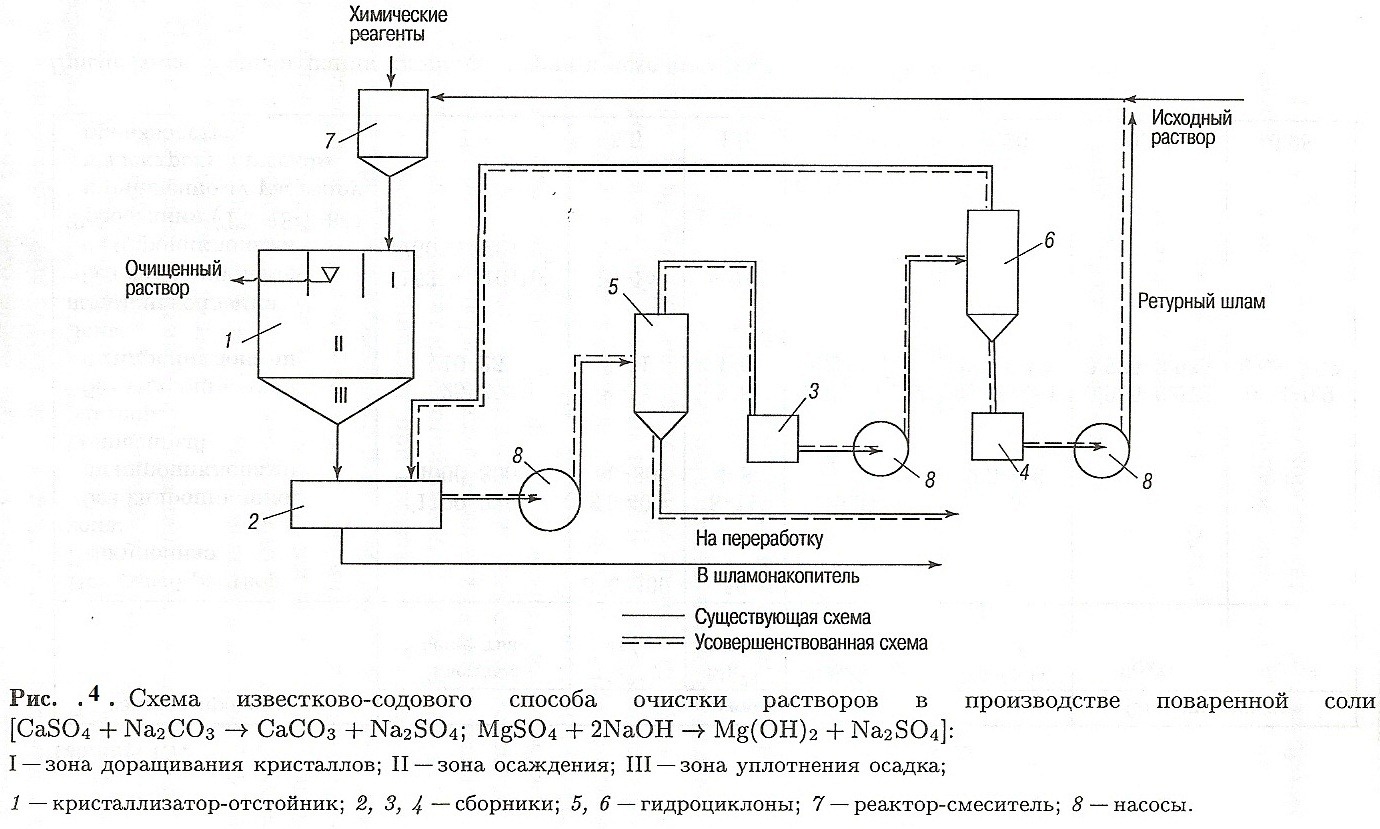
Показатели процесса очистки раствора приведены в табл. 1. Схема очистки показана на рис. 4.
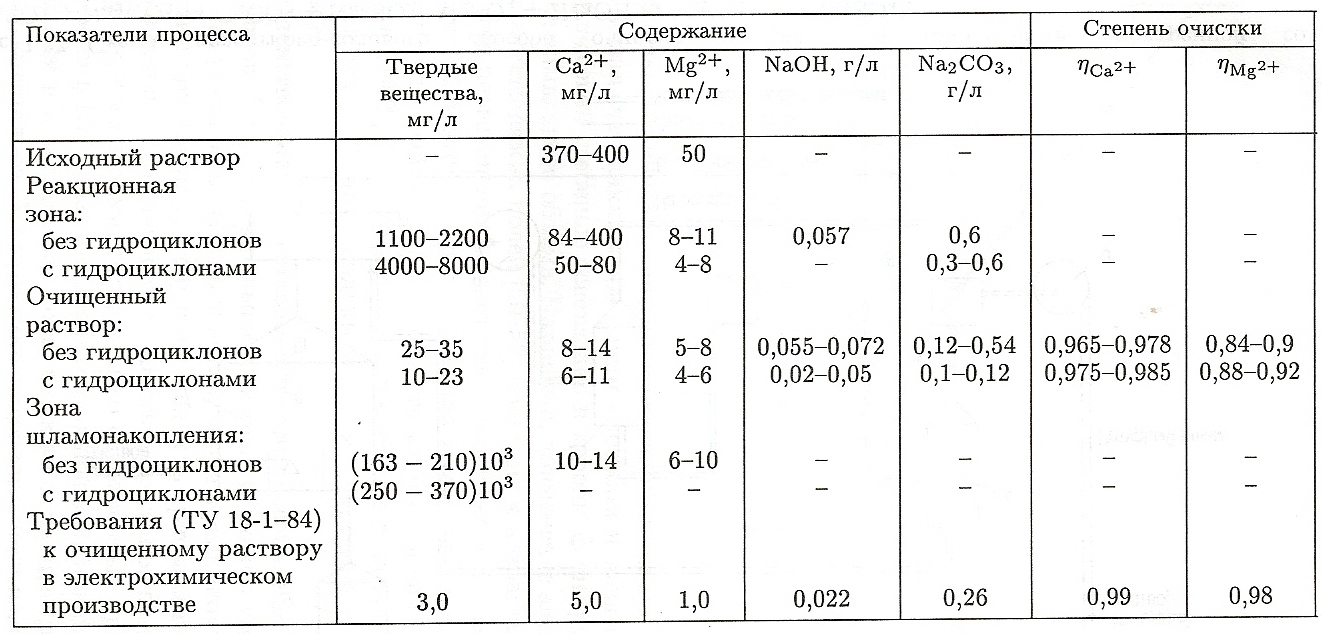
Одним из основных режимных параметров процесса является температура. В производственных условиях процесс проводят при температуре не ниже 285 К и не выше 303 К. Аррениусовская константа скорости kг с ростом температуры возрастает, а равновесная концентрация 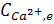 убывает, что приводит к увеличению скорости роста кристаллов CaCO3. Но при этом условия их осаждения ухудшаются из-за возникновения дополнительных конвективных восходящих потоков раствора, обусловленных градиентом температур по высоте кристаллизатора-отстойника 1. Для быстрого снятия пересыщения растворы очищают при избытке осадительных реагентов в реакторе 7. При избытке осадительных реагентов уменьшается растворимость карбоната кальция и увеличивается пересыщение раствора. Возрастает не только скорость роста кристаллов, но и скорость их образования. Это приводит к тому, что средний размер твердых частиц на выходе из реактора 7 уменьшается (рис. 5) и скорость их осаждения падает.
убывает, что приводит к увеличению скорости роста кристаллов CaCO3. Но при этом условия их осаждения ухудшаются из-за возникновения дополнительных конвективных восходящих потоков раствора, обусловленных градиентом температур по высоте кристаллизатора-отстойника 1. Для быстрого снятия пересыщения растворы очищают при избытке осадительных реагентов в реакторе 7. При избытке осадительных реагентов уменьшается растворимость карбоната кальция и увеличивается пересыщение раствора. Возрастает не только скорость роста кристаллов, но и скорость их образования. Это приводит к тому, что средний размер твердых частиц на выходе из реактора 7 уменьшается (рис. 5) и скорость их осаждения падает.
Таблица 1.
Примечание. Концентрация хлорида натрия в исходном растворе ≈ 270-285 г/л.
При последующем отстаивании в кристаллизаторе – отстойнике 1 (см. рис. 4) наблюдается значительный унос мелких нерастворенных примесей размером до ≈5 мкм с очищенным раствором и эффективность очистки уменьшается.
Для интенсификации реагентного метода очистки увеличивают скорость снятия пересыщения, либо осаждения, либо уплотнения. Анализ физико-химических методов интенсификации очистки растворов показал, что каким-либо одним способом нельзя получить раствор с высокой степенью осветления и хорошо фильтрующимся осадком
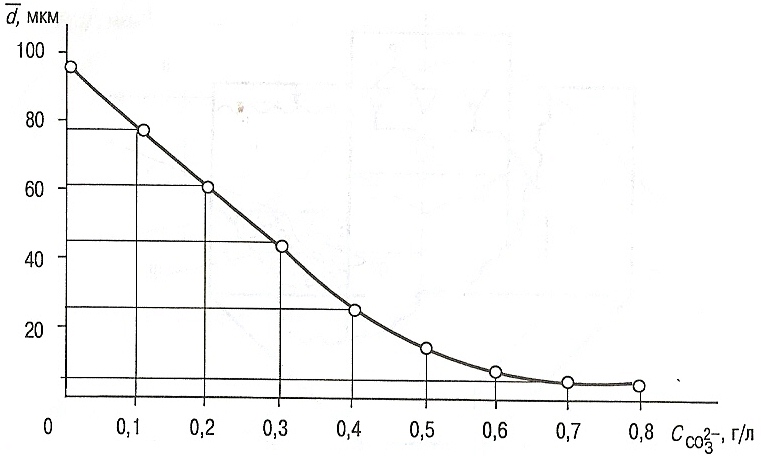
Рис. 5. Зависимость среднего размера твердых частиц от избытка соды.
минимального объёма. Например, применение электромагнитных и акустических полей приводит к возрастанию скорости снятия пересыщения за счет увеличения скорости зародышеобразования. При этом возникают мелкие кристаллы, образующие хорошо уплотняемый осадок, а скорость их осаждения невелика. Применение ПАВ приводит к увеличению скорость осаждения, но при этом период стадии индукции для ряда солей может увеличиваться.
Лекция №12. (продолжение лекции №11)
 2015-02-27
2015-02-27 1663
1663
