Задачи, относящиеся к теме «Химическая кинетика» можно разделить на следующие группы:
1. Определение скорости реакции в зависимости от температуры.
2. Определение скорости реакции в зависимости от изменения концентрации.
3. Решение задач на расчет констант равновесия, равновесных и исходных концентраций.
Задача 2
Определить во сколько раз увеличится скорость реакции, протекающей в газовой фазе при повышении температуры от 20оС до
60оС, если температурный коэффициент равен 3.
Дано:
| j = 3 to1 = 20oC to2 = 60oC | 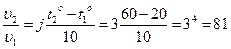 (раз) (раз) |
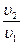 =?
=?
Ответ: скорость реакции при нагревании до 60оС увеличивается в 81 раз.
Задача 3
Взаимодействие между оксидом углерода (II) и хлором идет по уравнению СО + Cl2 ® COCl2
Концентрация оксида углерода 0,3 моль/л, а хлора 0,2 моль/л.
Как изменится скорость реакции, если увеличить концентрацию хлора до 0,6 моль/л, а концентрацию оксида углерода (II) до 1,2 моль/л?
Дано:
| [CO]1 = 0,3 моль/л [Cl2]1 = 0,2 моль/л [CO]2 = 0,6 моль/л [Cl2]2 = 1,2 моль/л | υ1 = k[CO]1 · [Cl2]1 υ2 = k[CO]2 · [Cl2]2 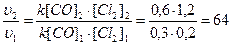 раза раза |
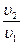 =?
=?
Ответ: При увеличении концентрации хлора до 1,2 моль/л и концентрации оксида углерода (II) до 0,6 моль/л скорость реакции увеличивается в 64 раза.
 2015-02-04
2015-02-04 1659
1659








