В 1920 г. А. Надсон (СССР) и в 1925 г. П. Анцель и П. Винтембергер (Франция) пришли к выводу, что наблюдаемые радиационные повреждения клетки – это результат двух противоположных процессов: развития повреждения и одновременно идущего процесса восстановления.
Соотношение между ними определяет степень тяжести лучевого поражения, что, в конечном итоге, отражается на общем результате лучевого поражения, включая ближайшие и отдаленные последствия.
Поражающий эффект облучения при одной и той же поглощенной дозе существенно зависит от временных условий воздействия, т.е. его продолжительности, зависящей при непрерывном облучении от мощности дозы. При этом различают облучение кратковременное или «острое», пролонгированное и хроническое. При разделении дозы на фракции тяжесть поражения зависит как от продолжительности, как самих фракций, так и интервалов между ними.
В большинстве случаев увеличение продолжительности облучения или разделение его на фракции при одной и той же суммарной дозе приводит к уменьшению повреждающего действия. Эффект зависит от развития в организме восстановительных процессов, приводящих к снижению величины поражения еще до окончания всего периода набора дозы. Объективным критерием оставшейся величины поражения к любому моменту времени после облучения является устойчивость к повторному воздействию радиации.
Эту устойчивость (радиорезистентность) можно оценить в эксперименте, определяя дозу облучения, вызывающую заданный биологический эффект, например, ЛД 50/30 - дозу, приводящую к гибели 50 % животных в течение 30 суток после облучения (Бутомо Н.В. и др., 2001).
Любые радиационные эффекты строго зависят от интенсивности облучения. Поражение максимально выражено при остром облучении и ослабляется при его пролонгировании. Это объясняется тем, что за миллионы лет в процессе эволюции животные и человек приобрели огромное количество ферментов, защищающих от большого числа вредных факторов. Эти репарационные ферменты восстанавливают клетки и от радиационных повреждений. При пролонгированном облучении условия для репарации облегчаются, благодаря чему вероятность проявления эффектов и степень их выраженности сильно снижаются (Ярмоненко С.П., 2000).
Репарация (восстановление) радиационных повреждений - это общебиологическое явление, обнаруженное при проведении опытов на всех лабораторных и сельскохозяйственных животных. Hа основании большого экспериментального материала американским ученым Г.Блэром (1952) была разработана теория «повреждения-восстановления», которая формулируется следующим образом: «Лучевое поражение развивается пропорционально интенсивности облучения, а процессы восстановления идут со скоростью, пропорциональной величине этого поражения. При этом остается необратимая часть поражения, которая пропорциональна величине общей накопленной дозы» [10].
Таким образом, радиационное воздействие на организм, кроме прямого действия на его функциональные подсистемы, индуцирует или активизирует и защитные системы (репарации, адаптации), регулирующая роль которых состоит в компенсации воздействия, минимизации прямого действия облучения, восстановлении функций и репарации повреждений. Результирующий, остаточный эффект воздействия после реализации восстановительных процессов зависит от соотношения «прямого» и «обратного» процессов, своего для каждой дозы.
Представляется важным проследить зависимость репарационных процессов от мощности и дозы облучения. Можно рассмотреть две крайние точки зрения:
1). системы восстановления включаются с одинаковой эффективностью при любой мощности и дозе облучения;
2). существуют такие мощности и (или) дозы облучения, которые организм не чувствует и поэтому не включает системы восстановления, или они начинают работать с большой задержкой во времени или с меньшей эффективностью.
В первом случае самое незначительное воздействие является своеобраз-
ным «спусковым крючком», запускающим системы восстановления. Тогда чем ниже мощность или доза облучения, тем меньше образуется повреждений и выше вероятность появления порога и даже возникновения эффекта противоположного знака.
Во втором случае должен существовать интервал доз облучения, где реализуются все полученные повреждения. По мере увеличения дозы (или времени после начала облучения) эффект растет, достигает максимума, а затем начинает снижаться вследствие включения систем репарации. В экспериментах была обнаружена зависимость «доза - эффект», хорошо согласующаяся со второй точкой зрения (Бурлакова Е.Б., Голощапов А.Н., Жижина Г.П. и др., 1999).
Ядро клетки более чувствительно к действию радиации по сравнению с цитоплазмой. Прямые доказательства этого факта были получены в опытах с прицельным облучением ядра. Оказалось, что попадание уже одной альфа-частицы в ядро оплодотворенного яйца насекомого вызывает гибель зародыша, тогда как при прохождении частиц через цитоплазму для достижения такого же эффекта необходимо 15 млн. альфа-частиц. В опытах на амебах с помощью микрохирургического метода было показано, что пересадка ядер клеток, облученных в дозе 15 крад, в необлученные клетки вызывает такой же эффект (5%-ную выживаемость). Если же облучению подвергали цитоплазму даже в дозе 25000 рад, после чего в нее трансплантировали необлученное ядро, то эффекта не наблюдалось: все 100% амеб делились и давали жизнеспособное потомство.
Внутриядерной структурой, ответственной за жизнеспособность клетки, является ДНК. Известно, что ДНК, уложенная в ядрах, представляет собой вещество наследственности, в ее цепях записана огромная по объему генетическая информация. Облучение вызывает различные повреждения ДНК и ее комплексов. К их числу относятся разрывы молекул ДНК, сшивки ДНК-ДНК, ДНК-белок, потеря оснований, изменение состава оснований. Разрывы цепей ДНК являются основной причиной гибели делящихся клеток. В клетке существует система репарации наследственного материала, которая исправляет часть разрывов ДНК, удаляет измененные участки генетического «текста»,
однако не всегда полностью «излечивает» молекулу ДНК. Поэтому раньше всего активируются репарирующие ферменты – полимеразы, лигазы (синтетазы), ликвидирующие разрывы спирали. ДНК и поврежденных азотистых оснований.
Критерием для изучения зависимости «доза – эффект» служит выживаемость клетки или организма. Зависимость выживания клеток описывается следующим уравнением:
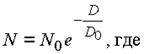
N – число выживших клеток,
N0 – число облученных клеток
D – любая доза облучения,
D0 – доза, при которой доля живых клеток уменьшается в е раз.
Таким образом, можно сделать вывод, что с увеличением дозы излучения увеличивается не только (и даже не столько) степень поражения всех облученных клеток, сколько доля пораженных, т.е. погибших клеток.
По мнению Н.В. Бутомо, Ю.Ю. Ивницкого и А.Н. Гребенюка (2001) наиболее выражены восстановительные процессы после облучения в сублетальных дозах (достаточно больших, но еще не приводящих организм к гибели). При дозах выше и ниже этого уровня темп восстановления замедляется. Считают, что при малых дозах воздействия радиации количество возникающих дефектов недостаточно для возникновения максимально возможного уровня восстановления. Облучение в высоких дозах повреждает сами механизмы восстановления. Важно отметить, что восстановление радиорезистентности может происходить на фоне прогрессирующего развития лучевого поражения, оцениваемого по клиническим проявлениям, картине крови и т.д.
В опытах на животных было установлено, что необратимая часть лучевого поражения составляет 10% общего повреждения, а интенсивность процессов репарации, определяемая по величине ЛД50 или по картине восстановления
гематологических показателей, существенно различается у животных разных
видов.
Период полувосстановления (время, в течение которого восстанавливается 50 % повреждений) для мышей составляет 3-8 суток, крыс- 6-9, собак- 14-18, ослов- 20-28, а человека - 25- 45 суток.
Таким образом, чем крупнее организм или больше продолжительность его жизни, тем длительнее период полувосстановления.
При этом следует учитывать:
1). место нахождения самого источника радиации относительно облучаемого организма (внешнее, внутреннее или комбинированное);
2). его вид (α-, β-,γ-, х - или n -излучение)
3). кратность и длительность облучения;
4). радиочувствительность организма в целом и отдельных его органов и тканей в частности.
В Соединенных Штатах нашлись дальновидные политики, которые поддержали предложенный учеными Национальной атомной лаборатории Окриджа проект широкомасштабных исследований действия радиации на млекопитающих в самых различных аспектах биологии и медицины. Он получил даже знаковое название «Грандиозная мышь», так как планировалось изучить в данном исследовании более миллиона мышей. Ко времени окончания эксперимента количество подопытных животных составило почти 7 млн. особей. Результаты этой грандиозной работы оказались настолько ошеломляющими, что длительное время не пропагандировались и были известны только узкому кругу специалистов.
Во-первых, различия в индивидуальной чувствительности разных особей к радиационному воздействию достигали 20-кратных(!) значений.
Во-вторых, если доза радиации растягивается во времени, то однократное облучение вызывает больший эффект, чем та же доза, полученная через определенные периоды - то есть на протяжении времени доза не накапливается и принцип «накопления» дозы, установленный на дрозофиле, на млекопита-
ющих не распространяется.
В-третьих, особи мужского пола более чувствительны к радиационным
последствиям облучения, чем самки.
В-четвертых, чем больше промежуток времени между временем облучения и оплодотворением, тем меньшее количество мутаций вызывает радиа-
ция у потомства.
Для млекопитающих и, в частности, человека, достаточно шести месяцев, чтобы свести до минимума генетические последствия, вызванные радиационным воздействием [54]. Расчеты показывают, что удвоение частоты самопроизвольных, спонтанных мутаций находится в диапазоне 0,5-2,5 Зв.
На дрозофиле величина удваивающей дозы была установлена на уровне
0,05 зиверта. Таким образом, как указывает Фрэнк фон Хиппель, профессор Принстонского университета (США), один из ведущих в мире специалистов в ядерной области, в отличие от дрозофилы, данные, полученные на млекопитающих в течение почти 30-летнего эксперимента «характеризуют радиацию как слабый мутаген в отношении млекопитающих» (Хиппель фон Ф. и др., 1988).
В научных журналах уже начали появляться статьи, в которых результаты экспериментов противоречили общепринятым популярным постулатам о неотвратимости генетических последствий радиации. Считалось, что закономерности радиационного мутагенеза, установленные на дрозофиле, имеют универсальный характер. Некоторые эксперименты, проведенные на млекопитающих, пошатнули эту идею.
Линдоп и Ротблад облучали самцов мышей в трех поколениях. В каждом поколении самцы получали дозу 350 рентген. Однако влияния этих облучений на продолжительность жизни потомства обнаружить не удалось. Не было найдено генетических изменений и после облучения животных большими дозами - от 500 до 720 Р [131].
 2015-02-04
2015-02-04 1568
1568








