Головной мозг. Интенсивность кровотока в сосудах мозга высока — в состоянии психического и физического покоя она составляет 55-60 мл/100 г/мин, т.е. около 15% сердечного выброса. При относительно небольшой массе (2% от веса тела) мозг потребляет до 20% всего кислорода и 17% глюкозы, которые поступают в организм человека. Интенсивность потребления кислорода мозгом составляет в среднем 3-4 мл/100 г/мин. Критическая величина интенсивности суммарного мозгового кровотока, при которой начинают проявляться признаки необратимых изменений мозгового вещества в связи с
299
недостатком кислорода, составляет около 15 мл/100 г/мин. Уже через 5- 7 с после прекращения кровообращения в мозге человек теряет сознание. При ишемии мозга, продолжающейся более 5 мин, отмечается феномен невосстановления кровотока, вследствие перекрытия микроциркуляторного русла из- за изменений эндотелия капилляров и отека глиальных клеток. В отличие от других органов мозг практически не располагает запасами кислорода.
Сосуды мозга способны путем ауторегуляторных механизмов поддерживать кровоток на относительно стабильном уровне при изменениях системного АД в пределах 60- 180 мм рт.ст. При подъеме АД выше 180 мм рт.ст. возможно резкое расширение артерий мозга, сопровождающееся нарушением функций гематоэнцефалического барьера, возникновением отека и возрастанием интенсивности мозгового кровотока. При относительном постоянстве общего мозгового кровотока локальный кровоток в различных отделах мозга не постоянен и зависит от интенсивности их функционирования. Так, при напряженной умственной работе локальный кровоток в коре головного мозга человека может возрастать в 2- 3 раза по сравнению с состоянием покоя.
В условиях герметичности и жесткости черепа общее сопротивление сосудистой системы головного мозга мало зависит от изменений давления в его артериях. Так, при повышении АД происходит расширение мозговых артерий, что ведет к повышению давления лик-вора, сжатию вен мозга и оттоку ликвора в спинальную полость. При этом сопротивление артерий падает, а вен — возрастает, так что общее сопротивление сосудистой системы мозга в целом практически не меняется.
Миогенная регуляция мозгового кровотока осуществляется за счет реакции гладких мышц артериальных сосудов мозга на изменение давления в них. Повышение АД приводит к возрастанию тонуса миоцитов и сужению артерий, снижение АД — к снижению тонуса и расширению артерий. Миогенная регуляция мозгового кровотока считается центральным звеном системы ауторегуляции кровообращения в мозге.
Гуморальная регуляция обеспечивается прямым действием на гладкие мышцы сосудов различных вазоактивных веществ: метаболитов, гормонов, биологически активных веществ.
Мощным регулятором мозгового кровотока является уровень напряжения углекислого газа в артериальной крови и связанный с этим уровень рН спинномозговой жидкости. На каждый миллиметр изменения напряжения СО2 величина мозгового кровотока изменяется примерно на 69?.
Возрастание напряжения СО2 в крови (гиперкапния) сопровождается расширением мозговых сосудов, а гипокапния — их сужением, столь значительным, что достигается порог кислородной недостаточности мозга (одышка, судороги, потеря сознания). Возрастание мозгового кровотока при гиперкапнии обеспечивает быстрое "вымывание" углекислоты и возвращение уровня напряжения СО2 и концентрации водородных ионов к исходной величине.
300
Напряжение 02 не является фактором градуальной регуляции общего мозгового кровотока. Лишь падение напряжения кислорода (гипоксия) до пороговой величины (около 50 мм рт.ст.) вызывает резкое возрастание общего кровотока в мозге. Поскольку при таких величинах напряжения кислорода имеет место прогрессирующее накопление в тканях мозга молочной кислоты (а значит снижение рН), конечной причиной усиления мозгового кровотока при гипоксии может быть расслабление сосудов мозга под действием снижения рН. Прямое вазодилататорное влияние недостатка кислорода на мозговые сосуды при этом не исключается. Усиление мозгового кровотока при гипоксии сохраняет величину потребления мозгом кислорода на прежнем уровне.
Метаболическая регуляция играет существенную роль при локальных перераспределениях крови между областями мозга, имеющими разный уровень функциональной активности в каждой конкретной ситуации. Локальное повышение функциональной активности нервных клеток приводит к повышению в межклеточной среде концентрации аденозина и ионов калия, что ведет к местному расширению сосудов и усилению в них кровотока.
Учитывая, что уровень концентрации ионов калия в межклеточной среде головного мозга может меняться в течение долей секунды от момента усиления функциональной активности нейронов, описанный механизм называют быстрым контуром регуляции. Более медленный контур регуляции мозгового кровотока связан с повышением напряжения СО2 в мозговом веществе, вследствие активного потребления кислорода работающими клетками. Это вызывает локальное снижение рН в межклеточной среде и приводит к расширению сосудов активно функционирующей области мозга.
Биологически активные вещества и гормоны могут оказывать как прямое, так и опосредованное влияние на сосуды мозга. К внутри-сосудистым вазоконстрикторам относятся: вазопрессин, ангиотензин, простагландины группы F, катехоламины. Сосудорасширяющий эффект оказывают: ацетилхолин, гистамин (средние и крупные артерии), брадикинин (мелкие артерии).
Вещества, способствующие изменению напряжения О2 и СО2 в крови, такие как тироксин, адреналин и другие, могут, через изменения рН влиять на тонус мозговых сосудов. Адреналин, кроме того, может вызывать повышение мозгового кровотока через усиление нейрональной активности в структурах центральной нервной системы.
Нейpогенная регуляция сосудов головного мозга менее эффективна, чем метаболическая. Основной зоной приложения ней-рогенных влияний являются мелкие артериальные мозговые сосуды, диаметром до 25-30 мкм. Венозная часть сосудистой системы мозга иннервирована значительно слабее, чем артериальная. Среди нервных волокон, обеспечивающих регуляцию тонуса мозговых сосудов, доказано существование адренергических, холинергических, серото-нинергических и пептилгргических волокон. Нервные влияния на стенку сосудов мозга опосредуются через а- и В-адренорецепторы
301
(норадреналин), М-холинорецепторы (ацетилхолин, вазоинтестиналь-ный пептид), D-рецепторы (серотонин).
Основной источник нервных влияний на сосуды мозга — по-стганглионарные симпатические волокна, начинающиеся в верхних шейных ганглиях. Показано, что интенсивная электрическая стимуляция симпатических нервов приводит к повышению сопротивления мозговых сосудов лишь на 6-8%. Существование парасимпатических влияний на мозговые сосуды не доказано. Получены данные о Прямой адренергической иннервации мелких мозговых сосудов и сосудов виллизиева круга от ядер голубого пятна, а также серото-нинергической и пептидергической иннервации магистральных и внутримозговых артерий от ядер шва.
Нейрогенные влияния на кровоснабжение мозга во многом зависят от выраженности ауторегуляции, исходного тонуса сосудов, напряжения СО2, О2, состава и концентрации ионов, присутствия биологически активных веществ в спинномозговой жидкости и Тканях мозга. Именно поэтому, конечный эффект нейрогенных влияний на мозговой кровоток не является однозначным.
Миокард. В состоянии покоя у человека через коронарные сосуды протекает 200-250 мл крови в минуту (60 мл/100 г/мин), это составляет 4- 5% минутного объема крови. При интенсивной мышечной работе коронарный кровоток может возрастать до 400 мл/ мин на 100 г ткани.
Кровоток в коронарных артериях претерпевает существенные колебания в связи с фазами сердечного цикла. В период систолы желудочков, расположенные в них сосуды частично пережимаются, кровоток к миокарду резко ослабевает (до 15%). Во время диастолы напряжение в стенке миокарда падает и кровоток увеличивается до 85%.
Несмотря на резкое снижение кровотока в миокарде во время систолы, коронарное кровообращение полностью удовлетворяет высокие метаболические потребности миокарда. Это достигается высокой объемной скоростью кровотока, растяжимостью сосудов сердца, фазными колебаниями кровотока в коронарных венах (во время систолы ускоряется отток крови из коронарного синуса, в диастолу он понижается), наличием густой капиллярной сети (сердечная мышца богато снабжена капиллярами — на каждое мышечное волокно приходится капилляр; малое диффузное расстояние от капилляра до кардиомиоцита облегчает доставку кислорода и питательных веществ к кардиомиоцитам), высокой экстракцией кислорода миокардом [в состоянии покоя миоглобин сердечной мышцы извлекает из артериальной крови 60-75% кислорода (в мозге — 25-30%)]. Миокард потребляет в покое кислорода до 10 мл/100 г/мин. При интенсивной мышечной работе экстракция; кислорода в миокарде возрастает примерно в 6 раз.
Миогенная регуляция. Для коронарных сосудов характерен высокий тонус, величина которого находится в обратно-пропорциональной зависимости от интенсивности обменных процессов миокарда. Миогенный механизм ауторегуляции кровотока обес-
302
печивает относительную независимость коронарного кровотока при изменении АД в пределах от 70 до 160 мм рт.ст.
Гуморальная регуляция. Важнейшее значение в гуморальной регуляции коронарного кровотока принадлежит метаболическим факторам. Наиболее мощным регулятором является напряжение кислорода в крови: расширение коронарных сосудов проявляется при снижении содержания кислорода в крови на 5%. Взаимосвязь между внешним потреблением кислорода и уровнем кровотока осуществляется через метаболические механизмы. "Аденози-новая теория" метаболической регуляции коронарного кровообращения в настоящее время является общепризнанной. Предполагают, что аденозин блокирует захват Са++ гладкими мышцами. Наблюдающееся при физической нагрузке увеличение концентрации ионов калия, водородных ионов, молочной кислоты, повышение концентрации двуокиси углерода, появление в межклеточной жидкости ва-зоактивных веществ (гистамин, кинины, простагландины группы Е, пептиды) вызывает расширение сосудов и увеличение кровотока в миокарде. Ацетилхолин через М-холинорецепторы расширяет коронарные артерии. Адреналин и норадреналин через а- адренорецеп-торы вызывают сужение, через В — расширение коронарных артерий и вен. Ангиотензин и вазопрессин только в больших дозах приводят к сужению коронарных сосудов. Инсулин расширяет коронарные артерии. Тироксин, кортизол и другие гормоны усиливают кровоснабжение миокарда через метаболические посредники.
Нервная регуляция. Нейрогенный тонус сосудов сердца невелик (около 20%). Симпатические нервы содержат сосудосуживающие волокна, их торможение вызывает коронародилатацию. Прямое действие вегетативных нервов и их медиаторов на артерии и вены миокарда в условиях целого организма трудно определить, так как они меняют работу сердца и, следовательно, его метаболизм. Нервные влияния находятся в конкурентных отношениях с метаболическими, которые представляют более мощный контур регуляции.
Легкие. Легочная артерия и ее ветви, имеющие диаметр более 1 мм, относятся к артериям эластического типа, они демпфируют (смягчают) пульсовые толчки крови, выбрасываемой в момент систолы правого желудочка. Артериолы в легких тесно связаны с окружающей альвеолярной паренхимой, это определяет непосредственную зависимость уровня кровоснабжения легких от режима вентиляции.
В отличие от большого круга кровообращения, капилляры которого имеют диаметр около 7-8 мкм, в легких имеются два типа капилляров — широкие (20-40 мкм) и узкие (6-12 мкм). Общая площадь капиллярного русла легких у человека составляет 35-40 м2. Стенка капилляров легких и стенка альвеол представляют в совокупности функциональное целое, обозначаемое как альвеоло-капиллярная мембрана.
Если функциональное значение сосудов малого круга кровообращения заключается, главным образом, в поддержании адекватного легочного газообмена, то бронхиальные сосуды обеспечивают питание тка-
303
ней самих легких. Венозная бронхиальная сеть дренирует кровь как в систему большого круга кровообращения (верхняя непарная вена, правое предсердие), так и малого — в легочные вены и левое предсердие. Только 30% крови, поступающей в бронхиальные артерии по системе большого круга кровообращения, достигает правого желудочка, основная же часть кровотока направляется через капиллярные и венозные анастомозы в легочные вены. Указанная особенность бронхиального кровотока формирует так называемый физиологический дефицит напряжения кислорода в артериальной крови большого круга. Примесь бронхиальной венозной крови к артериализированной крови легочных вен понижает на 6-10 мм рт.ст. напряжение кислорода по сравнению с его напряжением в крови легочных капилляров, что практически не сказывается на кислородном режиме в процессе обычной жизнедеятельности организма. Однако, в тех случаях, когда по каким-либо причинам имеет место усиление бронхиального кровотока (при эмболии легочных сосудов, митральном стенозе и др.), примесь бронхиальной венозной крови к потоку оксигенированной крови малого круга приводит к артериальной гипоксемии.
Главная задача легких заключается в обеспечении газообмена между организмом (кровью) и окружающей средой. Основным условием, определяющим степень оксигенации крови в легких, являются величины легочной вентиляции и кровотока, а также степень их соответствия друг другу.
Минутный объем кровообращения через легкие соответствует МОК в большом круге и составляет в условиях покоя 5-6 л/мин. Сопротивление сосудистого русла малого круга при этом приблизительно в 8- 10 раз меньше, чем в системе большого круга кровообращения. Легочные сосуды характеризуются высокой растяжимостью, поскольку их сосудистая стенка значительно тоньше, чем у соответствующих по калибру сосудов скелетной мускулатуры и спланхнической области. Это определяет роль легочных сосудов как депо крови.
Важной особенностью кровоснабжения легких является то, что сосуды малого круга кровообращения -- это система низкого давления. Среднее давление в легочной артерии у человека составляет 15-25 мм рт.ст., а давление в легочных венах — 6-8 мм рт.ст. Таким образом, градиент давления, определяющий движение крови по сосудам малого круга, составляет 9- 15 мм рт.ст., что значительно меньше градиента давления в большом круге кровообращения. Отсюда понятен физиологический смысл высокой растяжимости легочных сосудов: значительное увеличение кровотока в системе малого круга (например, при физической нагрузке) не будет сопровождаться повышением давления крови в силу указанных свойств сосудов легких. Эта физиологическая особенность стенок сосудов малого круга является одним из факторов предупреждения отека легких.
Другим следствием низкого градиента давления в малом круге является неравномерность кровоснабжения легких от их верхушки к основанию. В вертикальном положении тела кровоснабжение верхних долей несколько меньше, чем нижних. Это объясняется тем, что при движении крови от уровня сердца до верхних долей легких
304
кровоток испытывает дополнительное препятствие из- за гидростатических сил, определяемых высотой столба крови от уровня сердца до верхушки легкого. Напротив, при движении крови вниз, от уровня сердца до основания нижней доли, гидростатические силы будут" способствовать усилению кровотока. Зоны неоднородности кровоснабжения (верхняя, средняя и нижняя доли легких) получили название зон Веста (соответственно 1-я, 2-я и 3-я зоны).
Нервная регуляция. Легочные сосуды имеют двойную иннервацию: вагусную (афферентную) и симпатическую (эфферентную). Основным источником афферентной иннервации легочных сосудов являются блуждающие нервы (волокна, идущие от чувствительных клеток узловатого ганглия). Главными источниками эфферентной иннервации являются шейные и верхние грудные симпатические узлы.
Влияние нервной системы на легочные сосуды, в отличие от сосудов большого круга кровообращения, выражено намного меньше. Так, электрическая стимуляция симпатических нервов ведет к умеренному констрикторному эффекту, повышая давление в легочной артерии лишь на 10±15%, т.е. на 1-1.5 мм рт.ст.
Крупные легочные сосуды (особенно легочная артерия и область ее бифуркации) является важной рефлексогенной зоной, обеспечивающей реализацию рефлекторных реакций сосудов малого круга. Так, повышение давления в легочных сосудах приводит к рефлекторному падению системного артериального давления, замедлению ритма сердечных сокращений, увеличению кровенаполнения селезенки и вазодилатации в скелетных мышцах. Расширение периферических сосудов уменьшает приток крови в малый круг кровообращения и, тем самым, "разгружает" легочные капилляры и предохраняет легкие от отека. Описанный комплекс рефлекторных реакций с барорецепторов малого круга получил в литературе обозначение как рефлекс Швигка-Парина.
Рецепторный аппарат сосудов в малом круге представлен преимущественно «-адренорецепторами (хотя плотность их распределения значительно меньше, чем сосудов большого круга), Д-серотонино-выми, H1- гистаминовыми рецепторами и, в меньшей степени, М-холинорецепторами.
Гуморальная регуляция. В реализации гуморального контроля легочного кровообращения катехоламины и ацетилхолин играют значительно меньшую роль, чем в большом круге кровообращения. Введение в малый круг кровообращения катехоламинов вызывает менее выраженную вазоконстрикцию, чем те же дозы препаратов в сосудах других органов. Повышение концентрации аце-тилхолина в крови сопровождается умеренной дилатацией легочных сосудов. Гуморальная регуляция легочного кровотока определяется серотонином, гистамином, ашиотензином- II, простагландином- F. При повышении концентрации этих веществ в малом круге кровообращения имеет место сужение легочных сосудов и повышение давления в легочной артерии.
В регуляции кровоснабжения легких определенную роль играет изменение состава альвеолярного воздуха. Так, уменьшение содер-
305
жания кислорода во вдыхаемом, а соответственно, и в альвеолярном воздухе, приводит к сужению легочных сосудов и повышению давления в легочной артерии, тогда как сосуды большого круга кровообращения в ответ на гипоксию расширяются.
Желудочно-кишечный тракт (ЖКТ). В состоянии покоя на ЖКТ приходится до 20% сердечного выброса. Кровоток в различных отделах ЖКТ неодинаков: в желудке человека он достигает 40 мл/100 г/мин, в тонком кишечнике — 35 мл/100 г/мин, в толстом кишечнике — 20 мл/100 г/мин. При максимальной дилатации сосудов кишечника кровоток в нем увеличивается в 8- 10 раз, причем более 90% дополнительной крови поступает в слизисто-подслизистую сеть.
В первые минуты после еды происходит увеличение кровотока в сосудах ЖКТ (отчасти за счет выпрямления спиралевидных артерий), причем лишь в тех отделах, функциональная активность которых усилена. Эта фаза реакции сосудистой системы ЖКТ на прием пищи продолжается 5- 30 минут. Через 30 мин после приема пищи кровоток в брыжеечной артерии значительно возрастает (на 30- 130% по сравнению с состоянием "натощак") и сохраняется на этом уровне в течение 3-7 часов. Степень увеличения кровотока после приема пищи определяется ее химическим составом и исходным функциональным состоянием органов ЖКТ. Каждый из основных слоев стенки кишечника имеет свою, относительно самостоятельную систему кровообращения. Благодаря этому, осуществление трех основных функций кишечника (секреция, всасывание и моторика) может приводить к изменению кровоснабжения лишь той ткани, которая эту функцию выполняет.
Всасывание продуктов расщепления белков, жиров и углеводов усиливает кровоток в сосудах слизисто-подслизистого слоя по сравнению с состоянием функционального покоя. Добавление желчи к химусу значительно усиливает функциональную гиперемию кишечника.
Нервная регуляция сосудов ЖКТ осуществляется симпатическими вазоконстрикторными волокнами. Стимуляция этих волокон вызывает сужение артериальных (рис.7.22) и венозных сосудов, а также прекапиллярных сфинктеров, что обеспечивает увеличение регионарного сопротивления и уменьшение кровотока в органе. При снижении частоты импульсов в симпатических волокнах возникает обратный эффект — расширение сосудов ЖКТ.
В артериальных сосудах кишечника широко представлены а- и В-адренорецепторы. В венозных сосудах В- адренорецепторов значительно меньше. В интактном сосудистом русле ЖКТ при выделении ка-техоламинов В-адренорецептсры ограничивают констрикторный эффект, возникающий при возбуждении а-адренорецепторов. Это служит механизмом обеспечения необходимого кровоснабжения кишечника при активации симпато-адреналовой системы. Холинергические сосудорасширяющие волокна в кишечнике и в желудке не обнаружены. При длительной стимуляции симпатических вазоконстрикторных нервов в кишечнике происходит "ауторегуляторное ускользание" из-под влияния сосудосуживающих волокон нервной системы. Значение его в поддер-
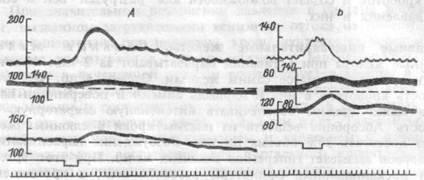
Рис.7.22. Величина и характер изменений сопротивления в сосудах селезенки и тонкой кишки при хеморефлексе с подвздошной кишки (А) и прессорном синокаротидном рефлексе (Б).
Сверху вниз: системное артериальное давление, перфузионное давление в сосудах селезенки, тощей кишки, отметка раздражения, отметка времени (5 с). Шкалы — в мм рт.ст.
жании постоянного кровотока и защите тканей ЖКТ (например, от ишемии при стрессорных воздействиях) велико.
Гуморальная регуляция. Объектом действия гуморальных агентов в сосудах ЖКТ являются, главным образом, артериолы и прекапиллярные сфинктеры. Велика роль в регуляции кровотока в ЖКТ таких метаболитов как СО2, Н+ и др. Эти вещества, как и недостаток кислорода, оказывают вазодилататорное действие. Метаболиты снижают тонус гладких мышц артериол и, тем самым, понижают сосудистое сопротивление в системе брыжеечной артерии, увеличивая кровоток в сосудах ЖКТ. Этот механизм не объясняет выполнение абсорбционной функции ворсинками, значительно удаленными от регулируемых артериол. В связи с этим считается, что в ЖКТ существует ряд специфических механизмов вазодилатации, не связанных с изменением содержания в тканях истинных метаболитов. Так, показано, что функциональная гиперемия ЖКТ после приема пищи обусловлена действием на сосуды ряда гастроингести-нальных гормонов, например, гастрина и гистамина. Противоположное действие на них оказывают вазопрессин, гастрон, простагландин Е. Большое значение отводится веществам, высвобождающимся в активно работающем органе. Так, в тонкой кишке расширение артериальных сосудов и прекапиллярных сфинктеров вызывают секретин и холецистокинин.
Миогенная регуляция. Сосуды ЖКТ отличаются высокой способностью к ауторегуляции кровотока. При локальном увеличении венозного давления в определенном регионе тонус прекапиллярных сфинктеров повышается, что уменьшает местный капилляр-
307
ный кровоток и создает возможности для "разгрузки" вен и снижения давления в них.
Главные пищеварительные железы. Слюнные железы. Слюнные железы при активации вырабатывают за 2 мин количество слюны, равное по массе самим железам. Отсюда ясно, что интенсивность кровотока в них и площадь обменной поверхности капилляров желез должны обеспечивать интенсивную секреторную способность. Абсорбция веществ из плазмы крови в слюнных железах может достигать 30% объема плазмы. Возбуждение парасимпатических нервов вызывает гиперемию слюнных желез. При этом артерио-лы и прекапиллярные сфинктеры расслабляются, а проницаемость капилляров возрастает, что создает благоприятные условия для транспорта веществ в железистые клетки. При активной работе желез, имеющиеся в них артерио-венозные шунты не функционируют и вся кровь проходит через капилляры.
Симпатические влияния на сосуды слюнных желез вызывают их сужение. Вазоконстрикторный эффект осуществляется через «-адре-норецепторы. В создании функциональной гиперемии участвуют: 1) вазодилататорные волокна, которые способствуют выработке сосудорасширяющих кининов, 2) метаболиты, 3) гистомеханический фактор — снижение трансмурального давления на стенку сосуда вследствие фильтрации части слюны в интерстиций.
Поджелудочная железа. Кровоснабжение эндокринных и экзокринных тканей железы осуществляется через одни и те же сосуды. Капилляры снабжают кровью а-, затем В - клетки островков Лангерганса и далее эндокринные ткани.
Железа иннервирована симпатическими и парасимпатическими нервами, сосуды железы — только симпатическими. Стимуляция симпатических нервов вызывает сужение сосудов и торможение секреции. Длительная стимуляция симпатических нервов приводит к "ауторегуляторному ускользанию". Увеличение кровотока в железе вызывают вещества, расслабляющие гладкие мышцы сосудов (АТФ, АДФ, брандикинин, холецистокинин и др.).
Функциональная гиперемия железы, возникающая при приеме пищи, связана с активацией парасимпатических центров вагуса, выделением соляной кислоты в желудке и эвакуацией пищи в двенадцатиперстную кишку. Освобождающиеся в дуоденум секретин и холецистокинин стимулируют выделение местных метаболитов, увеличивающих панкреатический кровоток. Допускают возможность выделения под влиянием парасимпатических нервов кининов, которые способствуют увеличению кровотока и проницаемости капилляров в поджелудочной железе.
Печень. К печени кровь притекает по печеночной артерии (25-30%) и воротной вене (70-75%). По прохождении капиллярной сети кровь дренируется в систему печеночных вен, которые впадают в нижнюю полую вену. Важной особенностью сосудистого русла печени является наличие большого количества анастомозов между
сосудами систем воротной вены, печеночной артерии и печеночных вен. При значительном повышении давления в системе портальной вены, вызванном затруднениями венозного оттока из печени (портальная гипертензия при циррозах), кровь шунтируется через многочисленные коллатерали в систему нижней и верхней полых вен.
Давление в печеночной артерии соответствует давлению в других магистральных сосудах — 100- 120 мм рт.ст. В воротной вене оно в 10 раз меньше и составляет около 10 мм рт.ст., в синусоидах — 3-5 мм рт.ст., в печеночных венах — 2-3 мм рт.ст. Такая небольшая разница между портальным давлением и давлением в печеночных венах оказывается достаточной для портального кровотока вследствие низкого сопротивления портальных сосудов.
Величина кровотока через печень человека составляет около 100 мл/100 г/мин, т.е. 20-30% от величины сердечного выброса. На долю портального кровотока приходится 70- 80% этого объема, а на долю кровотока в печеночной артерии 20-30%. При максимальной вазодилатации кровоток в печени может возрастать до 5000 мл/мин, т.е. примерно в 3 раза.
Важную роль в поддержании постоянства кровотока через печень играют артерио- портальные взаимоотношения, характеризующиеся четко выраженной реципрокностью. При усилении кровотока в воротной вене (при функциональной гиперемии желудочно-кишечного тракта в процессе пищеварения) кровоток в печеночной артерии уменьшается и, напротив, снижение объемной скорости кровотока в портальной системе приводит к увеличению артериальной перфузии печени.
Печень является одним из органов, выполняющих функцию депо крови в организме (в норме в печени содержится свыше 500 мл крови). За счет этого поддерживается оптимальный объем циркулирующей крови (например, при кровопотере) и обеспечивается необходимая в каждой конкретной гемодинамической ситуации величина венозного возврата крови к сердцу.
Отток венозной крови от печени происходит ритмически, его колебания тесно связаны с фазами дыхательного цикла. Во время вдоха происходит механическое сдавление сосудистого ложа желудочно-кишечного тракта, что увеличивает приток крови по портальной вене, кроме того, наличие отрицательного давления в грудной клетке оказывает присасывающее действие, усиливая кровоток в печеночных венах и нижней полой вене; оба указанных фактора обеспечивают значительный рост венозного оттока из печени при вдохе. Во время выдоха имеют место обратные отношения.
Ми о генная регуляция наиболее выражена и обеспечивает высокую степень ауторегуляции кровотока в печени. Даже небольшое увеличение объемной скорости портального кровотока приводит к сокращению гладких мышц воротной вены, что ведет к уменьшению ее диаметра, а также включает миогенную артериальную кон-стрикцию в печеночной артерии. Оба этих механизма направлены на обеспечение постоянства кровотока и давления в синусоидах.
Гуморальная регуляция. Адреналин вызывает сужение воротной вены, активируя расположенные в ней а- адренорецепто-
309
ры. Действие адреналина на артерии печени сводится, преимущественно, к вазодилатации вследствие стимуляции преобладающих в печеночной артерии В-адренорецелторов. Норадреналин при действии как на артериальную, так и на венозную систему печени приводит к сужению сосудов и повышению сосудистого сопротивления в обоих руслах, что ведет к уменьшению кровотока в печени. Ангиотензин суживает как портальные, так и артериальные сосуды печени, значительно уменьшая при этом кровоток в них. Ацетил-холин расширяет артериальные сосуды, увеличивая приток артериальной крови к печени, но сокращает печеночные венулы, ограничивая отток венозной крови из органа, что приводит к увеличению портального давления и увеличению объема крови в печени.
Метаболиты и тканевые гормоны (двуокись углерода, аденозин, гистамин, брадикинин, простагландин) вызывают сужение портальных венул, уменьшая портальный кровоток, но расширяют печеночные артериолы, усиливая приток артериальной крови к печени (ар-териализация печеночного кровотока). Другие гормоны (глюкокорти-костероиды, инсулин, глюкагон, тироксин) вызывают увеличение кровотока через печень вследствие усиления метаболических процессов в печеночных клетках. Возможно, что их действие опосредовано адреналином или тканевыми гормонами.
Нервная регуляция выражена сравнительно слабо. Вегетативные нервы печени идут от левого блуждающего нерва (парасимпатические) и от чревного сплетения (симпатические). Электрическая стимуляция блуждающего нерва существенно не влияет ни на скорость печеночного кровотока, ни на его распределение в органе. Стимуляция печеночных симпатических нервов повышает сосудистое сопротивление в печеночной артерии и в воротной вене. Феномен "ауторегуляторного ускользания" от симпатических влияний отмечается только в печеночных артериальных сосудах и отсутствует в портальной сосудистой системе.
Кожа. Кожа снабжается кровью из артерий, расположенных в подкожной клетчатке, которые, разветвляясь и широко анастомози-руя между собой, образуют глубокие и поверхностные сплетения. Одной из особенностей сосудов кожи является наличие большого числа артерио-венозных анастомозов, играющих важную роль в терморегуляции. Наибольшее число их находится в коже пальцев рук и ног, ушных раковин, кончика носа, т.е. там, где объем ткани мал по сравнению с поверхностью.
Кожа в большей степени, чем другие органы, подвержена прямому действию высоких и низких температур, ультрафиолетовых лучей, механических факторов и т.д. Кровоток по ее сосудам значительно превышает собственные нутритивные потребности. Это объясняется тем, что выполнение важнейшей функции кожи человека — участие в терморегуляции — определяется не активностью метаболических процессов в ней, а теплопереносящей функцией кровотока.
В покое, при нейтральной температуре внешней среды, кожа получает от 5 до 10% сердечного выброса. Суммарный кожный
310
кровоток взрослого человека при этом составляет 200- 500 мл/мин. В различных частях поверхности тела кожный кровоток значительно отличается. Например, в коже спины он составляет 9.5 мл/100 г/ мин, на передней поверхности тела 15.5 мл/100 г/мин. Наиболее интенсивный кровоток отмечается в коже пальцев рук и ног, где находится большое количество артерио-венозных анастомозов.
Диапазон возможного возрастания кровотока в коже велик: отношение объемной скорости кровотока в покое к максимальной его величине составляет 1:8, Максимальной величины кожный кровоток у человека достигает при тепловом стрессе. В условиях высокой внешней температуры он может возрастать с 200-500 мл/мин до 2.5-3 л/мин, а при продолжительном нагревании организма человека (температура кожи 42°С) увеличивается до 8 л/мин, составляя 50- 70% сердечного выброса.
Нервная регуляция кровоснабжения кожи обеспечивается широко представленной иннервацией ее сосудов (особенно артерио-венозных анастомозов) симпатическими адренергическими сосудосуживающими волокнами. Повышение тонуса симпатических адренер-гических волокон обуславливает сужение кожных сосудов, а торможение их активности приводит к вазодилатации.
Главным фактором в регуляции кожного кровотока является температура тела, снижение которой приводит к рефлекторному сужению как артериальных, так и венозных сосудов кожи, что способствует перемещению крови в глубокие вены и сохранению тепла. При общем охлаждении снижается кровоток как через артерио-венозные анастомозы, так и через капилляры кожи. Эта реакция опосредована через гипоталамус, а эффекторными ее путями являются адренергические нервные волокна. При общем воздействии на организм высоких температур происходит увеличение кожного кровотока за счет, главным образом, раскрытия артерио-венозных анастомозов, кровоток через которые увеличивается в 3-3.5 раза. Раскрытие анастомозов является следствием угнетения сосудосуживающей импульсации к кожным сосудам по симпатическим адренерги-ческим волокнам, обуславливающим стимуляцию альфа- адреноре-цепторов. Однако, этим объясняется лишь первоначальное увеличение кровотока, например, в коже кисти при тепловом стрессе. Последующее выраженное увеличение кровотока в сосудах кожи, проявляющееся при повышении температуры тела, связывают с активной нейрогенной вазодилатацией. Медиатором активной кожной вазодилатации является гистамин и допамин. Эти вазомоторные ответы развиваются в областях кожи или слизистых верхних дыхательных путей, играющих основную роль в теплоотдаче. Активный вазодилататорный компонент терморегуляторного рефлекса непременно сопряжен с включением других эффекторов терморегуляции: у человека и приматов — потоотделения, у собак, овец — тепловой одышки.
Сосуды кожи являются также эффекторным звеном хемо-, баро-рецепторных и других рефлексов. У человека при гипобарической гипоксии, например, кровоток в коже увеличивается. При стимуля-
311
ции каротидных хеморецепторов (гипоксемия и гиперкапния) расширяются кожные вены, а вены внутренних органов при этом суживаются. Рефлекторные изменения кровотока в коже при раздражении хеморецепторов связаны с уменьшением тонуса вазоконстрик-торов. При барорефлексах реакции сосудов в коже проксимальных и дисталъных отделов конечностей проявляются различным образом. У человека и животных в этих барорефлексах участвуют лишь артериальные сосуды проксимальных отделов конечностей (например, сосуды кожи предплечья у человека), которые отвечают констрикцией на снижение артериального и центрального венозного давления. Повышение давления в каротидном синусе, напротив, вызывает дилатацию сосудов кожи предплечья. Сосуды кожи дистальных отделов конечностей — кисти у человека — нечувствительны к баро-рецепторным влияниям. Венозные сосуды кожи также не участвуют в рефлексах с барорецепторов зон низкого и высокого давления.
Гуморальная регуляция. В коже имеется большое количество тучных клеток — источника вазоактивных веществ. Дегра-нуляция тучных клеток и выделение вазоактивных веществ (гиста-мина, серотонина и др.) происходит при непосредственном воздействии на кожу ультрафиолетового облучения, механических и других факторов. В сосудах кожи имеются Н1- и Н2-гистаминовые рецепторы, опосредующие вазодилататорное действие эндогенного и экзогенного гистамина. Расширение сосудов кожи вызывает субстанция Р, оказывая при этом как прямое влияние на гладкую мышцу сосудов, так и опосредованное — через гистамин, выделяющийся из тучных клеток. В коже происходит биосинтез простагландинов. Внутрикожное введение простагландинов Е2 и Н2 вызывает расширение кожных сосудов, а простагландина F2a — сужение их.
Температура самой крови является фактором, играющим важную роль в локально действующих механизмах контроля сосудистых функций в коже. При локальном нагревании кожи имеет место увеличение капиллярного кровотока без существенных изменений кровотока через артерио-венозные анастомозы. В механизме вазо-дилатации при локальном нагревании кожи большую роль играет освобождение вазоактивных веществ (АТФ, субстанция Р, гистамин) и накопление метаболитов. Однако, большее значение в развитии гиперемии в этом случае имеет прямое действие тепла на гладко-мышечные элементы кожных сосудов. При повышении температуры крови снижается миогенный тонус и уменьшаются реакции гладких мышц сосудов кожи на симпатическую импульсацию и вазокон-стрикторные вещества, в частности, на норадреналин. Снижение адренореактивности гладких мышц кожных сосудов под влиянием гипертермии связано с уменьшением чувствительности их альфа-адренорецепторов. Венодилатация в результате локального действия тепла обусловлена, главным образом, снижением чувствительности кожных вен к адренергическим воздействиям, тогда как расширение артериальных сосудов кожи — снижением их миогенного тонуса.
При локальном действии на кожу низких температур имеет место вазоконстрикция и снижение кожного кровотока, что обусловлено
312
как повышением сосудистого тонуса, так и увеличением вязкости крови.
Почка является одним из наиболее высоко снабжаемых кровью органов — 400 мл/100 г/мин, что составляет 20-25% сердечного выброса. Удельное кровоснабжение коркового вещества значительно превышает кровоснабжение мозгового вещества почки. У человека через корковое вещество почки протекает 80- 90% общего почечного кровотока. Медуллярный кровоток мал только в сравнении с корковым, однако, если сравнивать его с другими тканями, то он, например, в 15 раз выше, чем в покоящейся скелетной мышце.
Гидростатическое давление крови в капиллярах клубочков значительно выше, чем в соматических капиллярах, и составляет 50-70 мм рт.ст. Это обусловлено близким расположением почек к аорте и различием диаметров афферентных и эфферентных сосудов корковых нефронов. Существенной особенностью кровотока в почках является его ауторегуляция, особенно выраженная при изменениях системного артериального давления в диапазоне от 70 до 180 мм рт.ст.
Метаболизм в почках протекает более интенсивно, чем в других органах, включая печень, головной мозг и миокард. Интенсивность его определяется величиной кровоснабжения почек. Эта особенность характерна именно для почек, поскольку в других органах (мозг, сердце, скелетные мышцы) наоборот — интенсивность метаболизма определяет величину кровотока.
Гуморальная регуляция. Ангиотензин II (AT II) является мощным вазоконстриктором для сосудов по1ек, он влияет на почечный кровоток также опосредованно, стимулируя выброс медиатора из симпатических нервных окончаний. Кроме непосредственного действия на сосуды AT II стимулирует выработку альдостерона и антидиуретического гормона, которые, в свою очередь, усиливают констрикторный эффект в сосудах почек.
Почечные простагландины оказывают на сосуды почки выраженное дилататорное действие. В состоянии покоя простагландины практически не участвуют в регуляции почечного кровотока, однако, их активность резко возрастает при любых вазоконстрикторных эффектах, что и обуславливает ауторегуляцию почечного кровотока. Недостаточный синтез простагландинов является существенным фактором в развитии артериальной гипертензии.
Кинины являются местным гуморальным фактором регуляции коркового кровотока в почках. Действуя на кининовые рецепторы в сосудах, они вызывают вазодилатацию, увеличивая почечный кровоток и активируя натрийурез.
Катехоламины, воздействуя на а- адренорецепторы сосудов почек, вызывают их констрикцию, преимущественно, в корковом слое. До-памин в малых дозах вызывает в почках вазодилатацию, воздействуя на допаминовые рецепторы. При больших концентрациях допамин, влияя на «-адренорецепторы, вызывает вазоконстрикцию, наиболее выраженную в корковом слое почки.
Вазопрессин, наряду со специфическим влиянием на канальцы почек, вызывает констрикцию артериол, усиливает действие катехо-
313
ламинов, перераспределяет кровоток в почке, повышая корковый и снижая мозговой кровоток. Вазопрессин подавляет секрецию ренина и стимулирует синтез простагландинов. Ацетилхолин, воздействуя на гладкие мышцы артериол и повышая активность внутрипочечных холинергических нервов, увеличивает почечный кровоток. Секретин также вызывает увеличение общего почечного кровотока.
Накопление продуктов метаболизма (СО2), состояние гипоксии ведет к снижению кортикального кровотока без изменения медуллярного кровотока. Аденозин вызывает вазоконстрикцию, уменьшая общий почечный кровоток, при этом происходит перераспределение кровотока в пользу мозгового вещества почки.
Нервная регуляция. По сравнению с гуморальными факторами нервная регуляция почечного кровотока выражена меньше. Постганглионарные симпатические нервные волокна локализованы в перивазальной ткани основной, междолевых, междольковых артерий и достигают артериол коркового слоя, реализуя констрикторные эффекты через а-адренорецепторы. Сосуды почки, особенно мозгового слоя, иннервируются симпатическими холинергическими нервными волокнами, которые оказывают значительный вазодилататорный эффект.
Миогенная регуляция обеспечивает, в основном, ауторе-гуляцию кровоснабжения почек. Базальный тонус почечных сосудов определяется уровнем внутрисосудистого давления. Миогенными реакциями прегломерулярных сосудов обуславливается относительно постоянный уровень общего почечного кровотока в диапазоне колебаний системного давления крови от 70 до 180 мм рт.ст.
Скелетные мышцы. Большая масса скелетных мышц (около 40% массы тела) обуславливает необходимость обеспечения значительного кровотока в мышцах при их сокращении.
В покое интенсивность кровотока в скелетных мышцах колеблется от 2 до 5 мл/100 г/мин, что составляет 15-20% величины сердечного выброса. Функциональный резерв для увеличения кровотока в мышцах при физической работе обеспечивается высоким исходным базальным тонусом сосудов скелетных мышц.
С учетом возрастания системного артериального давления и ди-латации сосудов кровоток в мышцах при их интенсивной работе может возрасти более чем в 30 раз, достигая величины 100- 120 мл/ 100 г/мин (80-90% сердечного выброса). Потребление кислорода мышцами при этом увеличивается с 0.3 мл/100 г/мин до 6 мл/100 г/мин. Возросшая интенсивность метаболических процессов обеспечивается значительным увеличением числа функционирующих капилляров. В покое сткрыто 20-30%, имеющихся в мышце, капилляров. При работе скелетных мышц число функционирующих в них капилляров увеличивается в 2-3 раза.
М и о г е нн а я регуляция. В скелетных мышцах с их широким диапазоном активности обменных процессов высокий исходный тонус сосудов обусловлен, главным образом, миогенной активностью сосудистой стенки и в меньшей степени — влиянием симпатичес-
314
ких вазоконстрикторов (15-20% тонуса в покое нейрогенного происхождения). Ауторегуляция кровотока наиболее выражена при высоком исходном тонусе сосудов.
В условиях интенсивной мышечной работы сократительная активность гладких мышц сосудов снижена. Согласно гистомеханической гипотезе, сокращение мышц изменяет конфигурацию их артериол, тем самым уменьшая их продольное напряжение, что ведет к снижению спонтанной активность гладкомышечных клеток, расширению сосудов и увеличению интенсивности кровотока в работающей мышце.
Нервная регуляция сосудов скелетных мышц осуществляется через симпатические адренергические вазоконстрикторы. В артериях скелетных мышц имеются а- и В- адренорецепторы, в венах только а-адренорецепторы. Активация а-адренорецепторов приводит к сокращению миоцитов и сужению сосудов, активация В-адренорецепторов — к расслаблению миоцитов и расширению сосудов. Сосуды скелетных мышц иннервируются также симпатическими холинергическими нервными волокнами, возбуждение которых оказывает дилататорный эффект. В покое сосуды скелетных мышц находятся под тоническим влиянием симпатических вазоконстрикторов. При каротидных депрессорных рефлексах констрикторный тонус уменьшается и расширение сосудов скелетных мышц, наряду с расширением сосудов чревной области, ведет к снижению общего периферического сопротивления. Рефлекторное уменьшение активности симпатических вазоконстрикторов имеет место в работающих мышцах (функциональный симпатолиз).
Гуморальная регуляция. Наиболее мощным фактором гуморальной регуляции тонуса сосудов являются метаболиты, накапливающиеся в работающей мышце. В межклеточной жидкости и в оттекающей от мышцы венозной крови при этом резко падает содержание кислорода, растет концентрация угольной и молочной кислоты, аденозина. Среди факторов, обеспечивающих снижение тонуса сосудов в мышце при ее работе, ведущими являются быстрое повышение внеклеточной концентрации ионов калия, гиперосмоляр-ность, а также снижение рН тканевой жидкости.
Образующиеся в специализированных клетках серотонин, бради-кинин, гистамин оказывают сосудорасширяющее действие в скелетных мышцах. Адреналин при взаимодействии с а-адренорецептора-ми вызывает констрикцию, с В- адренорецепторами — дилатацию мышечных сосудов, норадреналин обладает сосудосуживающим действием через а-адренорецепторы. Ацетилхолин и АТФ приводят к выраженной дилатации сосудов скелетных мышц.
Сопряженные функции сосудов. Органным сосудам присущи три сопряженные функции: резистивная, емкостная и обменная. Рези cm и в на я функция присуща сосудам всех органов и тканей и определяет величину сопротивления кровотоку. Она характеризует, в основном, физиологические особенности сосудистых гладких мышц: тоническое напряжение и его органную специфичность, биофизические характеристики, закономерности ответов на нервные импуль-
315
сы или вазоактивные вещества, представительство адрено-, холино-рецепторов и т.д. В естественных условиях циркуляции резистивная функция гладких мышц сосудов определяет степень перераспределения кровотока между отдельными сосудистыми областями. Поэтому, сведения о резистивной функции сосудов не позволяют, естественно, судить о кровообращении в исследуемом органе или закономерностях его изменений.
Как уже отмечалось, в артериальном отделе сосудистого русла, играющем наиболее существенную роль в резистивной функции сосудов, содержится только 15- 18% циркулирующей крови. В то же время в области большого объема (или по другой классификации — низкого давления) находится 70-75% крови. В связи с этим для понимания механизмов и закономерностей органного кровообращения немаловажное значение имеет емкостная функция сосудов. Одним из характеризующих ее показателей является изменение венозного оттока из органа при постоянном притоке крови в исследуемую сосудистую область.
Венозные сосуды обладают рядом функций, имеющих существенное значение для обеспечения кровоснабжения органов и тканей. Главной отличительной особенностью венозных сосудов по сравнению с артериальными является то, что они имеют, по крайней мере, две четко выраженные функции: емкостную и резистивную, тогда как артериальным сосудам присуща лишь резистивная функция, а емкостная практически сведена к минимуму. Емкостная функция органных венозных сосудов направлена на формирование венозного возврата крови к сердцу, а резистивная — участвует в обеспечении обменных процессов на органном уровне.
Выявлены органные отличия изменений емкостной функции сосудов и ее высокая лабильность на нервные и гуморальные воздействия. Установлено, что эта функция венозных сосудов в скелетных мышцах и органах спланхнической области изменяется неоднозначно при постоянстве сдвигов резистивной функции сосудов этих органов. Аналогичным образом изменяется эта функция и в сосудах легких, в то время как для сосудов мозга и сердца характерны обратные отношения: в ответ на применение катехоламинов сопротивление сосудов этих органов может изменяться различно, а емкость венозных сосудов всегда уменьшается.
Изменение емкостной функции венозных сосудов, которая выражается в задержке крови в органах или в экстренном поступлении последней в систему кровообращения, формирует адекватный гемо-динамической ситуации возврат крови к сердцу, что обеспечивается активными и пассивными изменениями просвета органных вен. С другой стороны, активные реакции венозных сосудов, изменяя посткапиллярное сопротивление, должны влиять на интенсивность обменных процессов в капиллярах, что, в конечном итоге, и является кардинальной задачей регионарного кровообращения.
В свете сказанного, а также учитывая тот факт, что перфузионное давление и венозные отток (при постоянном артериальном притоке) характеризуют сосудистое русло органа на его "входе" и "выходе",
316
были предприняты специальные поиски возможности исследования микрососудов и их роли в осуществлении транскапиллярного обмена, что вылилось в специальное направление изучения обменной функции сосудов — микроциркуляиию.
 2015-02-15
2015-02-15 1112
1112
