Система – это совокупность материальных объектов (тел), ограниченных каким-либо образом от окружающей среды.
В зависимости от характера взаимодействия с окружающей средой термодинамические системы делятся на три типа:
1) изолированная – система, которая не обменивается с окружающей средой ни веществом, ни энергией;
2) замкнутая – система, которая может обмениваться с окружающей
средой лишь энергией и не может обмениваться веществом;
3) открытая – система, которая обменивается с окружающей средой и
энергией, и веществом.
Живые организмы являются открытыми системами.
Состояние любой термодинамической системы характеризуется двумя группами параметров:
Интенсивными термодинамическими параметрами (давление, температура и др.), не зависящими от массы или числа частиц в системе;
Экстенсивными термодинамическими параметрами (общая энергия, энтропия, внутренняя энергия), зависящими от массы или числа частиц в системе.
Изменение параметров термодинамической системы называется термодинамическим процессом.
Энергию системы (W) можно представить как совокупность двух частей: зависящую от движения и положения системы как целого (W ц) и не зависящую от этих факторов (U).
| W = W ц+ U | (1.1) |
Вторую составляющую этой совокупности U называют внутренней энергией системы.
Она включает энергию теплового движения частиц, а также химическую и ядерную энергию, определяющую поступательное, колебательное и вращательное движение молекул, внутримолекулярное взаимодействие и колебание атомов, энергию вращения электронов.
Внутренняя энергия в свою очередь разделяется на свободную энергию и связанную энергию.
Свободная энергия (G) – та часть внутренней энергии, которая может быть использована для совершения работы.
Связанная энергия (W св) – та часть энергии, которую нельзя превратить в работу.
| U = G + W св | (1.2) |
Потоки и Термодинамические силы. В термодинамических системах, в которых имеются градиенты температуры, концентраций компонентов, химических потенциалов, возникают необратимые процессы теплопроводности, диффузии, химических реакций.
Эти процессы характеризуются тепловыми и диффузионными потоками, скоростями химических реакций и т.д.
Они называются общим термином «потоки» и обозначаются Ji, а вызывающие их причины (отклонения термодинамических параметров от равновесных значений) — термодинамическими силами (Хк).
Связь между Ji и Хк, если термодинамические силы малы, записывают в виде линейных уравнений:
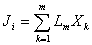
| (1.3) |
где i = 1, 2, …, m
 2015-03-20
2015-03-20 208
208







