Определить адиабатическую температуру горения этилового спирта в воздухе.
Решение: Расчет проводим по схеме, приведенной в табл. 2.3.
1. Так как горючее индивидуальное, для определения объема и состава продуктов горения запишем уравнение химической реакции горения:
С2Н5ОН+3О2+3∙3,76N2=2СО2+3Н2О+3∙3,76N2,
следовательно, продукты горения состоят из:
Vco2=3 моля, VН2О=3 моля, VN2=11,28моля, VПr=17,28 моля.
2. Низшую теплоту сгорания определим по формуле (2.2) Из табл.3приложениянаходим теплоту образования горючего- 278,2кДж/моль: Qн=3∙396,9+3∙242,2-278,2=1639,1 кДж/моль;
3. Средняя энтальпия продуктов горения:
∆Н ср = 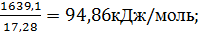
4. Так как ∆Н ср выражена в кДж/моль, по табл.1приложения выбираем, ориентируясь на азот, первую приближенную температуру горения Т1=25000С
5. Рассчитаем теплосодержание продуктов горения при 25000С по формуле (2.13):
Q 1пr=139,9∙3+115,1∙3+85,1∙11,28=1687,2 кДж/моль;
Сравниваем Qн и Qпr,так как Qпr> Qн выбираем температуру горения равной 24000С.
6. Рассчитываем теплосодержание продуктов горения при температуре равной 24000С:
Q 2пr=133,0∙3+109,6∙3+81,5∙11,28=1646,7 кДж/моль; так как Q2 пr> Qн, принимаем температуру равной 23000С
Q 3пr=126,9∙3+104,1∙3+77,8∙11,28=1570,6 кДж/моль.
7. Так как Q3 пr< Qн<Q2 пr определим температуру горения:
Тr *=2300+ 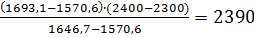 0C
0C
 2015-03-22
2015-03-22 1005
1005








