Подготовка гальванической ванны. Зачистите наждачной бумагой штанги (1) и подвесные крючки (2), промойте аноды (3) и подвесьте их по три штуки на каждую анодную штангу. Соберите схему установки по рис. 28.
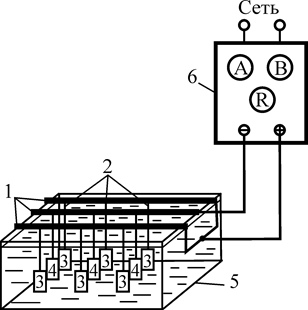
Рис. 28. Схема установки для нанесения металлических покрытий: 1 – штанги, 2 – контактные подвесные крючки (медные), 3 – аноды, 4 – стальные образцы (на катодной штанге), 5 – ванна, 6 – выпрямитель (подключается к сети)
Электролиз ведут в кислых электролитах цинкования или оловянирования (по указанию преподавателя) следующих составов (г/л): цинкование: 200 ZnSO4·7H2O, 30 KAl(SO4)·12H2O, 50 Na2SO4·10H2O, 3 декстрин; режим: температура комнатная; 30 мин; плотность тока 0,0125 А/см2; оловянирование: 50 SnSO4, 100 H2SO4, 20 фенол, 1 столярный клей; режим: температура комнатная; 10 мин; плотность тока 0,012 А/см2.
По заданному режиму рассчитывают величину тока, необходимую для покрытия трех образцов (с обеих сторон!):
I = S к i к, (115)
где I – сила тока, А; i к – катодная плотность тока, А/см2; S к – полная поверхность всех покрываемых образцов, см2.
При выполнении настоящей лабораторной работы обратите внимание на электрическую схему процесса. Проверьте, правильность сборки схемы, наличие контакта, отсутствие обрыва проводов. Прочитайте еще раз инструкцию по технике безопасности на стр. 7. Не включайте схему без проверки!
Залейте электролит в ванну так, чтобы полностью погрузить в него аноды, но медные контактные крючки не должны быть опущены в электролит.
Подготовка образцов к нанесению покрытия. Штангенциркулем замерьте размеры четырех стальных образцов с точностью ±0,1 мм. Зачистите их наждачной бумагой и обезжирьте органическим растворителем протиркой ватой или тампоном с содой (по указанию лаборанта). Промойте образцы горячей и холодной водой, критерий полного обезжиривания – полное смачивание образцов водой. От качества обезжиривания зависит качество получаемого покрытия, его пористость, защитные свойства и сцепление с подложкой. Вытрите образцы промоканием фильтровальной бумагой и высушите на сушке.
Взвесьте три образца вместе на аналитических весах с точностью до четвертого знака, четвертый образец отложите, он будет нужен для других испытаний.
Получение покрытия. Три образца завесьте в ванну на катодную штангу (центральную), включите выпрямитель и установите нужную силу тока (на амперметре, встроенном в выпрямитель). Ведите электролиз заданное время, затем выньте образцы, промойте холодной проточной водой, вытрите, высушите и снова взвесьте (все образцы вместе). Запишите результаты в табл. 25.
Таблица 25
| Показатели процесса | |
| Материал образца | |
| Полная поверхность, см2 | |
| Масса образцов, г: | |
| до покрытия | |
| после покрытия | |
| Масса покрытия, г | |
| Режим покрытия: | |
| сила тока, А | |
| напряжение, В | |
| продолжительность, ч | |
| Средний выход по току, % | |
| Показатели свойств покрытия | |
| Толщина слоя покрытия, мкм | |
| по расчету | |
| по капельному методу | |
| Пористость, % | |
| Полярность покрытия: | |
| показания прибора, мА | |
| полярность | |
| Оценка коррозионной стойкости |
Средний выход металла по току рассчитывают по формуле:
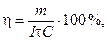 (116)
(116)
где η – выход металла по току, %; m – масса выделившегося металла покрытия, г; I – сила тока, А; τ – время электролиза, ч; С – электрохимический эквивалент осаждаемого металла, г/(А·ч) (для цинка 1,22; для олова 2,214).
Толщину покрытия вычисляют по формуле:
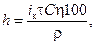 (117)
(117)
где h – толщина покрытия, мкм; i к – катодная плотность тока, А/см2; ρ – плотность металла покрытия, г/см3.
Для определения толщины покрытия капельным методом применяют растворы: дли цинка 200 г KI + 100 г I2 в 1 л воды (одна капля раствора за 1 мин растворяет при 20 °С 1,24 мкм, при 25 °С - 1,45 мкм цинка); для олова – раствор 90 г FeCl3·6H2O + 146 г CuSO4·5H2O + 348 мл CH3COOH (80 %);одна капля этого раствора растворяет за 30 с при 20 °С 1,75 мкм и при 25 °С 1,90 мкм олова.
Из капельницы наносят на поверхность первого (№1) из покрытых образцов одну каплю раствора и по секундомеру отмечают время: через 1 мин. каплю снимают фильтровальной бумагой и на то же место наносят другую каплю опять на 1 мин, пока для цинкового покрытия не появится участок основного металла, свободный от покрытия и равный половине поверхности, занимаемой каплей. Для оловянного покрытия появляется розовое пятно контактно выделившейся меди на стали (то есть все покрытие снялось каплями реактива). По общему числу капель определяют толщину. Средний результат от трех измерений заносят в таблицу результатов.
Определение пористости производится на втором (№2) покрытом образце. На поверхность промытого и высушенного образца накладывают на 5 мин фильтровальную бумагу, смоченную раствором 10 г K3[Fe(CN)6]+ 15 г NaCl в 1 л воды. В сквозных порах покрытия при этом образуется турнбулева синь в результате протекания реакции анодного растворения основного металла (коррозионный гальванический элемент в поре)
3Fe2+ + 2[Fe(CN)6]3- = Fe3[Fe(CN)6]2. (118)
Затем бумагу снимают, аккуратно отмывают от реактива, сушат и подсчитывают число синих точек, приходящихся на 1 см2 поверхности (среднее из 4-5 измерений); на ребрах, краях образца и около отверстия для подвески поры не учитываются. Поверхность 100 точек условно принята равной 1 см2. Вычисленную пористость (%) заносят в табл. 25. Испытание на пористость можно рассматривать как метод ускоренных коррозионных испытаний, так как показателем коррозионной стойкости деталей с защитным покрытием является число очагов коррозии на 1 см2 поверхности. Очаг коррозии с продуктами коррозии основного металла (например, ржавчины) возникает в месте несплошности защитного металлического покрытия, то есть в местах сквозной пористости.
Оцените по методике, изложенной в работе 20, защитную способность полученных покрытий по площади, занятой коррозионными повреждениями, исходя из результатов по определению пористости (точка-пора как очаг коррозионного повреждения). Запишите результат в табл. 25.
Определение полярности защитного покрытия по отношению к подложке – стали. Для этого используют третий из покрытых образцов (№3).
В планке-держателе (3) с помощью клемм укрепляют покрытый и непокрытый образцы (рис. 29). После этого образцы погружают в стакан с 3 %-ным раствором NaCl (имитация атмосферной коррозии под пленкой влаги) так, чтобы клеммы были не погружены в раствор.
В цель включают амперметр 4 с помощью нажатия на прерыватель 5 на 5 с и по направлению отклонения стрелки на амперметре 4 определяют полярность покрытия по отношению к основе. Для оловянного покрытия определяют полярность и в 3 %-ном NaCl, и в 3 %-ном C2H2O4 (имитация органической пищевой среды). Результаты записывают в табл. 25.
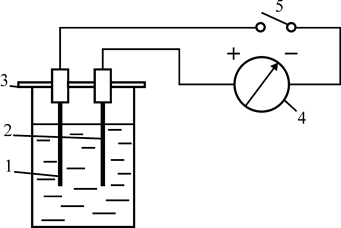
Рис. 29. Схема установки для определения полярности защитного покрытия: 1 – образец с покрытием; 2 – непокрытый стальной образец; 3 – планка-держатель; 4 – миллиамперметр; 5 – прерыватель
 2015-03-22
2015-03-22 1444
1444








