D. Фосфорилирование при участии минерального фосфора.
Е. Фосфорилирование при участии АТФ.
3. У новорожденного наблюдается рвота, понос, общая дистрофия, гепато- и спленомегалия. Данные симптомы исчезают при исключении из пищи молока. Какой главный наследственный дефект в патогенезе?
А. Нарушение обмена галактозы.
В. Нарушение обмена фенилаланина.
С. Гиперсекреция желез внутренней секреции.
D. Нарушение обмена глюкозы.
Е. Недостаточность глюкозо-6-фосфатдегидрогеназы.
4. Фруктоза поступает в организм главным образом в составе:
А. Мальтозы. В. Сахарозы. С. Крахмала. D. Лактозы. Е. Гликогена.
5. У новорожденного, который хорошо себя чувствует при кормлении гру-дным молоком, после добавления в пищу фруктов и соков возникают рвота, боли в животе, диарея, гипогликемия. Назовите возможную причину.
| А. Гипергликемия. | С. Болезнь Гирке. | Е. Наследственная непереносимость фруктозы. |
| В. Кетоз. | D. Глюкозурия. |
6. В регуляции активности ферментов важное место принадлежит постсинтетической ковалентной модификации. Как осуществляется регуляция активности гликогенфосфорилазы и гликогенсинтазы?
| А. Метилирование. | D. АДФ-рибозилирование. |
| В. Аденилирование. | Е. Фосфорилирование-дефосфорилирование. |
| С. Ограниченный протеолиз. |
7. Концентрация глюкозы (ммоль/л) в плазме крови здорового человека находится в пределах:
| А. 2–4. | В. 3,5–5,5. | С. 10–25. | D. 6–9,5. | Е. 1–2. |
8. У больного, 34 года, снижена выносливость к физическим нагрузкам, содержание гликогена в скелетных мышцах повышено. Снижением активности какого фермента это можно объяснить?
| А. Фосфофруктокиназы. | D. Гликогенсинтазы. |
| В. Глюкозо-6-фосфатдегидрогеназы. | Е. Глюкозо-6-фосфатазы. |
| С. Гликогенфосфорилазы. |
9. У новорожденного наблюдается жировое перерождение печени, галактозурия и аминоацидурия. Что необходимо исключить из рациона?
| А. Молочный сахар. | С. Фенилаланин. | Е. Сахарозу. |
| В. Жирные кислоты. | D. Холестерин. |
10. У ребенка с мутацией генов выявлено отсутствие глюкозы-6-фосфатазы, гипогликемия и гепатомегалия. Определите патологию, для которой характерные эти признаки.
| А. Болезнь Гирке. | D. Болезнь Паркинсона. |
| В. Болезнь Кори. | Е. Болезнь Мак-Ардля. |
| С.Болезнь Аддисона. |
11. У ребенка наблюдается увеличение печени, при биопсии выявлен значительный излишек гликогена. Концентрация глюкозы в крови ниже нормы. Что является причиной снижения концентрации глюкозы в крови?
А. Снижена (отсутствует) активность гликогенфосфорилазы в печени
В. Повышена активность гликогенсинтазы.
С. Снижена (отсутствует) активность гексокиназы.
D. Снижена (отсутствует) активность глюкозы-6-фосфатазы.
Е. Дефицит гена, который отвечает за синтез глюкозо-1-фосфатури-
динтрансферазы.
12. Для болезни Гирке характерно накопление гликогена в печени и почках. Дефицит какого фермента является причиной этого нарушения?
| А. Гликогенфосфорилазы. | D. Фосфоглюкомутазы. |
| В. Глюкозо-6-фосфатазы. | Е. Глюкокиназы. |
| С. Киназофосфорилазы. |
13. Пациент, 40 лет, не переносит кисломолочные продукты. Недостаточностью какого фермента пищеварения можно это объяснить?
| А. Амилазы. | С. Мальтазы. | Е. Лактазы. |
| В. Лактатдегидрогеназы. | D. Липазы. |
14. Характерным признаком гликогеноза является боль в мышцах при выполнении физической работы. Наследственная недостаточность какого фермента вызывает эту патологию?
| А. Гликогенфосфорилазы. | D. Амило-1,6-гликозидазы. |
| В. Глюкозо-6-фосфатазы. | Е. Лизосомальной гликозидазы. |
| С. Гликогенсинтетазы. |
15. Какой из указанных углеводов является гетерополисахаридом?
А.Крахмал. В. Глікоген. С. Мальтоза. D. Гепарин. Е. Целлобиоза.
ПРАКТИЧЕСКАЯ РАБОТА
Определение глюкозы в моче
Задание 1. Определить глюкозу в моче пробой Фелинга.
Принцип. Проба Фелинга базируется на способности глюкозы при нагревании восстанавливать Сu2+ в щелочной среде. При этом выпадает желтый осадок гидрата купрума гидроксида или красный осадок купрума оксида.
Ход работы. К 5 каплям реактива Фелинга прибавляют 5 капель мочи. Жидкость перемешивают и нагревают до начала кипения. Следует отметить, что в моче содержится много органических веществ (мочевая кислота, креатинин и др.), которые при длительном кипячении также могут восстанавливать тяжелые металлы. В отличие от этого, восстановление металлов в присутствии глюкозы происходит до кипения.
Фелинга реактив содержит: калий-натрий тартрат, NaOH, купрум (II) сульфат.
Задание 2. Определить глюкозу в моче пробой Ниландера.
Принцип. Проба Ниландера базируется на восстановлении висмута гидроксида до металла в присутствии глюкозы. Соли висмута особенно удобны для определения сахара в моче, поскольку в отличие от купрума висмут не восстанавливается мочевой кислотой.
Ход работы. В пробирку вносят 1 мл мочи, прибавляют реактив Ниландера и осторожно кипятят около двух минут. Сначала появляется коричневое, а затем черное окрашивание.
Ниландера реактив содержит: висмут нитрат, калий-натрий тартрат, аммониак.
Задание 3. Определить глюкозу в моче экспресс-методом (полуколичест-венное определение глюкозы в моче).
Ход работы. В ступке растирают в тонкий порошок 1 г купрум сульфата и 10 г безводного натрий карбоната. На предметное стекло насыпают немного порошка, наносят несколько капель мочи и нагревают до кипения. Синий цвет означает, что глюкоза отсутствует, желто-зеленый указывает на присутствие глюкозы в пределах 0,5%, зеленый - 1%, коричнево-красный - до 2%, интенсивно-красный - выше 2%.
Задание 4. Определить глюкозу в моче с помощью набора «Глюкотест».
Принцип. Метод базируется на визуальной оценке изменения цвета красителя (о -толидина), которым пропитана полоска бумаги «Глюкотест». По цветной шкале, которая содержится в наборе, устанавливают приблизительное содержание глюкозы в моче. Цвет полосок может изменяться от желтого через разные оттенки зеленого к темно-синему в зависимости от количества глюкозы в моче. Этот метод имеет высокую субстратную специфичность и позволяет определить в моче глюкозу в концентрации от 0,09 до 0,5% и выше, имеет важное клиническое значение благодаря высокой специфичности, скорости и простоте выполнения анализа. Больной может самостоятельно контролировать содержание глюкозы в моче и соответственно изменять диету.
Ход работы. Одну полоску «Глюкотеста» смачивают нормальной мочой, а другую - патологической, которая содержит глюкозу. Через несколько минут сравнивают окраску полосок с цветной шкалой. Кон-центрацию глюкозы в моче определяют по цвету полоски, который больше совпадает со шкалой (растворы глюкозы 0,1%, 0,5%, 2% и выше).
Клинико-диагностическое значение. В моче здорового человека глюкоза содержится в незначительном количестве (не выше 0,4 г/л) и не может быть выявлена обычными химическими реакциями. Глюкозурия наблюдается при нарушении гормональной регуляции углеводного обме-на, заболеваниях поджелудочной железы и нарушении реабсорбционной способности почек. Почечную глюкозурию наблюдают при введении в организм большого количества алкоголя, опиума, адреналина и др.
ЛИТЕРАТУРА
1. Губський Ю.І. Біологічна хімія. – Київ-Тернопіль: Укрмедкнига, 2000. – С. 57-71, 176-184, 387-389, 395-396.
2. Губський Ю.І. Біологічна хімія. Підручник. – Київ-Вінниця: Нова книга, 2007. – С. 78-93, 467-468, 477-478, 222-231.
3. Гонський Я.І., Максимчук Т.П., Калинський М.І. Біохімія людини: Підручник. – Тернопіль: Укрмедкнига, 2002. – С. 287-300.
4. Вороніна Л.М. та ін. Біологічна хімія. – Харків: Основа, 2000. – С. 229-245, 274-277.
5. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 1998. – С. 169-187, 319-327.
6. Биохимия: Учебник / Под ред. Е.С. Северина. – М.: ГЭОТАР-МЕД, 2003. – С. 297-333.
7. Николаев А.Я. Биологическая химия. – М.: ООО Медицинское информационное агентство, 1998. – С. 232-237, 246-254.
8. Практикум з біологічної хімії / Бойків Д.П., Іванків О.Л., Кобилянська Л.І./ За ред. О.Я. Склярова. – К.: Здоров’я, 2002. – С. 89-118.
9. Лабораторні та семінарські заняття з біологічної хімії: Навч. посібник для студентів вищих навч. закл. / Л.М. Вороніна, В.Ф. Десенко, А.Л. Загайко та ін. – Х.: Вид-во НФаУ; Оригінал, 2004. – С. 124-147.
ЗАНЯТИЕ 5
Тема: Гликолиз: реакции, энергетика, регуляция. Глюконеоге-нез. Количественное определение лактата в крови и пирувата в моче.
Актуальность. Знание особенностей метаболизма углеводов в организме человека позволяет понять его специфику как в условиях нормы (физиологическое состояние), так и при патологиях (сахарный диабет, заболевания печени и др.). Так как подавляющее большинство животных и растительных клеток в норме находится в аэробных условиях, углеводы окисляются полностью до СО2 и Н2О с помощью цикла Кребса, при этом из глюкозы высвобождается вся биологически доступная энергия. Знание путей окисления глюкозы является важным для будущих врачей в связи с их возможной коррекцией, а также для понимания их роли в энергообмене и пластических процессах в клетке.
Цель. Ознакомиться с аэробным и анаэробным окислением глюкозы и глюконеогенезом, их ролью в организме. Ознакомиться с методами количественного определения лактата и пирувата в биологических жидкостях и их клинико-диагностическим значением.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Пути внутриклеточного катаболизма моносахаридов. Аэробное и анаэробное окисление глюкозы, общая характеристика процессов.
2. Анаэробное окисление глюкозы – гликолиз: последовательность ферментативных реакций, биологическая роль, локализация в организме и клетке.
3. Гликолитическая оксидоредукция, субстратное фосфорилирование в гликолизе. Энергетический баланс анаэробного окисления глюкозы.
4. Регуляция гликолиза. Ключевые ферменты процесса.
5. Спиртовое и другие виды брожения.
6. Стадии аэробного окисления глюкозы.
7. Окислительное декарбоксилирование пировиноградной кислоты: ферменты, коферменты, последовательность реакций, регуляция функционирования пируватдегидрогеназного комплекса.
8. Взаимоотношения анаэробного и аэробного путей окисления глюкозы в клетке. Эффект Пастера.
9. Окисление цитозольного НАДН в митохондриях (глицеролфосфатный и малат-аспартатный челночные механизмы).
10. Сравнительная характеристика биоэнергетики аэробного и анаэробного окисления глюкозы.
11. Биосинтез глюкозы – глюконеогенез: субстраты, ключевые ферменты, реакции, внутримолекулярная локализация, физиологическое значение процесса. Энергетическое обеспечение глюконеогенеза.
12. Метаболическая и гормональная регуляция глюконеогенеза.
13. Взаимосвязь и реципрокная регуляция гликолиза и глюконеогенеза в организме. Глюкозо-лактатный и глюкозо-аланиновый циклы.
ТЕСТОВЫЕ ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ
1. Какое соединение включается в реакцию субстратного фосфорилирова-ния в процессе гликолиза?
| А. Глюкозо-6-фосфат. | D. Глицеральдегид-3-фосфат. |
| В. Фосфоенолпируват. | Е. 2-Фосфоглицериновая кислота. |
| С. Фруктозо-1,6-дифосфат. |
2. Выберите соединение, которое является субстратом глюконеогенеза.
А. Гликоген. В. Глюкоза. С. Пируват. D. Фруктоза. Е. Галактоза.
3. После интенсивной тренировки у спортсмена активируется глюконеогенез в печени. Назовите основной субстрат этого процесса.
| А. Серин. | D. Аспарагиновая кислота. |
| В. Лактат. | Е. Глютаминовая кислота. |
| С. α-Кетоглутарат. |
4. Назовите фермент, который катализирует реакцию образования глюкозо-6-фосфата из глюкозы в печени.
| А. Гексозофосфатизомераза. | D. Глюкозо-6-фосфатаза. |
| В. Глюкокиназа. | Е. Фосфоглюкомутаза. |
| С. Пируваткиназа. |
5. Укажите конечные продукты анаэробного гликолиза.
А. СО2 и Н2О. В. Оксалоацетат. С. Малат. D. Пируват. Е. Лактат.
6. У ребенка с признаками анемии установлен дефицит пируваткиназы в эритроцитах. Какой процесс в эритроцитах при этом нарушен?
| А. Окислительное фосфорилирование. | D. Распад пероксидов. |
| В. Тканевое дыхание. С. Анаэробный гликолиз. | Е. Дезаминирование аино-кислот. |
7. Выберите главный регуляторный фермент гликолиза.
| А. Фосфофруктокиназа. | D. Сукцинатдегидрогеназа. |
| В. Фосфорилаза. | Е. Пируваткиназа. |
| С. Лактатдегидрогеназа. |
8. Выберите фермент необратимой реакции гликолиза.
| А. Пируваткиназа. | D. Глицеральдегидфосфатдегидрогеназа. |
| В. Альдолаза. | Е. Триозофосфатизомераза. |
| С. Фосфоглицераткиназа. |
9. Назовите фермент, который катализирует преобразование пирувата в аэробных условиях.
| А. Пируватдегидрогеназа. | D. Гексокиназа. |
| В. Лактатдегидрогеназа. | Е. Триозофосфатизомераза. |
| С. Альдолаза. |
10. Выберите соединение, которое не образуется в процессе окислительного декарбоксилирования пирувата:
А. Ацетил-КоА. В. СО2. С. НАДН. D. Глицерол-3-фосфат. Е. ФАДН2 .
11. Укажите конечные продукты аэробного превращения глюкозы в тканях человека.
А. Лактат. В. Пируват. С. СО2 и Н2О. D. Малат. Е. Ацетон.
12. Вторым этапом аэробного окисления глюкозы является окислительное декарбоксилирование ПВК. Назовите основной продукт этого процесса.
| А. Сукцинил-КоА. | С. Цитрат. | Е. Ацетил-КоА. |
| В. Пируват. | D. Оксалоацетат. |
13. Для жизнедеятельности эритроцитов необходима энергия в виде АТФ. Какой процесс обеспечивает эти клетки необходимым количеством АТФ?
| А. Анаэробный гликолиз. | D. Цикл трикарбоновых кислот. |
| В. Аэробное окисление глюкозы. | Е. β-Окисление жирных кислот. |
| С. Пентозофосфатный цикл. |
14. Ферменты гликолиза локализованы в:
А. Митохондриях. В.Ядре. С.Цитоплазме. D.Микросомах. Е.Полисомах.
15. Углеводы не являются незаменимыми факторами питания, так как они синтезируются в организме путем глюконеогенеза из:
А. Глицерина, жирных кислот, лейцина.
В. Лактата, холестерина, карнитина.
С. Аланина, глицерина, лактата.
D. Холина, пирувата, ацетил-КоА.
Е. Глутамата, лейцина, масляной кислоты.
16. Какой из перечисленных ферментов катализирует реакцию, которая приводит к образованию макроэргического соединения?
| А. Гексокиназа. | D. Глицеральдегидфосфатдегидрогеназа. |
| В. Фосфофруктокиназа. | Е. Фосфоглицеромутаза. |
| С. Пируваткиназа. |
ПРАКТИЧЕСКАЯ РАБОТА
Определение промежуточных продуктов обмена углеводов -
молочной и пировиноградной кислот в биологических субстратах
Задание 1. Определить содержание молочной кислоты в крови по методу Баркера и Саммерсона.
Принцип. Метод базируется на способности молочной кислоты при нагревании с концентрированной сульфатной кислотой переходить в ацетальдегид, который дает с п -гидроксидифенилом характерную фиолетовую окраску,интенсивность которой пропорциональна её концентрации.
Ход работы. В центрифужную пробирку отмеривают 0,5 мл дистиллированной воды и вносят в нее 0,1 мл крови, взятой микропипеткой из пальца больного. Микропипетку промывают той же водой. К содержимому пробирки прибавляют 1 мл 20% раствора трихлоруксусной кислоты и помещают ее на 10 мин на лед (для лучшего осаждения белков), после чего центрифугируют 5 мин при скорости 3000 об/мин.
Надосадочную жидкость сливают в чистую центрифужную пробирку, приливают 1 каплю 4% раствора купрум сульфата и осторожно наслаивают 3 мл концентрированной сульфатной кислоты, при этом пробирку погружают в лёд и беспрерывно помешивают содержимое стеклянной палочкой. Потом пробирку кипятят на водяной бане и охлаждают ее на ней же до 20°С. К охлажденной смеси приливают 1 каплю свежеприготовленного щелочного раствора п -гидроксидифенила и ставят пробирку на водяную баню при 30°С на 30 мин, взбалтывая содержимое. В пробирке за это время развивается окраска, её помещают на 90 с на бурно кипящую водяную баню, за это время голубая окраска переходит в фиолетовую. Затем смесь охлаждают и фотометруют на ФЕК (зеленый светофильтр) в 10 мм кювете против воды.
Содержание молочной кислоты (Х) в ммоль/л рассчитывают по формуле:
Х = 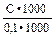 ,
,
где С - количество молочной кислоты в пробе, найденное по калибровочному графику (ммоль); 0,1 - объем крови, взятой на исследование (мл); 1000 в числителе - коэффициент пересчета на 1 л крови; 1000 в знаменателе - коэффициент перевода мкмоль в ммоль.
Клинико-диагностическое значение. В норме содержание молочной кислоты в крови 0,50-2,50 ммоль/л. Увеличение ее концентрации может наблюдаться при усиленной мышечной работе, а также заболеваниях, которые сопровождаются развитием гипоксии (недостаточность сердечной деятельности, хронические бронхиты, анемии и др.).
 2015-03-22
2015-03-22 828
828








