1 – эритроцит, 2 – сегментоядерный нейтрофильный гранулоцит, 3 – палочкоядерный нейтрофильный гранулоцит, 4 – юный нейтрофильный гранулоцит, 5 – эозинофильный гранулоцит, 6 – базофильный гранулоцит, 7 – большой лимфоцит, 8 – средний лимфоцит, 9 – малый лимфоцит, 10 – моноцит, 11 – тромбоциты (кровяные пластинки).
 “тени” эритроцитов
“тени” эритроцитов
Эритроциты составляют более 99% клеток крови. Они составляют 45% объема крови. Эритроциты - это красные кровяные тельца, имеющие форму двояковогнутых дисков диаметром от 6 до 9 мкм, а толщиной 1 мкм с увеличением к краям до 2,2 мкм. Эритроциты такой формы называются нормоцитами. Особая форма эритроцитов приводит к увеличению диффузионной поверхности, что способствует лучшему выполнению основной функции эритроцитов – дыхательной. Специфическая форма обеспечивает также прохождение эритроцитов через узкие капилляры.
Кровь имеет красный цвет благодаря присутствующему в эритроцитах белку, который называется гемоглобин. Именно гемоглобин связывает кислород и разносит его по всему организму, обеспечивая дыхательную функцию и поддержание рН крови. Гемоглобин - белок, образованный четырьмя цепями аминокислот. Каждая цепь присоединяется к молекулярной группе, группе гема, которая имеет один атом железа, фиксирующий молекулу кислорода. При этом валентность железа, к которому присоединяется кислород, не изменяется, т.е. железо остается двухвалентным. Гемоглобин, присоединивший к себе кислород, превращается в ярко красное вещество оксигемоглобин. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. После высвобождения кислорода возникает более темное вещество, называемое дезоксигемоглобин. У мужчин в крови содержится в среднем 130 – 1б0 г/л гемоглобина, у женщин – 120 – 150 г/л. В клинических условиях принято вычислять степень насыщения эритроцитов гемоглобином. Это так называемый цветовой показатель. В норме он равен 1. Такие эритроциты называются нормохромными. При цветовом показателе более 1,1 эритроциты гиперхромные, менее 0,85 – гипохромные. Цветовой показатель важен для диагностики анемий различной этиологии.
Содержание эритроцитов в крови обозначают их числом в одном кубическом миллиметре. В норме в крови у мужчин содержится 4,0 – 5,0х10"/л, или 4 млн – 5 млн эритроцитов в 1 мкл, у женщин – 4,5х10"/л, или 4,5 млн в 1 мкл. Повышение количества эритроцитов в крови называется эритроцитозом, уменьшение эритропенией.
Образование эритроцитов происходит в костном мозге путем эритропоэза. Образование идет непрерывно, потому что каждую секунду макрофаги селезенки уничтожают около двух миллионов отживших эритроцитов, которые нужно заменить.
Кровь снабжается клетками в основном при помощи красного костного мозга (тельца миелоидного происхождения). Поэтому у детей практически весь костный мозг-красный, в то время как у взрослого человека его процент составляет только половину, и только в определенных костях производится кровь. Когда лимфоциты переходят в лимфатические узлы, образуются лимфоциты В, участвующие в выработке антител, а когда переходят в тимус, образуются лимфоциты Т, вызывающие отторжения при пересадке органов.
Но каково происхождение крови? Несмотря на то что это еще довольно неясный вопрос, в настоящее время считается, что все клетки крови восходят к одной единственной изначальной клетке - материанской полипотентной клетке, которая порождает различные типы клеток и может воспроизводить сама себя. От нее происходят унопотентные материнские клетки, вынужденные дифференцироваться на эритроциты, лейкоциты или кровяные пластинки.
Этот процесс происходит примерно на третьей неделе жизни человеческого зародыша. И только к четвертому месяцу начинают проявлять активность костный мозг и лимфатические органы.
Для образования эритроцитов требуются железо и ряд витаминов. Железо организм получает из гемоглобина разрушающихся эритроцитов и с пищей. Для образования эритроцитов требуются витамин В12 (цианокобаламин) и фолиевая кислота.
Для нормального эритропоэза необходимы микроэлементы - медь, никель, кобальт, селен. Физиологическими регуляторами эритропоэза являются эритропоэтины, образующиеся главным образом в почках, а также в печени, селезенке и в небольших количествах постоянно присутствующие в плазме крови здоровых людей. Эритропоэтины усиливают пролиферацию клеток-предшественников эритроидного ряда – КОЕ-Э (колониеобразующая единица эритроцитарная) и ускоряют синтез гемоглобина. Они стимулируют синтез информационной РНК, необходимой для образования энзимов, которые участвуют в формировании гема и глобина. Эритропоэтины увеличивают также кровоток в сосудах кроветворной ткани и увеличивают выход в кровь ретикулоцитов. Продукция эритропоэтинов стимулируется при гипоксии различного происхождения: пребывание человека в горах, кровопотеря, анемия, заболевания сердца и легких. Эритропоэз активируется мужскими половыми гормонами, что обусловливает большее содержание эритроцитов в крови у мужчин, чем у женщин. Стимуляторами эритропоэза являются соматотропный гормон, тироксин, катехоламины, интерлейкины. Торможение эритропоэза вызывают особые вещества – ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, например у спустившихся с гор людей. Тормозят эритропоэз женские половые гормоны (эстрогены), кейлоны. Симпатическая нервная система активирует эритропоэз, парасимпатическая – тормозит. Нервные и эндокринные влияния на эритропоэз осуществляются, по-видимому, через эритропоэтины.
Об интенсивности эритропоэза судят по числу ретикулоцитов – предшественников эритроцитов. В норме их количество составляет 1 – 2%. Созревшие эритроциты циркулируют в крови в течение 100 – 120 дней. Разрушение эритроцитов происходит в печени, селезенке, в костном мозге посредством клеток мононуклеарной фагоцитарной системы. Продукты распада эритроцитов также являются стимуляторами кроветворения.
Процесс разрушения оболочки эритроцитов и выход гемоглобина в плазму крови называется гемолизом. При этом плазма окрашивается в красный цвет и становится прозрачной – “лаковая кровь”. Различают несколько видов гемолиза.
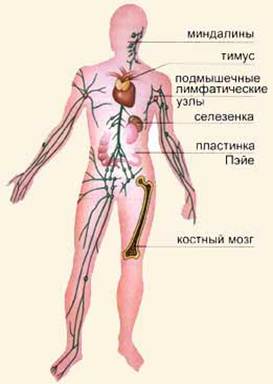
Органы, в которых образуются лейкоциты
Осмотический гемолиз может возникнуть в гипотонической среде. Концентрация раствора NаСl, при которой начинается гемолиз, носит название осмотической резистентности эритроцитов, Для здоровых людей границы минимальной и максимальной стойкости эритроцитов находятся в пределах от 0,4 до 0,34%. Химический гемолиз может быть вызван хлороформом, эфиром, разрушающими белково-липидную оболочку эритроцитов.
Биологический гемолиз встречается при действии ядов змей, насекомых, микроорганизмов, при переливании несовместимой крови под влиянием иммунных гемолизинов.
Температурный гемолиз возникает при замораживании и размораживании крови в результате разрушения оболочки эритроцитов кристалликами льда.
Механический гемолиз происходит при сильных механических воздействиях на кровь, например встряхивании ампулы с кровью.
Скорость оседания эритроцитов (СОЭ) у здоровых мужчин составляет 2 – 10 мм в час, у женщин – 2 – 15 мм в час. СОЭ зависит от многих факторов: количества, объема, формы и величины заряда эритроцитов, их способности к агрегации, белкового состава плазмы. В большей степени СОЭ зависит от свойств плазмы, чем эритроцитов.
Лейкоциты
Лейкоциты или белые кровяные шарики обладают полной ядерной структурой. Их ядро может быть округлым, в виде почки или многодольчатым. Их размер - от 6 до 20 мкм. Количество лейкоцитов в периферической крови взрослого человека колеблется в пределах 4,0 – 9,0х10' /л, или 4000 – 9000 в 1 мкл. Увеличение количества лейкоцитов в крови называется лейкоцитозом, уменьшение – лейкопенией. В клинике имеет значение не только общее количество лейкоцитов, но и процентное соотношение всех видов лейкоцитов, получившее название лейкоцитарной формулы, или лейкограммы.
Каждую секунду погибает примерно 10 миллионов эритроцитов, каждый из которых совершил около 172 000 полных оборотов в системе кровообращения.
Врачи следят за количеством лейкоцитов, поскольку любое его изменение зачастую является признаком болезни или инфекции. Лейкоциты - это пехота, защищающая организм от инфекции. Эти клетки защищают организм путем фагоцитоза (поедания) бактерий или же посредством иммунных процессов - выработки особых веществ, которые разрушают возбудителей инфекций. Лейкоциты действуют в основном вне кровеносной системы, но в участки инфекции они попадают именно с кровью.
Осуществление защитной функции различными видами лейкоцитов происходит по-разному. Нейтрофилы являются самой многочисленной группой. Основная их функция – фагоцитоз бактерий и продуктов распада тканей с последующим перевариванием их при помощи лизосомных ферментов (протеазы, пептидазы, оксидазы, дезоксирибонуклеазы). Нейтрофилы первыми приходят в очаг повреждения. Так как они являются сравнительно небольшими клетками, то их называют микрофагами. Нейтрофилы оказывают цитотоксическое действие, а также продуцируют интерферон, обладающий противовирусным действием. Активированные нейтрофилы выделяют арахидоновую кислоту, которая является предшественником лейкотриенов, тромбоксанов и простагландинов. Эти вещества играют важную роль в регуляции просвета и проницаемости кровеносных сосудов и в запуске таких процессов, как воспаление, боль и свертывание крови. По нейтрофилам можно определить пол человека, так как у женского генотипа имеются круглые выросты – “барабанные палочки”.
Эозинофилы также обладают способностью к фагоцитозу, но это не имеет серьезного значения из-за их небольшого количества в крови. Основной функцией эозинофилов является обезвреживание и разрушение токсинов белкового происхождения, чужеродных белков, а также комплекса антиген-антитело. Эозинофилы продуцируют фермент гистаминазу, который разрушает гистамин, освобождающийся из поврежденных базофилов и тучных клеток при различных аллергических состояниях, глистных инвазиях, аутоиммунных заболеваниях. Эозинофилы осуществляют противоглистный иммунитет, оказывая на личинку цитотоксическое действие. Поэтому при этих заболеваниях увеличивается количество эозинофилов в крови (эозинофилия). Эозинофилы продуцируют плазминоген, который является предшественником плазмина – главного фактора фибринолитической системы крови. Содержание эозинофилов в периферической крови подвержено суточным колебаниям, что связано с уровнем глюкокортикоидов. В конце второй половины дня и рано утром их на 20~ меньше среднесуточного уровня, а в полночь – на 30% больше.
Базофилы продуцируют и содержат биологически активные вещества (гепарин, гистамин и др.), чем и обусловлена их функция в организме. Гепарин препятствует свертыванию крови в очаге воспаления. Гистамин расширяет капилляры, что способствует рассасыванию и заживлению. В базофилах содержатся также гиалуроновая кислота, влияющая на проницаемость сосудистой стенки; фактор активации тромбоцитов (ФАТ); тромбоксаны, способствующие агрегации тромбоцитов; лейкотриены и простагландины. При аллергических реакциях (крапивница, бронхиальная астма, лекарственная болезнь) под влиянием комплекса антиген-антитело происходит дегрануляция базофилов и выход в кровь биологически активных веществ, в том числе гистамина, что определяет клиническую картину заболеваний.
Моноциты обладают выраженной фагоцитарной функцией. Это самые крупные клетки периферической крови и их называют макрофагами. Моноциты находятся в крови 2-3 дня, затем они выходят в окружающие ткани, где, достигнув зрелости, превращаются в тканевые макрофаги (гистиоциты). Моноциты способны фагоцитировать микробы в кислой среде, когда нейтрофилы не активны. Фагоцитируя микробы, погибшие лейкоциты, поврежденные клетки тканей, моноциты очищают место воспаления и подготавливают его для регенерации. Моноциты синтезируют отдельные компоненты системы комплемента. Активированные моноциты и тканевые макрофаги продуцируют цитотоксины, интерлейкин (ИЛ-1), фактор некроза опухолей (ФНО), интерферон, тем самым осуществляя противоопухолевый, противовирусный, противомикробный и противопаразитарный иммунитет; участвуют в регуляции гемопоэза. Макрофаги принимают участие в формировании специфического иммунного ответа организма. Они распознают антиген и переводят его в так называемую иммуногенную форму (презентация антигена). Моноциты продуцируют как факторы, усиливающие свертывание крови (тромбоксаны, тромбопластины), так и факторы, стимулирующие фибринолиз (активаторы плазминогена).
Лимфоциты являются центральным звеном иммунной системы организма. Они осуществляют формирование специфического иммунитета, синтез защитных антител, лизис чужеродных клеток, реакцию отторжения трансплантата, обеспечивают иммунную память. Лимфоциты образуются в костном мозге, а дифференцировку проходят в тканях. Лимфоциты, созревание которых происходит в вилочковой железе, называются Т-лимфоцитами (тимусзависимые).
Различают несколько форм Т-лимфоцитов. Т–киллеры (убийцы) осуществляют реакции клеточного иммунитета, лизируя чужеродные клетки, возбудителей инфекционных заболеваний, опухолевые клетки, клетки-мутанты. Т-хелперы (помощники), взаимодействуя с В-лимфоцитами, превращают их в плазматические клетки, т.е. помогают течению гуморального иммунитета. Т-супрессоры (угнетатели) блокируют чрезмерные реакции В-лимфоцитов. Имеются также Т-хелперы и Т-супрессоры, регулирующие клеточный иммунитет. Т-клетки памяти хранят информацию о ранее действующих антигенах.
В-лимфоциты (бурсозависимые) проходят дифференцировку у человека в лимфоидной ткани кишечника, небных и глоточных миндалин. В-лимфоциты осуществляют реакции гуморального иммунитета. Большинство В-лимфоцитов являются антителопродуцентами. В-лимфоциты в ответ на действие антигенов в результате сложных взаимодействий с Т-лимфоцитами и моноцитами превращаются в плазматические клетки. Плазматические клетки вырабатывают антитела, которые распознают и специфически связывают соответствующие антигены. Различают 5 основных классов антител, или иммуноглобулинов: JgA, Jg G, Jg М, JgD, JgЕ. Среди В-лимфоцитов также выделяют клетки-киллеры, хелперы, супрессоры и клетки иммунологической памяти. О-лимфоциты (нулевые) не проходят дифференцировку и являются как бы резервом Т- и В-лимфоцитов.
Лейкоциты образуются в разных органах тела: в костном мозге, селезенке, тимусе, подмышечных лимфатических узлах, миндалинах и пластинках Пэйе, в слизистой оболочке желудка.
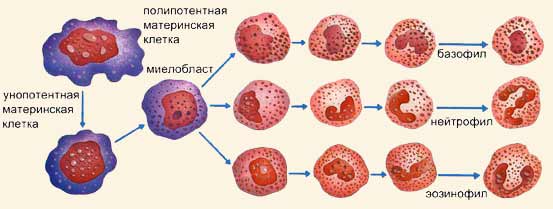
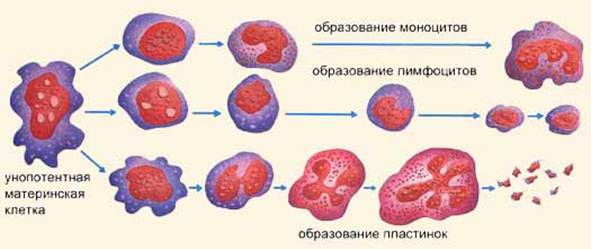
Процесс образования лейкоцитов, известный как лейкопоэз, может быть различным. С одной стороны, происходит процесс, порождающий гранулоциты: унопотентная материнская клетка претерпевает первое преобразование и превращается в миелобласт, с почти круглым ядром, а затем делится на миелоциты, с собственными признаками, которые приведут соответственно к образованию базофилов, нейтрофилов и эозинофилов. Моноциты всегда сохраняют признаки первичной клетки, поэтому они могут образовываться как при последовательных преобразованиях унопотентной материнской клетки, так и непосредственно из полипотентной материнской клетки.
Лейкоциты делятся на две большие группы: гранулоциты и агранулоциты в зависимости от того, наблюдается или нет зернистость в их цитоплазме. У первых имеется ядро различных форм, они осуществляют фагоцитоз. Самые многочисленные и активные - это нейтрофилы (70% от общего числа); кроме них имеются базофилы (1%) и эозинофилы (4%).
Незернистые лейкоциты - это моноциты, большего размера и с большой фагоцитарной активностью, и лимфоциты, подразделяющиеся на малые (90%) и большие (остальные 10%).
 |
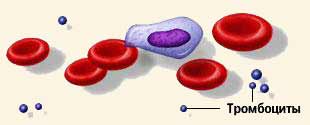
ТРОМБОЦИТЫ
Тромбоциты, или кровяные пластинки – плоские клетки неправильной округлой формы диаметром 2 – 5 мкм. Тромбоциты человека не имеют ядер - это фрагменты клеток, которые меньше половины эритроцита. Количество тромбоцитов в крови человека составляет 180 – 320х109/л, или 180 000 – 320 000 в 1 мкл. Имеют место суточные колебания: днем тромбоцитов больше, чем ночью. Увеличение содержания тромбоцитов в периферической крови называется тромбоцитозом, уменьшение – тромбоцитопенией.
Главной функцией тромбоцитов является участие в гемостазе. Тромбоциты помогают "ремонтировать" кровеносные сосуды, прикрепляясь к поврежденным стенкам, а также участвуют в свертывании крови, которое предотвращает кровотечение и выход крови из кровеносного сосуда. Способность тромбоцитов прилипать к чужеродной поверхности (адгезия), а также склеиваться между собой (агрегация) происходит под влиянием разнообразных причин. Тромбоциты продуцируют и выделяют ряд биологически активных веществ: серотонин (вещество, вызывающее сужение кровеносных сосудов уменьшение кровотока), адреналин, норадреналин, а также вещества, получившие название пластинчатых факторов свертывания крови. Так у тромбоцитов есть различные белки, способствующие коагуляции крови. Когда лопается кровеносный сосуд, тромбоциты прикрепляются к стенкам сосуда и частично закрывают брешь, выделяя так называемый тромбоцитарный фактор III, который начинает процесс свертывания крови путем превращения фибриногена в фибрин. Тромбоциты способны выделять из клеточных мембран арахидоновую кислоту и превращать ее в тромбоксаны, которые, в свою очередь, повышают агрегационную активность тромбоцитов. Эти реакции происходят под действием фермента циклооксигеназы. Тромбоциты способны к передвижению за счет образования псевдоподий и фагоцитозу инородных тел, вирусов, иммунных комплексов, тем самым, выполняя защитную функцию. Тромбоциты содержат большое количество серотонина и гистамина, которые влияют на величину просвета и проницаемость капилляров, определяя тем самым состояние гистогематических барьеров.
 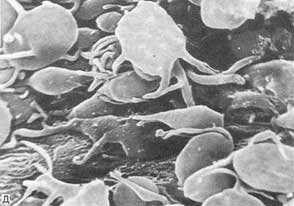 Тромбоциты, прилипшие к стенке аорты в зоне повреждения эндотелиального слоя. Тромбоциты, прилипшие к стенке аорты в зоне повреждения эндотелиального слоя. |
Тромбоциты образуются в красном костном мозге из гигантских клеток мегакариоцитов. Унопотентная клетка претерпевает неполное деление, потому что ядро делится, а цитоплазма нет. В результате образуется мегакариобласт, от цитоплазмы которого в конце отделяются пластинки.
Продукция тромбоцитов регулируется тромбоцитопоэтинами. Тромбоцитопоэтины образуются в костном мозге, селезенке, печени. Различают тромбоцитопоэтины кратковременного и длительного действия. Первые усиливают отщепление тромбоцитов от мегакариоцитов и ускоряют их поступление в кровь. Вторые способствуют дифференцировке и созреванию мегакариоцитов. Продолжительность жизни тромбоцитов составляет от 5 до 11 дней. Разрушаются кровяные пластинки в клетках системы макрофагов.
Активность тромбоцитопоэтинов регулируется интерлейкинами (ИЛ-6 и ИЛ-11). Количество тромбоцитопоэтинов повышается при воспалении, необратимой агрегации тромбоцитов.
В онтогенезе система крови претерпевает изменения, в процессе которых можно выделить несколько узловых моментов. В антенатальном периоде различают три стадии, которые перекрывают друг друга:
I стадия – эмбриональное или желточное кроветворение. Она начинается в стенке желточного мешка со 2-3 недели и продолжается до конца 2-го-начала 3-го месяца внутриутробной жизни;
II стадия – экстрамедуллярное или печеночное кровотворение. Начинается с конца 1-го – начала 2-го месяца эмбрионального развития, когда появляются очаги кроветворения в самом эмбрионе: сначала повсеместно, а затем – преимущественно в печени. На 5-м месяце развития кроветворная функция достигает максимума, а затем постепенно угасает. Начиная с 3-го до 6-го месяцев внутриутробного развития кроветворную функцию начинает выполнять селезенка. Наиболее активно процесс осуществляется на 4-5 месяцах.
III стадия медуллярное кроветворение, которое начинается с 4-го месяца и становиться основным.
У нормального ребенка кроветворение происходит в костном мозге, вначале повсеместно, а затем с 4-х летнего возраста отмечается превращение красного костного мозга в желтый жировой. Этот процесс продолжается до 14-15 лет. К периоду полового созревания кроветворение сохраняется только в костном мозге губчатого вещества тел позвонков, ребер, грудины, костей голени и бедренных костей. Однако при ухудшении функционального состояния организма, патологических состояниях у детей очаги кроветворения могут возникать в местах эмбрионального эритролейкопоэза.
Количество крови у детей не является постоянной величиной и подвержено широким колебаниям в зависимости от возраста и массы ребенка. По отношению к массе тема у новорожденного количество крови составляет около 15%, у детей 1 года – 11%, 3 лет – 8%, 6-9 лет как и у взрослых – 7-8%. У мальчиков относительное количество крови несколько больше, чем у девочек. Больший объём крови у детей связан с более интенсивным обменом веществ.
Соотношение между объёмом кровяных телец и всем объёмом крови (гематокритное число) выше у новорожденных, чем у взрослых. Это объясняется высокой концентрацией эритроцитов. Нормальные для взрослых величины (40-45%) устанавливаются по завершении пубертатного периода.
Первичные эритроциты появляются на стадии эмбрионального кроветворения. На первых неделях развития преобладает примитивный гемоглобин, затем заменяется фетальным гемоглобином. Приблизительно с 16-недели внутриутробного развития начинается синтез гемоглобина взрослого. Важным свойством фетального и примитивного гемоглобинов является их высокое сродство к кислороду и большая диссоциация оксигемоглобина. Это обеспечивает плоду достаточное снабжение тканей кислородом в условиях относительной гипоксии.
Сразу после рождения в крови новорожденного отмечается повышенное содержание гемоглобина. Начиная с 1-2 дня жизни происходит разрушение эритроцитов, выход билирубина в кровь, что приводит к развитию физиологической желтухи ребенка. К 7-10 – му дню после рождения физиологическая желтуха новорожденного проходит.
Продукты разрушения эритроцитов стимулируют повышенный эритропоэз, который в 5 раз выше чем у детей старшего возраста. У новорожденных эритроциты имеют разный размер, обладают ускороченных сроком жизни.
В отличии от новорожденного кровь детей грудного возраста отличается относительно более низким содержанием эритроцитов и гемоглобина.
В последующие годы наблюдаются значительные возрастные колебания количества гемоглобина. В пубертатном периоде отмечается разница содержания гемоглобина и эритроцитов между мальчиками и девочками, что вероятно, связано с развитием мускулатуры.
Лейкоциты впервые появляются в периферической крови в конце 3-го месяца антенатального развития. Постепенно к моменту рождения концентрация лейкоцитов становиться более высокой, чем у взрослого человека. Причем, начиная с 2-го дня жизни увеличивается количество лимфацитов, нейтрофилов уменьшается. К 5-6–му дню после рождения их количество уравнивается. На протяжении всего грудного периода развития отмечаются взаимные колебания лимфоцитов и нейтрофилов. А после первого года жизни количество лейкоцитов снижается и к 12-14 годам устанавливаются такие же взаимоотношения между различными формами лейкоцитов, как и у взрослых.
Тромбоциты уже у новорожденного примерно соответствуют взрослому. В дальнейшем концентрация тромбоцитов практически не меняется. Чем младше ребенок, тем больше у него юных форм тромбоцитов.
Плазма крови у детей мало меняется с возрастом. Наибольшие отклонения по сравнению со взрослыми можно отметить в период новорожденности.
Система свертываемости крови созревает и формируется в период раннего эбриогенеза. В различные периоды жизни процессы свертывания имеют свои особенности. На 8-10- недели внутриутробной жизни появляется реакция сужения сосудов. Однако еще на 16-20 недели внутриутробной жизни кровь не способна свертываться из-за отсутствия фибриногена в плазме, в то время, как концентрация гепарина очень высока. Появляясь на 4-м месяце внутриутробного развития концентрация фибриногена увеличивается постепенно к моменту рождения.
Концентрация факторов свертывающих и противосвертывающих систем не зависит от их содержания в крови матери. Они не проходят через плацентарный барьер, а синтезируются в печени плода. Для системы свертывания крови характерна неравномерность включения отдельных ферментативных систем.
Скорости свертывания крови и у детей и у взрослых мало отличаются, т.к. зависят не от количества отдельных факторов свертывающих систем, а от их соотношения концентраций.
Наибольший размах индивидуальных колебаний показателей системы свертывания крови отмечается в препубертатном и пубертатном периодах, что связано, вероятно, с неустойчивым гормональным фоном.
Иммунитет, как и все другие функции организма, формируется и совершенствуется по мере роста и развития ребенка.
ТЕМА 6. СИСТЕМА КРОВООБРАЩЕНИЯ.
 2015-03-27
2015-03-27 1549
1549