Природные воды почти всегда содержат то или иное количество органических веществ.
С санитарно-гигиенической точки зрения присутствующие в воде органические вещества делятся на две группы:
1) продукты биохимического распада растительных и животных остатков и обмена веществ, главным образом планктонного происхождения (автохтонные);
2) продукты разложения разнообразных отходов, попадающих в воду вместе со сточными водами (аллохтонные).
Основные источники обогащения поверхностных вод органическими веществами:
1) поступление с водосборной площади;
2) образование в самом водном объекте;
3) поступления из подземных водоносных горизонтов;
4) промышленные, хозяйственно-бытовые и сельскохозяйственные стоки.
Ввиду большого разнообразия органических соединений, которые могут содержаться в воде, индивидуальное определение каждого из них может оказаться очень сложным и во многих случаях это нецелесообразно. Наиболее распространенной характеристикой суммарного содержания органических веществ в воде является так называемая ²окисляемость².
²Окисляемость² - это количество кислорода в миллиграммах, расходуемое на окисление всех органических веществ, содержащихся в титре воды.
В зависимости от применяемого окислителя различают перманганатную окисляемость (окислитель KMnO4) и бихроматную окисляемость (окислитель K2Cr2O7). Во избежание ошибки предварительно в исследуемой воде определяют неорганические восстановители (Fe2+, SO32-, H2S). Затем к пробе воды приливают заведомо избыточное количество окислителя и проводят окисление. Определяют количество окислителя, которое осталось непрореагировавшим, и по разности рассчитывают окисляемость анализируемой воды.
Окисление перманганатом проводят в кислой (метод Кубеля) или в щелочной среде (метод Шульца) в зависимости от содержания хлорид-ионов в исследуемой воде. Окисление органических соединений перманганатом калия происходит неполно, поэтому его используют главным образом, как экспресс-метод качественной оценки природных вод.
Органические вещества окисляются более полно бихроматом калия, окисление бихроматом во всех случаях проводят в кислой среде. Этот способ используют для анализа сточных вод, определяя так называемое ХПК – химическое потребление кислорода. Полнота окисления в значительной степени зависит от концентрации серной кислоты. Условия, предписываемые арбитражным методом, позволяют найти значение ХПК близкое к теоретическому (табл.2). Теоретическим значениям ХПК называют количество мг кислорода необходимое для полного окисления 1 мг органического вещества. Расчёт производят, полагая, что углерод, сера, фосфор и другие элементы (кроме азота), присутствующие в органическом веществе, окисляются до СО2, Н2О, Р2О5, SO3 и соответствующих оксидов других элементов, а азот превращается в аммиак. Кислород входящий в состав окисляемых органических веществ, участвует в процессе окисления, а водород этих соединений при наличии азота расходуется на образование аммиака в соотношении N: Н = 3: 1. Например, окисление нитроанилина:
NO2C6H4NH2 + 100 → 6СО2 + 2NH3
моль нитроанилина = 138
10 моль – атомов кислорода = 16 . 10 = 160
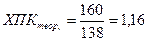 мг/мг.
мг/мг.
Таблица 2
Теоретические значения ХПК для некоторых органических веществ
| Вещество | ХПКтеор., мг/мг. | Вещество | ХПКтеор., мг/мг. |
| анилин | 2,41 | нафталин | 3,00 |
| ацетон | 2,21 | нафтол | 2,42 |
| ацетальдегид | 1,82 | нитробензол | 1,43 |
| бензол | 3,07 | пропиловый спирт | 2,40 |
| бутиловый спирт | 2,59 | резоцин | 1,89 |
| глицерин | 1,21 | октан | 3,51 |
| гептан | 3,52 | толуол | 3,13 |
| диэтиленгликоль | 1,51 | фенол | 2,38 |
| диэтаноламин | 1,52 | фенилендиамин | 1,92 |
| додецилбензолсульфонат | 2,34 | формальдегид | 1,07 |
| натрия (ПАВ) | этиловый спирт | 2,09 | |
| крезол | 2,52 | этаноламин | 1,31 |
| ксилол | 3,17 | этиленгликоль | 1,29 |
| кумол (изопропилбензол) | 3,20 | уксусная кислота | 1,07 |
| масляная кислота | 1,82 |
 2015-03-27
2015-03-27 793
793








