· Зависимость давления газа от концентрации молекул и температуры
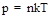
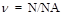
где N — число структурных элементов (молекул, атомов, ионов и т.п.), составляющих тело (систему); NA — постоянная Авогадро: NA =6,02×1023 моль-1.
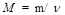
где m — масса однородного тела (системы); v — количество вещества этого тела.
· Относительная молекулярная масса вещества
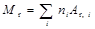
где ni — число атомов i -го химического элемента, входящего в состав молекулы данного вещества; A r, i — относительная атомная масса этого элемента. Относительные атомные массы приводятся в таблице Д. И. Менделеева.
· Связь молярной массы М с относительной молекулярной массой M r вещества
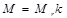
где k=10-3 кг/моль.
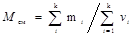 ,
,
где m i — масса i -го компонента смеси; vi — количество вещества i-го компонента смеси; k — число компонентов смеси.
· Массовая доля i -го компонента смеси газов
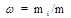
где m i — масса i -го компонента смеси; m — масса смеси.
· Уравнение состояния идеальных газов (уравнение Клапейрона — Менделеева)
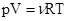 ,
,
где m — масса газа; М — его молярная масса; R — молярная газовая постоянная; Т — термодинамическая температура; v — количество вещества.
· Закон Дальтона
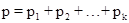
где p — давление смеси газов; pi — парциальное давление i-го компонента смеси; k — число компонентов смеси.
 2015-03-27
2015-03-27 1088
1088
