Отщепление аминогруппы у аминокислоты называют дезаминированием. Различают два типа реакций: прямое и непрямое дезаминирование. Имеется несколько типов прямого дезаминирования. Эти реакции генерируют свободный аммиак — токсическое соединение, подлежащее связыванию и обезвреживанию.
Прямое дезаминирование:
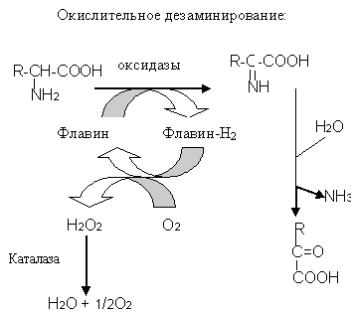
Выделены ферменты, катализирующие окислительное дезаминирование с участием флавиновых коферментов. Эти ферменты обладают выраженной специфичностью к D- и
L-аминокислотам. Они получили название оксидаз аминокислот из-за их способности взаимодействовать с молекулярным кислородом с образованием пероксида водорода. Особо высокой активностью в клетках обладают оксидазы D-аминокислот. Окислительное дезаминирование L-аминокислот при помощи оксидаз аминокислот у большинства млекопитающих обнаружено только в печени и почках. Некоторые из этих реакций не играют важной роли у человека, а некоторые аминокислоты дезаминируются при помощи специальных реакций.
Окислительное дезаминирование глутаминовой кислоты с образованием a-кетоглу-тарата и аммиака:
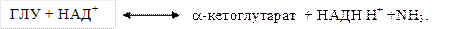
Эта реакция протекает с участием НАД+ или НАДФ+. Фермент — глутаматдегидрогеназа присутствует в митохондриальном матриксе в высоких концентрациях и обладает высокой активностью. Аммиак, полученный в печеночных митохондриях, используется для синтеза мочевины.
Пути обезвреживания аммиака в организме — синтез глутамина и мочевины.
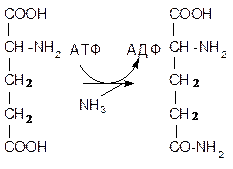 |
1. Синтез глутамина. Реакция катализируется глутаминсинтетазой:
Распределение и субклеточная локализация. Реакция протекает в цитозоле клеток всех тканей, но особенно выражена в мозге, где аммиак наиболее токсичен, и мышцах, где обмен белков мышц сопровождается образованием значительных количеств аммиака.
Функции глутамина:
a) во всех тканях глутамин является донором азота для синтеза важных молекул, в частности, для пуринового и пиримидинового синтеза;
б) является нетоксичной формой транспорта аммиака из разных тканей к клеткам печени, где он превращается в мочевину;
в) в кишечнике служит источником энергии для энтероцитов;
г) в почках участвует в поддержании кислотно-щелочного равновесия. Гидролиз амидной группы в боковой цепи глутамина глутаминазой позволяет связывать протоны. Это особенно важно в условиях метаболического ацидоза.
2. Синтез мочевины. Печень — единственный орган, клетки которого содержат все ферменты синтеза мочевины и, следовательно, являются главным местом ее синтеза. Участвуют митохондриальные ферменты и ферменты цитозоля.
Суммарная реакция синтеза мочевины:
Аспартат + NH3 + CO2 + 3АТФ ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾®
3 H2O + мочевина + фумарат + 2АДФ + АМФ + 2Фн + пирофосфат.
Энергетический баланс. 3 молекулы АТФ расходуется на синтез каждой молекулы мочевины.
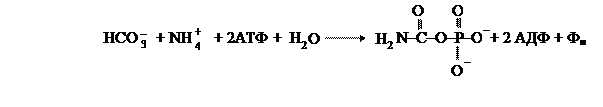 1. Синтез карбамоилфосфата (происходит в митохондриях):
1. Синтез карбамоилфосфата (происходит в митохондриях):
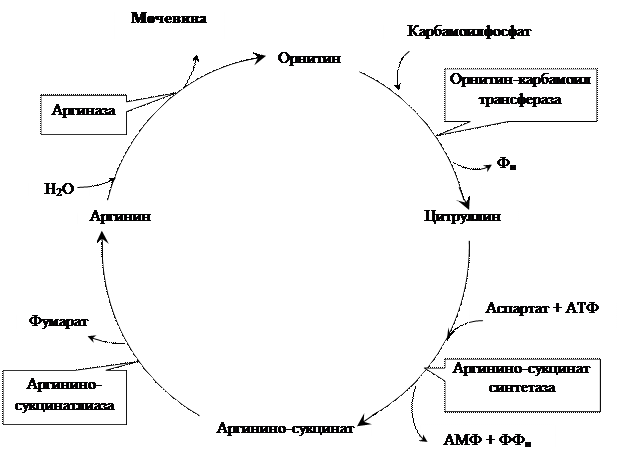 |
2. Орнитиновый цикл мочевинообразования:
 2015-03-20
2015-03-20 1000
1000








