При написании формул гидросолей необходимо помнить, что одноосновные кислоты, содержащие один атом Н (НCl, HNO3 и другие), гидросолей не образуют. Диссоциация такой кислоты приводит к образованию одного вида кислотного остатка: HCl Û H+ + Cl- (который входит в состав солей).
Составим формулы гидросолей:
гидросульфидмагния (разберем последовательно по названию состав соли): H+ S2- Mg2+
HS-
кислотный остаток гидросоли (его заряд определяют по сумме составляющих его атомов), формула соли имеет вид: Mg(HS)2.
По латыни водород в русской транскрипции - гидрогениум, поэтому приставка «гидро» в названии соли по полусистематической (международной) номенклатуре указывает на присутствие одного атома водорода в составе кислотного остатка; наличие двух или трех атомов водорода отражают приставками: дигидро и тригидро.
Д игидр о(орто)фосфа т железа (III) (приставку «орто» в данном случае можно не писать, т.к. метакислота не образует гидросолей):
2H+ PO43- Fe3+
H2PO4- - кислотный остаток, соль имеет вид: Fe(HPO4)3;
гидрофосфат калия:
H+ PO 43- K+
HPO2-, соль - K2HPO4.
Рассмотрим обратную задачу – по формуле соли составим ее название:
Na H 3 SiO 4 – название соли начинаем с кислотного остатка (подчеркнут):
¯ тригидро(орто)силикат (SiO44- - ортосиликат-ион), название соли - тригидроортосиликат натрия.
Ca(HSO 4)2
стехиометрический коэффициент, стоящий за скобками и указывающий количество кислотных остатков (подчеркнуты) не входит в название соли. Он вводится для сохранения ее электронейтральности (равенства положительных и отрицательных зарядов). Кислотный остаток – гидросульфат-ион, соль - гидросульфат кальция.
Получают гидросоли перечисленными выше способами, наиболее часто можно использовать следующие:
1. основание + кислота (или кислотный оксид) - избыток по сравнению с получением средней соли (см. число молей кислоты на 1 моль (1 м) основания):
2KOH + H2CO3 (СО2) = K2CO3 + 2 H2O (1)
1 м 0,5 м карбонат калия (нормальная соль)
KOH + H2CO3 = KHCO3 + H2O (2)
1 м 1 м гидрокарбонат калия (гидросоль)
В реакции (2) используют избыток кислоты по сравнению с получением нормальной соли.
2. взаимодействие нормальной соли с кислотой:
MgCO3 + H2CO3 (CO2 + H2O) = Mg(HCO3)2
Данная реакция происходит, например, при взаимодействии подземных вод, насыщенных углекислым газом, с карбонатными породами, содержащими CaCO3 и MgCO3. Поскольку гидросоли растворимы лучше средних солей, воду, обогащенную катионами Ca2+ и Mg2+, называют жесткой. Такая вода при кипячении образует накипь, т.к. соли нестойчивых кислот легко разлагаются при нагревании:
Mg(HCO3)2 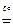 MgCO3¯ + H2O + CO2
MgCO3¯ + H2O + CO2
Мыло утрачивает свою моющую способность в такой воде из-за образования нерастворимых солей органических кислот:
C17H35COONa + Ca2+ = (C17H35COO)2Ca¯ + Na+
(К) (Mg2+) (Mg2+) (K+)
стеарат натрия (калия) - основа мыла
Небольшое содержание катионов кальция и магния в воде является полезным для человека, т.к. Ca2+ и Mg2+ являются важными компонентами живых организмов. При их малом присутствии в воде последнюю называют мягкой водой.
Гидросоли легко переходят в средние при действии оснований
(желательно использовать сильные хорошо растворимые основания), происходит реакция нейтрализации:
Ca(HSO4)2 + Ca(OH)2 = CaSO4 + H2O
2NaOH = Ca SO4 + Na2SO4 + H2O
Часто возникает вопрос, какие соли может образовать данная кислота. Рекомендуем сначала представить схему ступенчатой диссоциации кислоты (многоосновные кислоты при диссоциации последовательно отщепляют ионы H+), такая операция позволяет определить вид всех кислотных остатков и их заряд, например:
H2SO4 Û H+ + HSO4- (1 ступень)
НSО4- Û Н+ + SО42- (2 ступень)
При взаимодействии такой кислоты, например, с гидроксидом калия KOH, можно, используя ступенчатую диссоциацию кислоты и диссоциацию основания, проанализировать, какие соли возможны:
+ - + 2-
KOH + H2SO4 =?
OH- + K+ H+ + HSO4- гидросульфат - ион
H+ + SO42- сульфат – ион
В данном случае возможно образование двух солей: KHSO4 и K2SO4. Определив виды солей, следует записать уравнения реакций их образования при различном соотношении основания и кислоты:
KOH + H2SO4 = KHSO4 + H2O
гидросульфат калия
2 KOH + H2SO4 = K2SO4 + H2O
сульфат калия
Рассмотрим еще один пример:
+ - + 3-
NaOH + H3PO4 =?
OH- + Na+ H+ + H2PO4- [(2+) + (3-) =1-] *
H+ + HPO42- [(1+) + (3-)= 2-] *
H+ + PO43-
*Примечание: для определения заряда кислотных остатков, содержащих атомы водорода, рекомендуем в формуле кислоты указать заряд атома водорода (Н+) и кислотного остатка, в данном случае РО43-.
Запишем формулы возможных солей:
NaH2PO4 - дигидро(орто)фосфат Na
Na2HPO4 - гидро(орто)фосфат Na
Na3PO4 - ортофосфат Na
 2015-03-20
2015-03-20 1472
1472








