Электролиты – вещества, молекулы которых в растворах или расплавах подвергаются процессу диссоциации, т.е. распаду на ионы (К+ - катионы и А- - анионы):
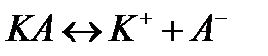 , (3.2)
, (3.2)
Процесс распада молекул электролита под действием полярных молекул воды (растворителя) называется электролитической диссоциацией (в дальнейшем просто диссоциацией).
С позиций теории электролитической диссоциации:
Кислота – соединение, при диссоциации которого образуется избыток катионов водорода (H+):
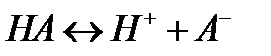 , (3.3)
, (3.3)
Основание – соеденение, при диссоциации которого образуется избыток анионов гидроксила (OH-):
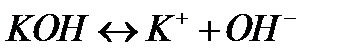 . (3.4)
. (3.4)
При диссоциации солей образуются катионы металлов (или катионы аммония NH4+) и анионы кислотных остатков.
Сила электролита определяется величиной степени диссоциации
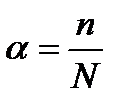 ,(3.5)
,(3.5)
где n – число молекул, распавшихся на ионы,
N – общее число молекул в растворе.
Для «идеально» сильных электролитов α=1 (100%), для неэлектролитов α=0.
Диссоциация – обратимый процесс.
Константа равновесия процесса диссоциации (3.1) называется константой диссоциации Kg:
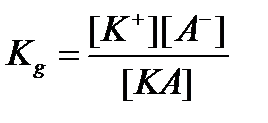 . (3.6)
. (3.6)
Чаще всего именно величина Kgявляется критерием силы электролита. ЗначенияKgприводятся в справочной литературе (таблицу П2).
Сильные электролиты. Признаками сильного электролита являются:
1. Степень диссоциации α близка к 1.
2. α практически не зависит от концентрации раствора.
3. Величины Kg> 1 (как правило >> 1).
Примеры сильных электролитов:
1. Все соли.
2. Некоторые кислоты: HCl, H2SO4, HNO3и др.
3. Сильные основания – щелочи: NaOH, KOH, Ca(OH)2и др.
Слабые электролиты. Признаками слабых электролитов являются:
1. Степень диссоциации может меняться в широких пределах 0<α<1.
2. α зависит от концентрации раствора.
Эта зависимость выражается законом разведения Оствальда:
Если C – концентрация раствора, а α – степень диссоциации электролита,
то уравнение (3.6) приобретает вид:
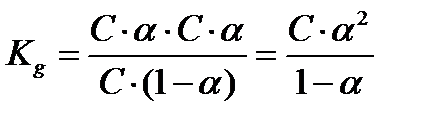 . (3.7)
. (3.7)
Для электролитов с α<<1 уравнение упрощается:
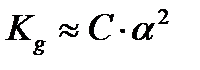 (3.8)
(3.8)
и
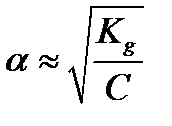 . (3.9)
. (3.9)
Из уравнения (3.9) видно, что величина α растет с уменьшением концентрации раствора, стремясь при бесконечно большом разбавлении к 1.
 2015-04-01
2015-04-01 1259
1259
