Электрохимия - наука о взаимных превращениях химической и электрической энергии. Преобразование химической энергии (или энергии химических реакций) в электрическую осуществляется в гальванических элементах (химических источниках тока). Преобразование энергии электрического тока в химическую энергию (химические превращения) называется электролизом.
Электрохимическая система содержит два электрода, ионный проводник (проводник II рода - раствор или расплав) и внешнюю электрическую цепь.
В электрохимической системе всегда происходят окислительно-восстановительные реакции (ОВР), т.е. реакции, сопровождающиеся изменением степени окисленности элементов.
Окисление - процесс повышения степени окисленности (отдачи электронов).
Восстановление - процесс понижения степени окисленности элемента (прием электронов).
Окислитель (Оx) - частица (атом, молекула или ион), понижающая степень окисленности (принимает электроны или восстанавливается).
Восстановитель (Red) - частица, повышающая степень окисленности (отдает электроны или окисляется). В случае сложного иона или молекулы (например, MnO4-,Н20, Н202 и т.д.) термин «степень окисленности» относится к одному из ионов, входящих в состав сложного.
Электродом называют проводник I рода (металл или полупроводник), погруженный в ионный проводник (электролит). На границе раздела за счет взаимодействия металла и электролита возникает так называемый двойной электрический слой и, следовательно, скачок потенциала. Это явление и обусловливает возникновение электродного потенциала, который в условиях устанавливающегося равновесия между металлом и электролитом называют равновесным электродным потенциалом.
Таким образом, любой электрод представляет собой окислительно-восстановительную (RedOx) систему - равновесие между окислителем (окисленной формой Ох) и восстановителем (восстановленной формой Red):
Ох + ne↔Red или сокращенно Ох| Red (5.1)
(знак | обозначает границу раздела между проводниками I и II рода).
В зависимости от того, что представляют собой окисленная и восстановленная формы, различают три типа электродов (табл. 2):
Таблица 2
| П/п | Тип электрона | Ох | Red | Пример | № |
| металлический | Men+ | Me | Zn2++2e↔ Zn Или Zn2+|Zn | (1) | |
| газовый | Одна из форм - газ | Cl2+2e↔2Cl-Cl2|Cl- 2H+ +2e ↔H2 2H+| H2 | (2) (3) | ||
| Окислительно-восстанови- тельный или RedOx | Ионы или молекулы (но не металлы или газы) | Fe3+ +e↔Fe2+ MnO4-+5e+8H+↔Mn2+ +4H2O | (4) (5) |
Абсолютные значения потенциалов электродов измерить невозможно. Поэтому на практике используют относительные значения, которые измеряют как разность потенциалов между данным электродом и электродом сравнения в составе гальванического элемента. Причем потенциал электрода сравнения считается известным. Тогда э.д.с. (Е) такого элемента равна потенциалу электрода относительно потенциала электрода сравнения. В качестве последнего принято использовать стандартный водородный электрод, в котором осуществляется равновесие:
2Н++2e↔Н2, Pt (газообразный водород адсорбируется на платине - инертном проводнике).
В стандартных условиях (Рн2=1ат, аH+=1 (рН=0)) потенциал такого электрода условно принят за нуль В. Если второй электрод находится в стандартных условиях, то его потенциал называют стандартным электродным потенциалом γ°. Значения стандартных потенциалов некоторых электродов приведены в приложении (П.2).
Для обозначения гальванического элемента принята следующая форма записи:
Red1|Ox1 || Ox2|Red2. (5.2)
┌──γлев──┐┌──γправ──┐
Здесь знак || обозначает границу раздела между проводниками II рода (электролитами). Принято записывать справа электрод с большим значением γ° (γправ>γлев) Например, элемент Даниэля- Якоби будет записан:
Zn|Zn2+||Cu2+|Cu. (5.3)
В разделе «Химическая термодинамика» было показано, что самопроизвольно протекают те реакции, которые сопровождаются убылью свободной энергии Гиббса (∆G<0). Изменение свободной энергии Гиббса равно максимальной работе (за вычетом работы расширения p-∆V), которую может совершить система в обратимом процессе. Работа, совершаемая гальваническим элементом, равна произведению э.д.с. на количество пропущенного электричества:
Amax=-∆G=-n∙F∙E, (5.4)
где η - число моль электронов, участвующих в электродных реакциях;
F - число Фарадея (F≈96500Кл∙моль-1).
Таким образом, если ∆G<0, то Е>0, то есть, если э.д.с. обратимого гальванического элемента положительна, то реакция происходит самопроизвольно. Это условие является критерием самопроизвольного протекания окислительно-восстановительных реакций.
Условимся называть окислительно-восстановительную систему с большим потенциалом окислителем, с меньшим - восстановителем, а соответствующие им потенциалы γокиγвосст.. Тогда э.д.с. самопроизвольно протекающей ОВР
Е=γок.-γвосст. (5.5)
Чем более положительное значение имеет Е, тем более отрицательно ∆G и, следовательно, тем более вероятно протекание данной реакции. Отсюда также следует, что «сила» окислителя тем больше, чем более положительным значением потенциала характеризуется соответствующая Red|Ox система. И наоборот, «сила» восстановителя тем больше, чем более отрицательное значение потенциала имеет соответствующая Red|Оx система.
Значения стандартных потенциалов определяется природой электродов. Используя уравненияи (5.4),легко получить выражения для Е и потенциалов электродов в условиях, отличных от стандартных:
E=E0- 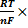 Ln(accadD…/aAaabB…) (5.6)
Ln(accadD…/aAaabB…) (5.6)
и
γ=γ0- 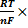 Ln(accadD…/aAaabB…). (5.7)
Ln(accadD…/aAaabB…). (5.7)
Эти соотношения носят название уравнений Нернста. Для потенциалов металлических и Red | Ox электродов уравнения Нернста приобретают вид:
γ(Men+|Me)=γ0 (Men+|Me)+ 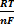 Ln(a (Men+) ) (5.8)
Ln(a (Men+) ) (5.8)
γOx|Red= γ0Ox|Red + 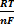 Ln(aOx/aRed), (5.9)
Ln(aOx/aRed), (5.9)
где аMen+, aOx,aRed - активности ионов металла, окисленной и восстановленной форм в растворе соответственно. Например, для Red|Ox системы (5) из табл. 2 уравнение (5.9) имеет вид:
γMnO4-,H+|Mn2+ = γ0MnO4-,H+|Mn2+ + 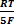 Ln(aMnO4-/aMn2+) × a8H+ (5.10)
Ln(aMnO4-/aMn2+) × a8H+ (5.10)
Активность Н20 по определению равна 1. В случае разбавленных растворов активности могут быть заменены соответствующими молярными концентрациями.
 2015-04-01
2015-04-01 425
425








