Водородная связь образуется между положительно поляризованным атомом водорода одной молекулы и отрицательно поляризованным атомом (О, F, N, реже S, Сl и др.) другой молекулы. Водородная связь может быть как межмолекулярной, так и внутримолекулярной. Водородная связь обозначается пунктирной линией. Энергия водородной связи невелика, 17–26 кДж/моль, но тем не менее эта связь играет очень важную роль, особенно в биохимии.
Понятие о водородной связи было введено Верналом и Фаулером для объяснения сил, связывающих молекулы в жидкой воде. Предполагалось, что ионы водорода (протоны) молекулы воды взаимодействуют с неподеленной парой электронов кислорода другой молекулы воды так, что получается система:
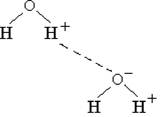 |
При этом за счет оттягивания атома водорода одной молекулы атомом кислорода другой молекулы длина связи О–Н увеличивается. Объем молекулы Н2О тоже увеличивается, а плотность твердой воды (льда) уменьшается. Поэтому благодаря наличию водородной связи лед не тонет в воде, а плавает по её поверхности.
Несмотря на малую прочность водородной связи, она определяет иногда структуру вещества и существенно влияет на его химические и физические свойства. Благодаря водородным связям молекулы объединяются в ди-меры, полимеры, циклы и более сложные ассоциаты. Водородная связь обладает свойствами ненаправленности и ненасыщаемости.
Многие физические свойства веществ с водородной связью (Н2О, НF) отличаются от общего хода изменения их в ряду аналогов. Так, летучесть ассоциированных жидкостей мала, а вязкость, теплота парообразования, температура кипения (табл. 3.2) аномально высоки.
Таблица 3.2
Температура кипения гидридов элементов VI и VII группы
| Вещество | Ткип, °С | Вещество | Ткип, °С |
| НС1 | -114,2 | H2S | -60,35 |
| HBr | -86,9 | H2Se | -41,4 |
| HJ | -50,8 | H2Te | -2,0 |
| HF | +20,0 | н 2 о | +100,0 |
Водородная связь очень распространена и встречается повсеместно – в воде, белках, полимерах, живых организмах и т. д. Такая ее универсальность
 2015-04-01
2015-04-01 991
991








