Порядок исследования термодинамических процессов.
1. Записывается уравнение процесса в P-V координатах.
2. Выводятся соотношения между параметрами состояния рабочего тела.
3. Определяются изменения внутренней энергии, энтальпии и энтропии.
4. Вычисляется работа деформации газа в процессе.
5. Вычисляется количество теплоты, участвующей в процессе.
6. Процесс изображается на pV диаграммах.
Обратимый изобарный процесс идеального газа.
1. При изобарном процессе давление остается постоянным: p=const
Для проведения обратимого процесса требуется множество источников теплоты разной температуры.
2. Из уравнения состояния идеального газа 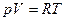 при p=const находим:
при p=const находим: 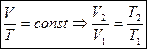 , (1.50)
, (1.50)
Выражение (1.50) называется законом Гей-Люссака и показывает, что в изобарном процессе объем газа меняется прямо пропорционально температуре.
3. Изменение удельной внутренней энергии определяется одинаково для всех процессов, так как 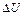 является параметром состояния рабочего тела:
является параметром состояния рабочего тела: 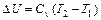 (1.51)
(1.51)
Изменение энтальпии определяется выражением:
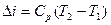 (1.52)
(1.52)
Изменение энтропии в изобарном процессе определяется из формулы (1.49):
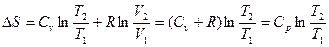 (1.53)
(1.53)
4. Удельная работа расширения или сжатия газа:
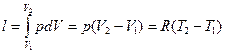 (1.54)
(1.54)
Для M кг газа:
L = M·p(V2-V1)= MR(T2 –T1) (1.55)
5.Определим удельное количество теплоты участвующее в процессе:
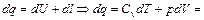
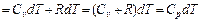
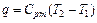 (1.56)
(1.56)
Полная теплота процесса: 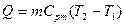 (1.57)
(1.57)
6. Графически изобарный процесс в PV координатах изображается горизонтальной прямой (рис. 1.4): линия 1 – 2: изобарное расширение рабочего тела (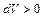 ), температура в процессе увеличивается, теплота подводится dq > 0, совершается положительная работа
), температура в процессе увеличивается, теплота подводится dq > 0, совершается положительная работа 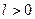 .Линия 1-2
.Линия 1-2  : изобарное сжатие (
: изобарное сжатие (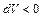 ), здесь температура уменьшается, тепло отводится
), здесь температура уменьшается, тепло отводится 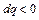 , над системой совершается работа
, над системой совершается работа 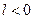 .
.
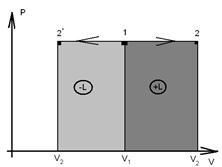
Рис. 1.4 - Процесс изменения состояния идеального газа в изобарном процессе.
 2015-04-01
2015-04-01 1031
1031








