Температура кипения растворов нелетучего вещества всегда выше, чем температура кипения чистого растворителя при том же давлении. Рассмотрим р – T диаграмму состояния растворителя (воды) и ее растворов различной концентрации (Рис.18). Любая жидкость (растворитель или раствор) кипит при той температуре, при которой давление насыщенного пара становится равным внешнему давлению. Соответственно температуры, при которых изобара р = 1 атм пересекает кривые ОА, ВС и DE, представляющие собой зависимости давления пара над чистым растворителем и растворами с возрастающими концентрациями соответственно, будут температурами начала кипения этих растворов (Рис. 18).
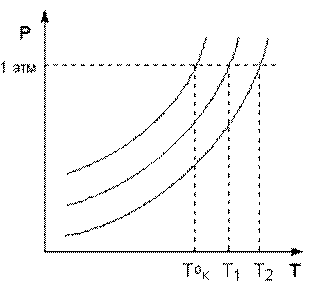
Рис. 18. Повышение температуры кипения разбавленных растворов
Введем определение повышения температуры начала кипения растворов нелетучих веществ:
ΔTк = Tк – T0к
Величина ΔTк пропорциональна понижению давления насыщенного пара и, следовательно, прямо пропорциональна моляльной концентрации раствора mB. Коэффициент пропорциональности EА есть эбулиоскопическая постоянная растворителя, не зависящая от природы растворенного вещества.
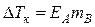 (56)
(56)
 2015-04-01
2015-04-01 471
471








