Способы получения металлов из руд.
1. Электрометаллургический способ - э то способы получения металлов с помощью электрического тока (электролиза). Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы.
При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов:
NaCl (расплав) D Na+ + Cl-
катод Na+ + e à Na0 ¦ 2
анод 2Cl- - 2e à Cl20 ¦ 1
суммарное уравнение: 2NaCl (распл.) – (э.ток)à 2Na + Cl2
Современный способ получения алюминия был изобретен в 1886 году. Он заключается в электролизе раствора оксида алюминия в расплавленном криолите. Расплавленный криолит растворяет Al2O3, как вода растворяет сахар.
Al2O3 (расплав) D Al3+ + AlO33–
катод Al3+ +3e à Al 0 ¦ 4
анод 4AlO33– –12 e à 2Al2O3 +3O2 ¦ 1
суммарное уравнение: 2Al2O3(распл.) – (э.ток)à 4Al + 3O2.
2. Пирометаллургический способ - это восстановление металлов из их руд при высоких температурах с помощью восстановителей: неметаллических: кокс, оксид углерода (II), водород; металлических: алюминий, магний, кальций.
| Алюмотермия: Fe+32O3 +2Al = 2Fe0 + Al2O3 | Получают железо, хром. |
| Восстановление оксидов металлов водородом (водородотермия): Cu +2O + H2 –(t)à Cu0 + H2O | Получают малоактивные металлы – медь, вольфрам. |
| Получение чугуна: В вертикальной печи кокс окисляется до СО, затем происходит постепенное восстановление железа из руды: | 3Fe2O3 + CO –(t)à 2Fe3O4 + CO2, Fe3O4 + 4CO –(t)à 3FeО + 4CO2 FeO + CO –(t)à Fe+ CO2 |
| Восстановление углём (коксом): ZnO + C –(t)à Zn + CO | Получают цинк, никель. |
3. Гидрометаллургический способ основан на растворении природного соединения с целью получения раствора соли этого металла и вытеснением данного металла более активным. Например, руда содержит оксид меди и ее растворяют в серной кислоте: CuO + H2SO4 = CuSO4 + H2O, затем проводят реакцию замещения:
CuSO4 + Fe = FeSO4 + Cu.
Таким способом получают серебро, цинк, молибден, золото, ванадий.
Если для восстановления требуется оксид металла, то в процессе переработки сначала получают оксид:
а) из сульфида – обжигом в кислороде: 2ZnS + 3O2 = 2ZnO + 2SO2
б) из карбоната – разложением: СаСО3 – (t)à СаО + СО2
Чугун и сталь.
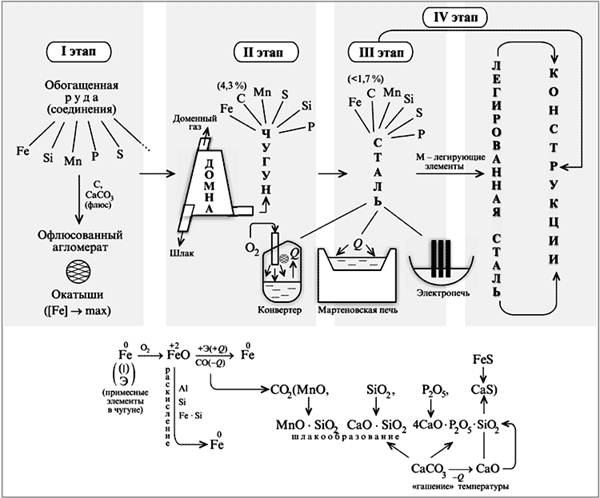
Производство железа основано на карботермическом восстановлении оксидных металлсодержащих руд.
1) Сульфидные и другие руды вначале подвергают окислительному обжигу: 4FeS2 + 11O2 = 2Fe2O3 + 8SO2.
2)Восстановление оксидных руд осуществляется в доменных печах, при этом протекают следующие реакции:
3Fe2O3 + CO – (t)àCO2 + 2Fe3O4,
Fe3O4 + CO – (t)àCO2 + 3FeO,
FeO + CO – (t)àCO2 + Fe
или FeO + C – (t)àCO + Fe.
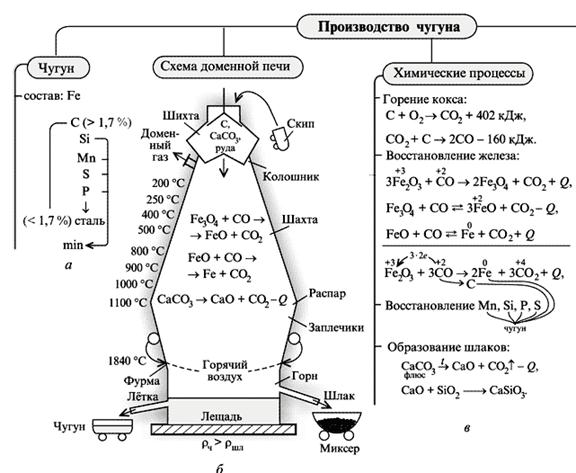
Полученное железо насыщено углеродом.
3)Затем происходит «выжигание» углерода в сталеплавильных или конверторных печах с образованием стали.
 2015-04-06
2015-04-06 371
371






