Пусть m0(L) - масса образца вещества L, имеющего химическую формулу АxByCz
I. Расчет молярной массы вещества M(L) и его количества nо(L):
M(L) = x× M(A) + y× M(B) + z× M(C), где M(A), M(B), M(C) – молярные массы химических элементов A, B, C иnо(L)= 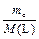
II. Расчет количества элементов A, B, C в образце вещества L:
n 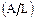 = x× nо(L), n
= x× nо(L), n 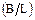 = y× nо(L) и n
= y× nо(L) и n 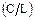 = z× nо(L)
= z× nо(L)
III. Расчет массы элементов A, B, C в образце вещества L:
m 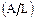 = M(A) · n
= M(A) · n 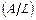 = M(A) · x× nо(L) и аналогично
= M(A) · x× nо(L) и аналогично
m 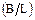 = M(B) · y× nо(L), m
= M(B) · y× nо(L), m 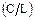 = M(C) · z× nо(L),
= M(C) · z× nо(L),
причем должно выполняться очевидное равенство – сумма масс элементов, входящих в состав вещества L, равна массе его образца m0 (L): m 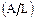 + m
+ m 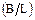 + m
+ m 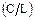 = m0 (L).
= m0 (L).
IV. Удобными вспомогательными величинами являются массовые доли химических элементов w, представляющие собой отношение массы каждого из элементов к массе вещества L, числовые значения которых лежат в интервале 0<w<1. Эти безразмерные характеристики рассчитывают по формулам:
w(А/L)= 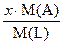 , w(A/L)% = w(A/L)×100%;
, w(A/L)% = w(A/L)×100%;
w(В/L) = 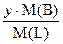 , w(B/L)% = w(B/L)×100%;
, w(B/L)% = w(B/L)×100%;
w(С/L) = 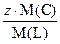 , w(C/L)% = w(C/L)×100%,
, w(C/L)% = w(C/L)×100%,
между которыми существует очевидная связь
w 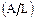 + w
+ w 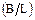 + w
+ w 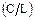 = 1 или 100%.
= 1 или 100%.
Знание массовых долей позволяет рассчитать массы элементов в образце вещества, если его масса равна m0:
m(A/L) = mо×w 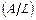 ; m(B/L) = mо×w
; m(B/L) = mо×w 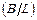 ;
;
m(C/L) = mо ×w 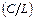 .
.
V. Индексы в химической формуле вещества задают отношение количеств элементов А, В и С в образце вещества АхByCz произвольной массы:
x: y: z = n(A/L): n(B/ L): n(C/L).
Можно легко получить другие формы записи последнего соотношения, если провести замены в правой части:
а) поскольку n(A/L) = 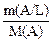 и т.д., то
и т.д., то
x: y: z = 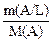 :
: 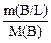 :
: 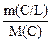
б) согласно пункту IV: m(A/L) = m0×w(А/L) и т.д., что при подстановке в предыдущее соотношение дает
x: y: z = 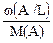 :
: 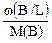 :
: 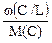 ,
,
где в правой части проведено сокращение на общий множитель m0. В практических расчетах величины массовых долей элементов удобно брать в процентах.
VI. Условие электронейтральности гетероядерной молекулы АхByCz имеет вид 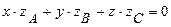 ,
,
где 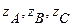 – степени окисления элементов в молекуле. Данное уравнение можно переписать в другом виде по аналогии с пунктом V
– степени окисления элементов в молекуле. Данное уравнение можно переписать в другом виде по аналогии с пунктом V
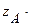 n(A/L) +
n(A/L) + 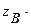 n(B/ L) +
n(B/ L) + 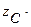 n(C/L) = 0.
n(C/L) = 0.
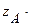
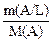 +
+ 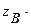
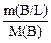 +
+ 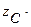
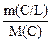 = 0
= 0
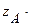
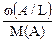 +
+ 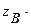
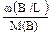 +
+ 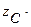
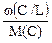 = 0,
= 0,
где в последнем уравнении массовые доли элементов удобно брать в процентах.
Соотношения пункта V используют для определения индексов в химических формулах сложных веществ по результатам их элементного химического анализа. В эксперименте обычно определяют качественный состав вещества и массы или массовые доли химических элементов в его пробе. На основе этих данных рассчитывают правую часть приведенных выше соотношений. Как правило, получают отношение дробных чисел. Эти числа следует разделить на наименьшее из них, а затем умножить на одно и то же целое число, добиваясь ситуации, чтобы произведения стали практически целыми числами. Последние являются индексами в простейшей химической формуле вещества.
Пример 1. Э лементный химический анализ пробы вещества L дал результат n(A): n(B): n(C) = 1,50: 0,75: 2,63. Определите простейшую формулу вещества.
n(A): n(B): n(C) = 1,50: 0,75: 2,63 = (разделим каждое из чисел на наименьшее из них) = 2: 1: 3,5 = (умножим найденные числа на два) = 4:2:7 и простейшая формула вещества L имеет вид А4В2С7.
Простейшая формула не обязательно является истинной химической формулой вещества, поскольку по результатам анализа можно определить лишь отношение индексов, а не их абсолютные значения. Последнее утверждение вытекает из очевидного равенства
x: y: z = n×x: n×y: n×z,
где n – любой множитель, а в нашем случае – это целое число. Для нахождения истинных индексов необходимо определить величину “ n ” по известной из условия задачи или опыта молярной массе вещества. В частном случае, когда n = 1 простейшая формула совпадает с истинной формулой вещества.
Расчет “ n ” проводят по следующей схеме:
Простейшая формула вещества Истинная формула вещества
AxByCz AnxBnyCnz
¯ ¯
Молярная масса Молярная масса
М(AxByCz) М(AnxBnyCnz)
n = 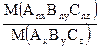
Например, простейшая формула глюкозы имеет вид СН2О, а истинная – С6Н12О6 , где n(С): n(Н): n(О) = 6:12:6 = 1: 2: 1. Между молярными массами существует связь (n = 6):
М (С6Н12О6) = 6 × М (СН2О).
Пример 2. Определите массовые доли натриевых солей двухосновной неорганической кислоты в водном растворе, в котором на 5 атомов серы приходится 7 атомов натрия, 185 атомов кислорода и 333 атома водорода (других атомов нет).
(Олимпиада по химии 2001 г., РХТУ им. Д.И. Менделеева)
В средних солях простейших двухосновных серосодержащих кислот на каждый атом серы приходится два атома натрия, поэтому приведенное в условии задачи соотношение между их числом свидетельствует о том, что в растворе присутствует смесь кислой и средней солей.
Обозначим качественный состав трехкомпонентного раствора – Na2SOx, NaHSOx, H2O, где х = 0 соответствует солям сероводородной, х = 3 – сернистой, х = 4 – серной кислотам.
Пусть раствор состоит из а моль Na2SOx, в моль NaHSOx и с моль Н2О, в котором имеет место следующее соотношение между количествами атомов
n(S): n(Na): n(O): n(H) = 5: 7: 185: 333.
Согласно правилам расчета по химическим формулам
(пункт II), можно записать: 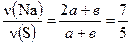 ,
,
откуда находим в = 1,5 а;
из 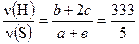 , с учетом предыдущего результата получаем с = 82,5 а;
, с учетом предыдущего результата получаем с = 82,5 а;
из 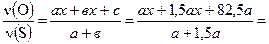
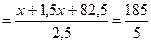 следует х = 4.
следует х = 4.
Таким образом, в растворе присутствуют гидросульфат и сульфат натрия. Масса раствора равна
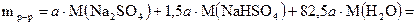
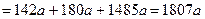 ,
,
а массовые доли солей составляют
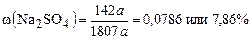
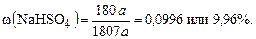
Пример 3. Электронные конфигурации атомов трех элементов X, Y, Z имеют окончания...4s1;... 4s13d5;...2p4 соответственно. Они образуют сложное соединение, в молекуле которого число атомов X равно числу атомов Y; молярная масса вещества равна 294 г/моль, а общее число электронов в молекуле 142. Определите химическую формулу вещества.
Окончания электронных конфигураций соответствуют элементам:...4s1 – K;...4s13d5 – Cr;...2p4 – O
Обозначим через m, n, k индексы элементов в химической формуле сложного вещества K m Cr n O k и составим уравнения для их определения:
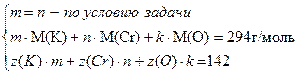 ,
,
где М(...) – молярные массы элементов; z (...) – порядковые номера элементов соответствующие числу электронов в атомах. Последнее уравнение представляет собой условие электронейтральности молекулы – сумма зарядов всех ядер равна общему количеству электронов в молекуле. Подставляя числовые значения и решая систему уравнений: 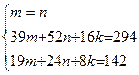 , находим
, находим 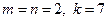 .
.
Итак, химическая формула искомого вещества К2Cr2O7 – бихромат калия.
 2015-04-30
2015-04-30 1635
1635
