Универсальным восстановителем оксидов железа является твёрдый углерод; при восстановлении газообразными часто применяют СО и Н2.
Термодинамика процессов восстановления оксидов железа твёрдыми и газообразными восстановителями в принципе одинакова.
При использовании окиси углерода СО следует рассматривать равновесия в системе FemOn– CO – CO2, которые описываются следующими реакциями:
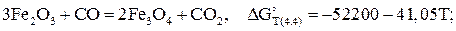 (4.4)
(4.4)
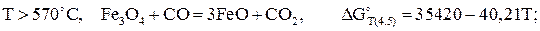 (4.5)
(4.5)
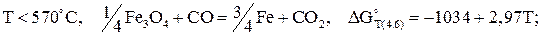 (4.6)
(4.6)
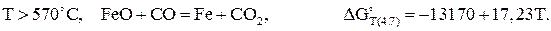 (4.7)
(4.7)
Равновесные составы газа, соответствующие реакциям (4.4)–(4.7), приведены на рис. 4.1.
Указанные на рис. 4.1 кривые равновесных составов рассчитываются при решении системы, состоящей из двух уравнений:
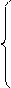
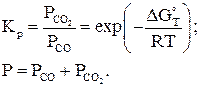 (4.8)
(4.8)
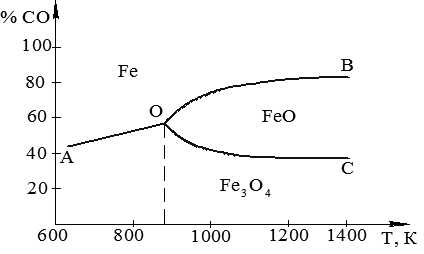
Рис. 4.1. Равновесный состав газовой фазы системы FemOn – CO – CO2
На диаграмме отсутствует зона стабильного существования фазы Fe2O3, поскольку, согласно расчётам, данная фаза является в рассматриваемом интервале температур неустойчивой уже при содержании СО > 0,01%.
Точка О является точкой нонвариантного равновесия с газовой фазой трёх твёрдых фаз.
При использовании в качестве восстановителя водорода либо какого-нибудь иного восстановителя кривые равновесного состава газа будут рассчитываться аналогично.
При использовании в качестве восстановителя оксидов железа углерода процесс можно описать реакциями, отвечающими равновесию в системе
Fe2O3 – Fe3O4 – FeO – Fe – C – CO – CO2, содержащей семь компонентов.
Однако с учётом нестабильности Fe2O3, целесообразно проанализировать следующие химические равновесия:
Fe3O4 + CO = 3FeO + CO2;
FeO + CO = Fe + CO2;
2CO = C + CO2.
Кроме частных равновесий, в соответствии с правилом фаз возможно одновременное равновесие пяти фаз – четырёх твёрдых и газообразной (смеси СО и СО2).
Кривые равновесия указанных реакций приведены на рис. 4.2.
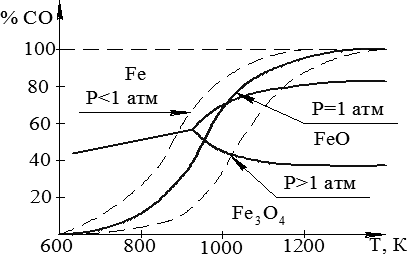
Рис. 4.1. Равновесные содержания моноксида
углерода при косвенном восстановлении оксидов
железа и реакции газификации твёрдого углерода
Количественные характеристики равновесий в рассматриваемой системе можно получить, решив совместно уравнения, выражающие зависимость констант от состава газовой фазы. Из решения системы этих уравнений следует, что с увеличением давления в системе температуры начала восстановления оксидов железа возрастают, а с понижением давления – наоборот.
Таким образом, фазовые равновесия в системе Fe–O в присутствии твёрдого углерода определяются температурой и общим давлением газовой фазы
(СО + СО2).
 2015-05-05
2015-05-05 627
627








