Кроме упомянутого лекарственного средства «Аскорбиновая кислота» производится также биологически активная добавка под названием «Аскорбинка». В состав этой добавки входит аскорбиновая кислота, но технология её производства и безопасность (прохождение клинических испытаний и пр.) не относится к категории «лекарственное средство».
[править]Источники витамина С
Наиболее богаты аскорбиновой кислотой плоды барбадосской вишни (1000-3300 мг/100 г), свежего шиповника (650 мг/100 г), болгарского красного перца (250 мг/100 г), чёрной смородины и облепихи (200 мг/100 г), яблоки (содержат 165 мг/100 г), перец зелёный сладкий и петрушка (150 мг/100 г), брюссельская капуста (120 мг/100 г), укроп и черемша (колба) (100 мг/100 г), земляника садовая (60 мг/100 г), цитрусовые (38-60 мг/100 г)[11], недозрелые плоды грецкого ореха, хвоя сосны и пихты[1
24Нуклеиновые кислоты. Состав, структура и роль в биосинтезе белков.
В обмене веществ организма ведущая роль принадлежит белкам и нуклеиновым кислотам. Белковые вещества составляют основу всех жизненно важных структур клетки, они входят в состав цитоплазмы. Белки обладают необычайно высокой реакционной способностью. Они наделены каталитическими функциями, т. е. являются ферментами, поэтому белки опреде ляют направление, скорость и теснейшую согласованность, сопряженность всех реакций обмена веществ.
Ведущая роль белков в явлениях жизни связана с богатством и разнообразием их химических функций, с исключительной способностью к различным превращениям и взаимодействиям с другими простыми и сложными веществами, входящими в состав цитоплазмы.
Нуклеиновые кислоты входят в состав важнейшего органа клетки — ядра, а также цитоплазмы, рибосом, митохондрий и т. д. Нуклеиновые кислоты играют важную, первостепенную роль в наследственности, изменчивости организма, в синтезе белка.
Процесс синтеза белка является очень сложным многоступенчатым процессом. Совершается он в специальных органеллах — рибосомах. В клетке содержится большое количество рибосом. Например, у кишечной палочки их около 20 000.
Каким образом происходит синтез белка в рибосомах?
Молекулы белков по существу представляют собой полипептидные цепочки, составленные из отдельных аминокислот. Но аминокислоты недостаточно активны, чтобы соединиться между собой самостоятельно. Поэтому, прежде чем соединиться друг с другом и образовать молекулу белка, аминокислоты должны активироваться. Эта активация происходит под действием особых ферментов. Причем каждая аминокислота имеет свой, специфически настроенный на нее фермент.
Источником энергии для этого (как и для многих процессов в клетке) служит аденозинтрифосфат (АТФ).
В результате активирования аминокислота становится более лабильной и под действием того же фермента связывается с т-РНК.
Важным является то, что каждой аминокислоте соответствует строго специфическая т-РНК. Она находит «свою» аминокислоту и переносит ее в рибосому. Поэтому такая РНК и получила название транспортной.
Следовательно, в рибосому поступают различные активированные аминокислоты, соединенные со своими т-РНК. Рибосома представляет собой как бы конвейер для сборки цепочки белка из поступающих в него различных аминокислот (рис. 13 А и Б).
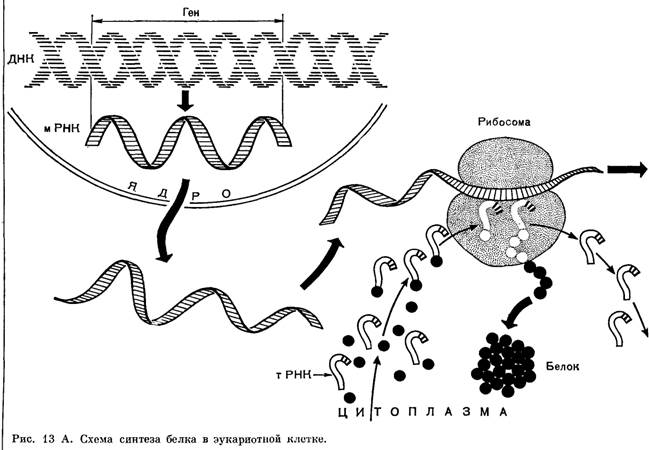
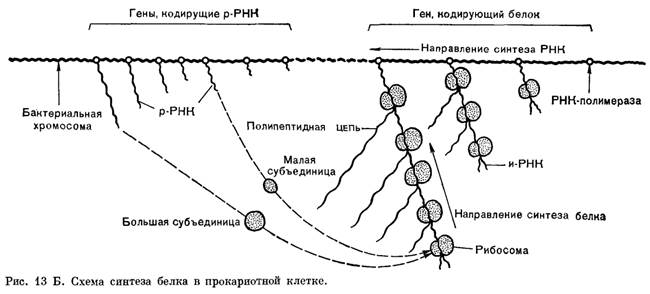
, 
Возникает вопрос: от чего зависит порядок связывания между собой отдельных аминокислот? Ведь именно этот порядок и определяет, какой белок будет синтезирован в рибосоме, так как от порядка расположения аминокислот в белке зависит его специфика. В клетке содержится более 2000 различных по строению и свойствам специфических белков.
Оказывается, что одновременно с т-РНК, на которой «сидит» своя аминокислота, в рибосому поступает «сигнал» от ДНК, которая содержится в ядре. В соответствии с этим сигналом в рибосоме синтезируется тот или иной белок, тот или иной фермент (так как ферменты являются белками).
Направляющее влияние ДНК на синтез белка осуществляется не непосредственно, а с помощью особого посредника, той формы РНК, которая получила название матричной или информационной РНК (м-РНК или и-РНК).
Информационная РНК синтезируется в ядре иод влиянием ДНК, поэтому ее состав отражает состав ДНК. Молекула РНК представляет собой как бы слепок с формы ДНК.
Синтезированная и-РНК поступает в рибосому и как бы передает этой структуре план — в каком порядке должны соединяться друг с другом поступившие в рибосому активированные аминокислоты, чтобы синтезировался определенный белок. Иначе, генетическая информация, закодированная в ДНК, передается на и-РНК и далее на белок.
Молекула информационной РНК поступает в рибосому и как бы прошивает ее. Тот ее отрезок, который находится в данный момент в рибосоме, определенный кодоном (триплет), взаимодействует совершенно специфично с подходящим к нему по строению триплетом (антикодоном) в транспортной РНК, которая принесла в рибосому аминокислоту. Транспортная РНК со своей аминокислотой подходит к определенному кодону и-РНК и соединяется с ним; к следующему, соседнему участку и-РНК присоединяется другая т-РНК с другой аминокислотой и так далее, до тех пор пока не будет считана вся цепочка и-РНК и пока не нанижутся все аминокислоты в соответствующем порядке, образуя молекулу белка. А т-РНК, которая доставила аминокислоту к определенному участку полипептидной цепи, освобождается от своей аминокислоты и выходит иэ рибосомы. Затем снова в цитоплазме к ней может присоединиться нужная аминокислота, и она снова перенесет ее в рибосому. В процессе синтеза белка участвует одновременно не одна, а несколько рибосом — полирибосомы.
Основные этапы передачи генетической информации: синтез на ДНК как на матрице и-РНК (транскрипция) и синтез в рибосомах полипептидной цепи по программе, содержащейся в и-РНК (трансляция), универсальны для всех живых существ. Однако временные и пространственные взаимоотношения этих процессов различаются у про- и эукариотов.
У организмов, обладающих па стоящим ядром (животные, растения), транскрипция и трансля ция строго разделены в пространстве и времепи: синтез различных РНК происходит в ядре, после чего молекулы РНК должны покинуть пределы ядра, пройдя через ядерную мембрану (рис. 13 А). Затем в цитоплазме РНК транспортируются к месту синтеза белка— рибосомам. Лишь после этого паступает следующий этап — трансляция.
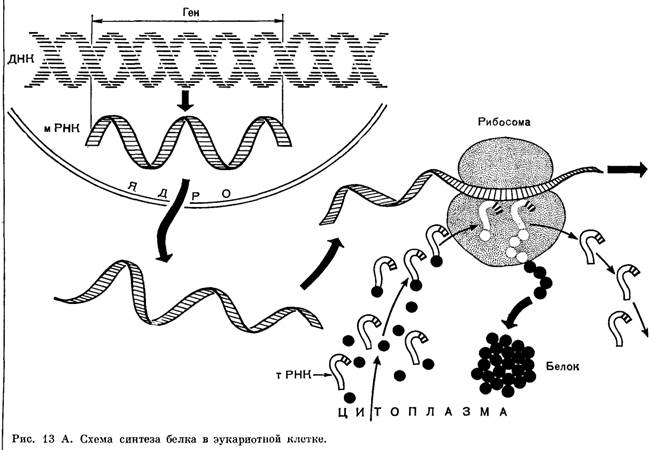
У бактерий, ядерное вещество которых не отделено от цитоплазмы мембраной, транскрипция и трансляция идут одновременно (рис. 13 Б).

Современные схемы, иллюстрирующие работу генов, построены на основании логического анализа экспериментальных данных, полученных с помощью биохимических и генетических методов. Применение тонких электронно-микроскопических методов позволяет в буквальном смысле слова увидеть работу наследственного аппарата клетки. В последнее время получены электронно-микроскопические снимки, на которых видно, как на матрице бактериальной ДНК, в тех участках, где к ДНК прикреплены молекулы РНК-полимеразы (фермента, катализирующего транскрипцию ДНК в РНК), происходит синтез молекул и-РНК. Нити и-РНК, расположенные перпендикулярно к линейной молекуле ДНК, продвигаются вдоль матрицы и увеличиваются в длине. По мере удлинения нитей РНК к ним присоединяются рибосомы, которые, продвигаясь, в свою очередь, вдоль нити РНК по направлению к ДНК, ведут синтез белка.
Из всего сказанного следует, что местом синтеза белков и всех ферментов в клетке являются рибосомы. Образно выражаясь, это как бы «фабрики» белка, как бы сборочный цех, куда поступают все материалы, необходимые для сборки полипептидной цепочки белка иэ аминокислот. Природа же синтезируемого белка зависит от строения и-РНК, от порядка расположения в ней нуклеоидов, а строение и-РНК отражает строение ДНК, так что в конечном итоге специфическое строение белка, т. е. порядок расположения в нем различных аминокислот, зависит от порядка расположения нуклеоидов в ДНК, от строения ДНК.
Изложенная теория биосинтеза белка получила название матричной теории. Матричной эта теория называется потому, что нуклеиновые кислоты играют как бы роль матриц, в которых записана вся информация относительно последовательности аминокислотных остатков в молекуле белка.
Создание матричной теории биосинтеза белка и расшифровка аминокислотного кода является крупнейшим научным достижением XX века, важнейшим шагом на пути к выяснению молекулярного механизма наследственности.
29Пентозофосфатный цикл.
ПЕНТОЗОФОСФАТНЫЙ ЦИКЛ (пентозный путь, гексо-зомонофосфатный шунт, фосфоглюконатный путь), совокупность обратимых ферментативных р-ций, в результате к-рых происходит окисление глюкозы до CO2 с образованием восстановленного никотинамидадениндинуклеотид-фосфата (НАДФН) и H +, а также синтез фосфорилир. Сахаров, содержащих от 3 до 7 атомов С.
Пентозофосфатный цикл осуществляется в цитозоле (жидкой фазе) клеток животных, растений (особенно в темноте) и микроорганизмов. У растений часть р-ций пентозофосфатного цикла участвует также в образовании гексоз при фотосинтезе.
Первая (окислит.) стадия пентозофосфатного цикла (р-ции 1-3, см. схему) осуществляется с образованием НАДФН (осуществляет восстановлениесубстратов в организме) и рибулозо-5-фос-фата, к-рый затем превращ. в рибозо-5-фосфат (все сахара находятся в D-форме), входящий в составмолекул ряда важнейших прир. соед. (нуклеиновых к-т, нуклеотидов и др.). На неокислит. стадии пентозофосфатного цикла (остальные р-ции) в результате взаимопревращения Сахаров образуются промежут. продукты гликолиза (фруктозо-6-фосфат, глицеральдегид-3-фосфат) и таким образом осуществляется обратимая связь пентозофосфатного цикла с гликолитич. путем метаболизма глюкозы.
В отличие от др. осн. путей метаболизма углеводов (гликолиза, трикарбоновых кислот цикла)функционирование пентозофосфатного цикла нельзя представить в виде линейной последовательности р-ций, приводящей непосредственно от 1 молекулы глюкозо-6-фосфата к 6 молекулам CO2. Пентозофосфатный цикл характеризуется возможностью многообразных взаимопревращений его метаболитов, происходящих по неск. альтернативным путям. Р-ции отдельных стадий пентозофосфатного цикла (их стехиометрия) и суммарная р-ция цикла приведены в таблице.
Важная особенность пентозофосфатного цикла (в сравнении с др. путями метаболизма углеводов)-его гибкость. Если потребность в рибозо-5-фосфате значительно превышает потребность в НАДФН, то б.ч. глюкозо-6-фосфата по гликолитич. пути превращ. в глицеральдегид-3-фосфат, 1молекула к-рого, вступая в р-ции с 2 молекулами фруктозо-6-фосфата, превращ. в 3 молекулы рибозо-5-фосфата (обращение р-ций 6-8).
В случаях, когда потребность в НАДФН и рибозо-5-фосфате сбалансирована, преобладающими становятся р-ции окислит, стадии пентозофосфатного цикла и р-ция 4. Суммарное ур-ние такого процесса:
Глюкозо-6-фосфат + 2 НАДФ + H2O 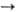 ри-бозо-5-фосфат + 2 НАДФН + 2 H+ + CO2
ри-бозо-5-фосфат + 2 НАДФН + 2 H+ + CO2
Если потребность в НАДФН значительно превышает потребность в рибозо-5-фос-фате, происходит полное окисление глю-козо-6-фосфата до CO2, включающее окислит, стадию пентозофосфатного цикла и ресинтез глюкозо-6-фос-фата из фруктозо-6-фосфата по пути глю-конеогенеза (р-ции 1-4, 6, 10-12). В этом случае суммарное ур-ние р-ции:
Глюкозо-6-фосфат + 12 НАДФ + 7 H2O 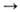 6CO2 + 12 НАДФН + 12 H+ + H3PO4
6CO2 + 12 НАДФН + 12 H+ + H3PO4
В условиях, когда потребность в НАДФН значительно превышает потребность в рибозо-5-фосфате, возможна реализация др. механизма, в соответствии с к-рым образующийся рибозо-5-фосфат превращ. не в глюкозо-6-фосфат, а в пиро-виноградную к-ту (пируват) в результате гликолизафруктозо-6-фосфата и глице-ральдегид-3-фосфата, образующихся в р-циях 6-8. При этом образуются НАДФН, НАДН (восстановленная форма никотинамидадениндинуклеотида) и АТФ по суммарному ур-нию:
3 глюкозо-6-фосфат + 6 НАДФ + 5 НАД + + 5 H3PO4 + 8 АДФ 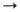 5 пируват + 3 CO2 + + НАДФН + 5 НАДН + 8 АТФ + 2 H2O + 8H +
5 пируват + 3 CO2 + + НАДФН + 5 НАДН + 8 АТФ + 2 H2O + 8H +
HАД - окисленная форма НАДН, АДФ-аденозиндифосфат Образующаяся пировиноградная к-та может далее претерпевать превращ. в цикле трикарбоновых к-т (при этом образуется АТФ) в др. р-циях в обмене в-в.
Регуляция направленности р-ций в пентозофосфатном цикле осуществляется гл. обр. ферментами, участвующими в этом цикле: избыток того или иного субстрата подавляет активность фермента, катализирующего его синтез, или активирует фермент, катализирующий его трансформацию в др. соединение.
Относит. кол-ва глюкозы, превращающиеся через пентозофосфатный цикл, неодинаковы в разных тканях. В мышцах скорость пентозофосфатного цикла очень низка, а в печени не менее 30% CO2 образуется при окислении глюкозы в пентозофосфатном цикле. В др. тканях, где активно проходитбиосинтез жирных к-т и стероидов (семенниках, жировой ткани, лейкоцитах, коре надпочечников, молочной железе), доля пентозофосфатного цикла в окислит. метаболизме глюкозы также очень значительна.
Интенсивность пентозофосфатного цикла зависит от функцион. состояния ткани и от гормонального статуса (напр., в печени резко снижается при голодании из-за инактивации дегидрогеназ пентозофосфатного цикла и восстанавливается вскоре после кормления). Скорость пентозофосфатного цикла регулируется в первую очередь концентрацией НАДФН. Обе дегидрогеназы пентозофосфатного цикла (р-ции 1 и 3) чувствительны к изменению величины отношения НАДФ/НАДФН: при его величине 0,02 активность дегидрогеназ в печени максимальна, а при величине 0,01 снижается на 90%. Интенсивный пентозофосфатный цикл происходит в эритроцитах, что связано с необходимостью НАДФН-зависимоговосстановления глутатиона кофактора глутатионредуктазы эритроцитов.
Нарушения функционирования нек-рых ферментов пентозофосфатного цикла приводят к развитию тяжелых заболеваний человека. Недостаточность глюкозо-6-фосфат-дегидрогеназы в эритроцитах служит причиной лек. гемолитич. анемии, а снижение активности транскетолазы в результате нарушения ее способности связывать тиамин приводит к развитию нервно-психич. расстройства синдрома Вернике Корсакова.
1. 33 Структура и свойства глюкозы. Качественные реакции.
Глюко́за (греч. γλυκόζη, от γλυκύς сладкий) (C6H12O6), или виноградный сахар, или декстроза встречается в соке многих фруктов иягод, в том числе и винограда, от чего и произошло название этого вида сахара. Является шестиатомным сахаром (гексозой). Глюкозное звено входит в состав ряда ди- (мальтозы, сахарозы и лактозы) и полисахаридов (целлюлоза, крахмал). Открыта в 1802 году лондонским врачом Уильямом Праутом. В 1819 году Анри Бракконо получил глюкозу из древесных опилок. Физические свойства
Бесцветное кристаллическое вещество сладкого вкуса, растворимое в воде, растворимо в реактиве Швейцера (аммиачном растворе гидроксида меди Cu(NH3)4(OH)2), в концентрированном растворе хлорида цинка и концентрированном растворе серной кислоты.
[править]Строение молекулы
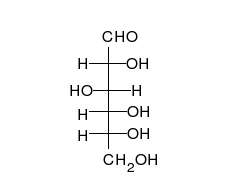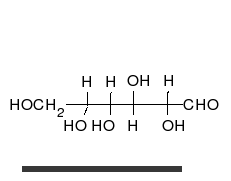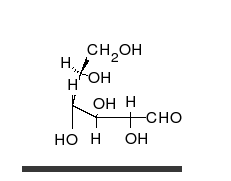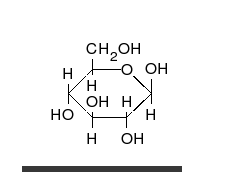

Переход глюкозы из проекции Фишера впроекцию Хоуорса.
Глюкоза — конечный продукт гидролиза большинства дисахаридов и полисахаридов.
[править]Получение
В промышленности глюкозу получают гидролизом крахмала. В природе глюкоза образуется растениями в процессе фотосинтеза.
[править]Химические свойства
Глюкоза может восстанавливаться в шестиатомный спирт (сорбит). Глюкоза легко окисляется. Она восстанавливает серебро из аммиачного раствора оксида серебра и медь(II) до меди(I).
Проявляет восстановительные свойства. В частности, в реакции растворов сульфата меди с глюкозой и гидроксидом натрия. При нагревании эта смесь реагирует с обесцвечением (сульфат меди сине-голубой) и образованием красного осадка оксида меди(I).
Образует оксимы с гидроксиламином, озазоны с производными гидразина.
Легко алкилируется и ацилируется.
При окислении образует глюконовую кислоту, если воздействовать сильными окислителями на ее гликозиды, и гидролизовать полученный продукт можно получить глюкуроновую кислоту, при дальнейшем окислении образуется глюкаровая кислота.
[править]Биологическая роль
Глюкоза — основной продукт фотосинтеза, образуется в цикле Кальвина.
В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспеченияметаболических процессов. Глюкоза депонируется у животных в виде гликогена, у растений - в виде крахмала, полимер глюкозы - целлюлозаявляется основной составляющей клеточных оболочек всех высших растений.
[править]Применение
Глюкозу используют при интоксикации (например при пищевом отравлении или деятельности инфекции), вводят внутривенно струйно и капельно, так как она является универсальным антитоксическим средством. Также препараты на основе глюкозы и сама глюкоза используется эндокринологами при определении наличия и типа сахарного диабета у человека (в виде стресс теста на вывод повышенного количества глюкозы из организма)
СН2ОН – (СНОН)4 – СОН + Сu(ОН)2 = СН2ОН – (СНОН)4 – СООН + Сu2О↓+ Н2О
СН2ОН – (СНОН)4 – СОН + Ag2O = СН2ОН – (СНОН)4 – СООН + 2Ag↓
36 Ксенобиотики.
сенобиотики (от греч. ξένος — чуждый и βίος — жизнь) — условная категория для обозначения чужеродных для живых организмов химических веществ, естественно не входящих в биотический круговорот. Как правило, повышение концентрации ксенобиотиков в окружающей среде прямо или косвенно связано с хозяйственной деятельностью человека. К ним в ряде случаев относят: пестициды, некоторые моющие средства (детергенты), радионуклиды, синтетические красители, полиароматические углеводороды и др. Попадая в окружающую природную среду, они могут вызвать повышение частоты аллергических реакций, гибель организмов, изменить наследственные признаки, снизить иммунитет, нарушить обмен веществ, нарушить ход процессов в естественных экосистемах вплоть до уровня биосферы в целом.
Изучение превращений ксенобиотиков путём детоксикации и деградации в живых организмах и во внешней среде важно для организации санитарно-гигиенических мероприятий по охране природы.
Ксенобиотики — любые чуждые для организма вещества (пестициды, токсины, др. поллютанты), способные вызвать нарушение биологических процессов, не обязательно яды или токсины. Однако в большинстве случаев ксенобиотики, попадая в живые организмы, могут вызывать различные прямые нежелательные эффекты[1], либо вследствие биотрансформации образовывать токсичные метаболиты:
· токсические или аллергические реакции
· изменения наследственности
· снижение иммунитета
· специфические заболевания (болезнь минамата, болезнь итай-итай, рак)
· искажение обмена веществ, нарушение естественного хода природных процессов в экосистемах, вплоть до уровня биосферы в целом.
Изучением влияния ксенобиотиков на иммунную систему занимается иммунотоксикология.
· тяжёлые металлы (кадмий, свинец, ртуть и другие)
· фреоны
· нефтепродукты
· пластмассы, особенно это относится к пластиковой упаковке (полиэтиленовые пакеты, пластиковые ПЭТФ-бутылки и т.д.)
· полициклические и галогенированные ароматические углеводороды
· пестициды
· синтетические поверхностно-активные вещества[2]
Некоторые вещества, относимые к ксенобиотикам, могут быть найдены в природе. Так, диоксины образуются в результате естественных процессов, таких как извержения вулканов и лесные пожары[3]. Многие вещества, например ксилол, стирол, толуол, ацетон, бензол, пары бензина или хлороводорода, могут быть отнесены к ксенобиотикам, если они накопятся вокружающей среде в неестественно высоких концентрациях в процессе промышленного производства.
39Гликоген, его превращения при нагрузке и в период отдыха. Влияние алкоголя на гликогенез.
Гликоген синтезируется в печени и откладывается в ней про запас. Это дает организму возможность немедленно получить новую порцию гликогена в случае необходимости, например, при потребности в энергии в результате усиленного физического напряжения или при больших промежутках между приемами пищи. В таких случаях гликоген расщепляется и вновь превращается в глюкозу. Процесс расщепления гликогена сопровождается выделением энергии.
Печень поддерживает содержание гликогена на постоянном уровне. Количество гликогена в печени должно быть не ниже определенного уровня, поскольку недостаток гликогена в печени снижает ее устойчивость к вредным воздействиям. Поэтому очень важно, особенно при заболеваниях печени, обеспечивать достаточный приток глюкозы в печень. Одновременно необходимо также обеспечить поступление в организм витамина С, который способствует отложению гликогена в печени.
При нормальной деятельности печени запасы гликогена в ней пополняются непрерывно из имеющихся в крови моносахаридов: глюкозы, фруктозы, галактозы и маннозы. Синтез и распад гликогена регулируется сложным механизмом с участием нервной и эндокринной систем.
Содержание гликогена в печени меняется при физической нагрузке. При интенсивной и длительной мышечной работе количество гликогена в печени может резко упасть до нижней границы физиологической нормы. Интенсивная физическая работа при недостаточном питании может полностью лишить печень гликогена. Об этом надо всегда помнить и по возможности не допускать подобных ситуаций.
1. 41 Оксигеназы и их роль в трансформации веществ.
Оксигеназы - это ферменты, катализирующие активирование О2 и последующее включение 1 или 2 его атомов в молекулы различных субстратов. Если субстратом (акцептором О2) служит водород, фермент называют оксидазой. В этом смысле оксидазы можно рассматривать как специализированный класс оксигеназ.
Оксигеназы играют важную роль в процессах биосинтеза, деградации и трансформации клеточных метаболитов: ароматических аминокислот, липидов, сахаров, порфиринов, витаминов. Субстратами, на которые воздействуют оксигеназы, часто служат сильно восстановленные не растворимые в воде соединения; их окисление приводит к тому, что продукты реакции становятся более растворимыми в воде и, следовательно, биологически активными, что важно для их последующего метаболизирования. У строго анаэробных прокариот кислород, включаемый в молекулу субстрата, происходит не из О2, а из других соединений, например воды.
47Классификация витаминов.
Современная классификация витаминов не является совершенной. Она основана на физико-химических свойствах (в частности, растворимости) или на химической природе, но до сих пор сохраняются и буквенные обозначения. В зависимости от растворимости в неполярных органических растворителях или в водной среде различают жирорастворимые и водорастворимые витамины. В приводимой классификациивитаминов, помимо буквенного обозначения, в скобках указан основной биологический эффект, иногда с приставкой «анти», указывающей на способность данного витамина предотвращать или устранять развитие соответствующего заболевания; далее приводится номенклатурное химическое название каждоговитамина.
 2015-05-06
2015-05-06 768
768








