8…10 г почвы, отделенной от растительных остатков и просеянной через сито 0,25 мм, поместить в коническую колбу на 100 мл. Из бюретки прилить точно 10 мл хромовой смеси (K2Cr2O7 в кислоте). Осторожно круговыми движениями взболтать содержимое.
Накрыв колбу воронкой, кипятить содержимое колбы ровно 5 мин. Отсчет времени начинают с момента появления пузырьков газа. Кипение должно быть медленным.
При нагревании идет реакция
2K2Cr2O7+8Н2SO4+3C(гумус) → 2K2SO4+2Cr2(SO4)3+8H2O+3CO2
По окончании кипения колбу снять с плитки, охладить до комнатной температуры. Перенести содержимое в колбу на 500 мл, смыть дистиллятом остатки с воронки и маленькой колбы и тоже перенести вместе с дистиллятом в колбу. Довести содержимое большой колбы до 250 мл. Добавить 2 мл 85 %-ного раствора фосфорной кислоты и восемь капель дифениламина в качестве индикатора (вместо дифениламина можно использовать 5 … 8 капель 2 %-ного раствора фенилантраниловой кислоты).
Содержимое колбы оттитровать 0,2 н. раствором соли Мора до перехода темно-бурой окраски через фиолетовую и синюю в грязно-зеленую. При появлении синего цвета титровать нужно осторожно.
Параллельно необходимо провести холостое титрование. Для этого взять 0,2 г прокаленного песка, поместить в коническую колбу на 100 мл, прилить 10 мл 0,4 н. раствора хромовой смеси, закрыть воронкой, прокипятить 5 мин, охладить и, добавив фосфорную кислоту и индикатор (как указано выше), оттитровать.
Вычислить процентое содержание гумуса в почвенном образце по формуле
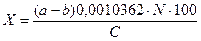 ,
,
где a – объем раствора соли Мора, затраченный на холостое титрование 10 мл хромовой смеси, мл; b – объем раствора соли Мора, затраченный на титрование содержимого колбы после окисления гумуса бихроматом калия, мл; N – концентрация соли Мора; 100 – коэффициент пересчета на 100 гпочвы; 0,0010362 – коэффициент пересчета на гумус (показывает, что 1 мл 0,2 н. раствора соли Мора соответствует такому количеству хромовой кислоты, которое окисляет 0,0010362 г гумуса, или 0,0006 г углерода).
 2015-04-20
2015-04-20 505
505








