В реакции между серной кислотой и тиосульфатом натрия:
Na2S2O3 + H2SO4 = Na2SO4 + H2S2O3,
H2S2O3 = H2O + SO2 + S
нерастворимая сера выделяется в виде мути. Время от начала реакции до появления первых следов мути зависит от концентрации реагирующих веществ и температуры.
Опыт. Возьмите 8 пронумерованных пробирок. В четыре пробирки (1, 2, 3, 4) налейте указанное в таблице количество мл раствора тиосульфата натрия и воды, тщательно перемешайте. Массовая доля раствора тиосульфата натрия ω0 = 7 %, плотность – ρ = 1,049 г/мл. В другие (1а, 2а, 3а, 4а) четыре пробирки отмерьте из бюретки по 6 мл раствора серной кислоты. Влейте в пробирку №1 отмеренное количество серной кислоты №1а, хорошо перемешайте, отсчитайте время по секундомеру с момента сливания до появления мути в пробирке. При прочих равных условиях, относительную скорость реакции можно определить как величину, обратно пропорциональную найденному времени (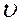 = 1/t).
= 1/t).
Произведите такие же опыты со всеми другими пробирками. Результаты опыта сведите в таблицу 2.1.
Таблица 2.1
| № пробирки | Объем | Объем | Объем | Массовая доля Na2S2O3 в растворе, ω, % | Промежуток времени от начала отсчета до помутнения, t, с | Относи-тельная скорость реакции, 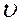 = 1/t = 1/t |
| раствора Na2S2O3 V(a),мл | H2O V(в),мл | раствора H2SO4, V,мл | ||||
Массовая доля Na2S2O3 в растворе рассчитывается по формуле:

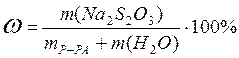 ,
,
где m(Na2S2O3) – масса тиосульфата натрия в растворе, г;
mР-РА – масса раствора тиосульфата натрия, г;
m(Н2О) – масса добавленной воды, г.
Масса Na2S2O3 рассчитывается по формуле:
m(Na2S2O3)= (ω0·V(a)·ρ) / 100%.
Масса раствора рассчитывается по формуле:
mР-РА= V(a)·ρ.
Масса добавленной воды рассчитывается по формуле:
m(Н2О) = V(в)·ρ(Н2О),
где ρ(Н2О) – плотность воды, ρ(Н2О) = 1 г/мл.
Постройте график зависимости скорости реакции 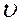 (ось y) от концентрации С (ось х). В соответствии с законом действия масс зависимость скорости реакции от концентрации должна выражаться прямой линией, проходящей через начало координат. Сделайте вывод о зависимости скорости реакции от концентрации.
(ось y) от концентрации С (ось х). В соответствии с законом действия масс зависимость скорости реакции от концентрации должна выражаться прямой линией, проходящей через начало координат. Сделайте вывод о зависимости скорости реакции от концентрации.
 2015-04-20
2015-04-20 880
880








