Развитие представлений о развитии атома
Этапы делятся на 4 типа:
1) «Кусочки материи».
Демокрит полагал, что свойства того или иного вещества определяются формой, массой, пр. характеристиками образующих его атомов: у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с дружкой, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов.
2) «Пудинг с изюминками» (модель Дж. Томсона).
Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Эта модель не объясняет сериальный характер излучения атома.
3) Атом, «типа Сатурна». 1904 год. Хентара Нагаока. Маленькое положительное ядро, вокруг которого, по орбиталям, вращаются электроны.
4) «Планетарная модель атома». 1911 год. Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой скорее некоторое подобие планетной системы, то есть что электроны движутся вокруг положительно заряженного тяжёлого ядра, расположенного в центре атома. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает. Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Квантовые числа и двойственная природа электрона
Квантовые числа — энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
1. Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3,...)
2. Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n -1(l = 0, 1, 2, 3,..., n -1). Каждому значению l соответствует орбиталь особой формы. Орбитали с l = 0 называются s -орбиталями,
l = 1 – р -орбиталями (3 типа, отличающихся магнитным квантовым числом m),
l = 2 – d -орбиталями (5 типов),
l = 3 – f -орбиталями (7 типов).
3. Магнитное квантовое число m определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Его значения изменяются от + l до - l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р -АО: р x, р y, р z.
4. Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином (от англ. веретено). Для обозначения электронов с различными спинами используются символы: 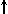 и
и 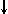 .
.
5. Отчетливо проявляющаяся двойственная природа электрона не позволяет его рассматривать как обычную (классическую) частицу.
6. С двойственной природой электрона связано соотношение неопределенностей, в соответствии с которым невозможно одновременно точно измерить и координаты, и импульс (mv) этой частицы. Если электрон локализован в небольшой области около ядра, неопределенность его положения мала, но в этом случае велика неопределенность импульса, что означает большую кинетическую энергию электрона.
В чем заключается двойственная природа электрона.
7. Представления о стационарных состояниях атома и двойственной природе электрона, а также требования принципа неопределенности были использованы австрийским физиком Эрви-ном Шредингером, который в 1926 г. предложил модель, описывающую электрон в атоме как своего рода стоячую волну, причем вместо точного положения электрона в пространстве рассматривалась вероятность его пребывания в определенном месте.
8. Атомы химического элемента не имеют строго Определенных размеров, что обусловлено двойственной природой электронов. Пользуются эффективными или кажущимися радиусами шарообразных атомов, сближенных при образовании кристаллов.
9. В последнее время в электронной теории химической связи были выдвинуты новые идеи на основе квантово-механических воззрений, вытекающих из положения современной физики о двойственной природе электрона, в единстве сочетающего свойства микрочастицы и волны. По этим воззрениям движение электронов может быть рассмотрено с учетом принципа вероятности и описано уравнениями волновой механики.
10. В последнее время в электронной теории химической связи были выдвинуты новые идеи на основе квантово-механических воззрений, вытекающих из положения современной физики о двойственной природе электрона, в единстве сочетающего свойства микрочастицы и волны, По этим воззрениям движение электронов может быть рассмотрено с учетом принципа вероятности и описано уравнениями волновой механики.
11. Двойственная природа электрона - корпускулярная и волновая - не совместима с понятиями классической механики, которая представляет электрон как точечную частицу, описывающую вполне определенную траекторию со скоростью, известной в каждый момент времени.
12. Подобно тому как для объяснения всех свойств света необходимо привлекать как волновую, так и корпускулярную модели, точно так же электроны и ядра атомов приходится рассматривать и как электрически заряженные частицы, и как волны. Математическим выражением двойственной природы электронов, находящихся в атомах и молекулах, является волновое уравнение Шредингера. Решая это дифференциальное уравнение для какой-либо системы, можно получить значения энергии различных возможных состояний, или уровни энергии, на которых может находиться система. Поглощение атомом или молекулой кванта света может произойти только в том случае, если величина кванта точно равна разности энергий двух состояний, возможных для системы.
13. Необходимо исправить прежнюю механику с учетом двойственной природы электрона. Электронная волна с течением времени распространяется причинно, по законам распространения волн, но положение электрона как частицы нельзя предсказать точно, можно только указать вероятность того или иного положения. Чем плотнее в данном месте электронная волна, тем выше вероятность обнаружить там электрон.
14. Гейзенбергом был предложен принцип неопределенности, который позволяет учесть двойственную природу электрона при описании его поведения.
 2015-04-20
2015-04-20 3928
3928







