а) Алкилирование
Примеры реакций алкилирования обсуждались при рассмотрении методов получения аминов.
б) Ацилирование
2RNH2 + R/COX ® R/CONHR + RNH3X
2R2NH + R/COX ® R/CONR2 + R2NH2X
(X=Cl, OCOR/)
Ацилирование аминов функциональными производными карбоновых кислот дает возможность получать вторичные и третичные амиды из первичных и вторичных аминов соответственно. Реакция подробно обсуждена ранее (лекция №36).
в) Взаимодействие с сульфонилхлоридами
Сульфонилхлориды взаимодействуют с аминами, давая сульфонамиды. Реакция с бензолсульфонилхлоридом лежит в основе пробы Гинсберга, позволяющей различать и разделять первичные, вторичные и третичные амины.
Сульфонамиды, образующиеся из первичных аминов, являются NH-кислотами и со щелочами дают растворимые в воде соли.
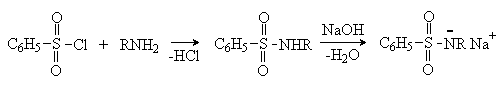
Вторичные амины дают сульфонамиды, которые не содержат кислого водорода и не растворяются в щелочах.
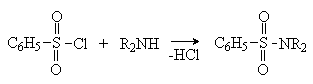
Третичные амины не реагируют.
г) Нитрозирование
Нитрозирование аминов происходит при взаимодействии с азотистой кислотой в кислой среде. Неустойчивую азотистую кислоту генерируют действием сильной кислоты на нитриты. Реакция протекает по-разному в зависимости от типа амина.
Первичные алифатические амины реагируют с образованием неустойчивых алкилдиазониевых солей, которые разлагаются с выделением газообразного азота и сложной смеси продуктов дезаминирования.
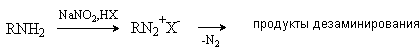
Образование солей диазония – сложный многостадийный процесс, который подробно будет рассмотрен на примере ароматических аминов.
Разложение катиона алкилдиазония приводит к образованию карбокатиона, который стабилизируется путем алкилирования присутствующих в реакционной среде нуклеофилов или путем отщепления протона с образованием алкена. Этим процессам может предшествовать изомеризация карбокатиона в энергетически более стабильный ион. Так, разложение катиона н -пропилдиазония в водном растворе наряду н-пропиловым спиртом дает изопропиловый спирт, а также продукт элиминирования - пропен.
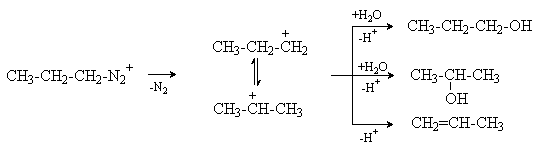
Со вторичными аминами азотистая кислота образует нерастворимые в реакционной среде нитрозамины.
R2NH + NaNO2 + HCl ® R2N-N=O + NaCl + H2O
Третичные амины в сильнокислой среде при комнатной температуре с азотистой кислотой не реагируют.
Нитрозирование аминов препаративного значения не имеет. Аналитическое значение этих реакций заключается в возможности качественно различить первичные, вторичные и третичные амины.
д) Галогенирование
Первичные и вторичные амины реагируют с гипогалогенитами с образованием N-галогенаминов.
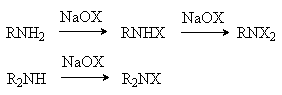
(X= Cl, Br)
N-галогенамины – сильные окислители и галогенирующие реагенты.
 2015-04-23
2015-04-23 794
794








