Определение. Эвтектика – это механическая смесь двух или более видов кристаллов, одновременно кристаллизовавшихся из жидкости.
Это слово (греч.) обозначает хорошо, или легко, плавящийся.
Фазами эвтектики могут быть чистые элементы (А и В), химические соединения (AmBn) и твердые растворы (А(В), В(А)). Обозначаются эвтектики Э(Ф1 + Ф2), где Ф – соответствующая фаза, например Э(Рb + Sb), Э(А1(Сu) + СuА12).
Эвтектики могут состоять из двух и более фаз. При микроскопическом исследовании металлографических шлифов эвтектические структуры выглядят как механические смеси кристаллов. По строению эвтектики могут быть пластинчатыми, игольчатыми, дендритными и т. д. (рис. 3.3), зависящими от условий охлаждения, сходства или различия кристаллических решеток фаз, составляющих эвтектику.
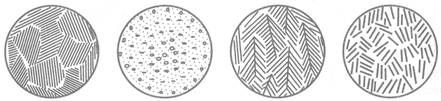
Рис. 3.3 – Строение эвтектик
В диаграммах III рода не образуются фазы, представляющие собой чистые компоненты. Из жидкости могут выделяться только твердые растворы а или В. Следовательно, около вертикалей А и В (рис. 3.4), соответствующих чистым компонентам, находятся области существования твердых растворов α или β. Предельная растворимость компонента В в А определяется линией DF, а предельная растворимость А в В – линией CG.
Сплавы, находящиеся между этими двумя линиями, находятся за пределами растворимости и являются двухфазными, состоящими из α + β.
Линия АЕВ является линией ликвидус, линия ADCB – линией солидус. Применяя правило фаз и правило отрезков, проследим за процессом кристаллизации сплава.
Кристаллизация сплава I. Выше точки 1 сплав находится в жидком состоянии. В точке 1 начинается процесс кристаллизации. Выделяются кристаллы твердого раствора α, концентрация которого изменяется по кривой а – 2, а состав жидкости изменяется по кривой 1 – b. В точке 2 кристаллизация закончится, и полученные кристаллы твердого раствора α будут иметь концентрацию исходной жидкости.
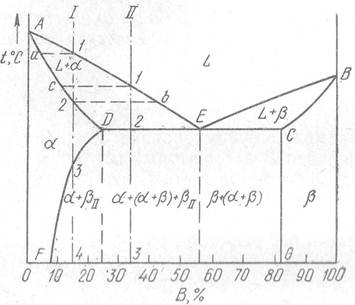
Рис. 3.4 – Диаграмма состояния с эвтектикой
Эти кристаллы не претерпевают изменений до точки 3, лежащей на линии предельной растворимости. Ниже этой точки твердый раствор α является пересыщенным (по отношению к компоненту В) и выделяет избыточные кристаллы. Такими кристаллами являются кристаллы β-твердого раствора, что определяют, применяя правило рычага для сплава, лежащего внутри двухфазной области α + β (т. е. для сплава ниже линии DF).
Состав твердого раствора α изменяется по кривой 3 – F, вследствие выделения кристаллов β концентрации G. Количество кристаллов β при охлаждении увеличивается. Количество кристаллов β, выделившихся из сплава I, характеризуется отрезком от вертикали I до линии 3 – F.
Кривая охлаждения и схемы структур этого сплава при различных температурах показаны на рис. 3.5.
Определения. 1. Кристаллы β, выделившиеся из твердого раствора, называются вторичными кристаллами и часто обозначаются символом βII в отличие от первичных β-кристаллов (βI), выделяющихся из жидкости.
2. Процесс выделения вторичных кристаллов из твердой фазы носит название вторичной кристаллизации в отличие от процесса первичной кристаллизации, когда кристаллы (первичные) образуются в жидкой фазе.
Отметим, что сплав, концентрация которого лежит левее точки F, не будет иметь вторичных выделений β-кристаллов.
Так как линия CG в отличие от линии FD изображена на рис. 3.5 вертикальной, т.е. растворимость компонента А в В не зависит от температуры, то вторичных выделений α-кристаллов нет, но они были бы, если бы линия CG была наклонена вправо, т. е. растворимость (компонента А) уменьшалась бы с понижением температуры.
Точка D для твердого раствора α показывает максимальную растворимость компонента В в компоненте А.
Рис. 3.5 –
Кристаллизация сплава II. При кристаллизации этого сплава, в отличие от предыдущего, при достижении горизонтальной линии DEC наступает нонвариантная реакция.
 2015-04-23
2015-04-23 2141
2141







