§ Простые. Неполярные:
§ омыляемые;
§ жиры (триаглицерины);
§ воска (эфиры);
§ неомыляемые;
§ стероиды (холестерин).
§ Сложные. Полярные. Омыляемые:
§ глицерофосфолипиды;
§ сфингофосфолипиды;
§ гликолипиды.
3.Фосфопротеины - сложные белки. Их простетическая группа представлена фосфорной кислотой. Остатки фосфата соединяются с белковой частью молекулы сложноэфирными связями через гидрокси-группы аминокислот серина и треонина.
К фосфопротеинам относятся казеины - белки молока, вителлины - яичного желтка, овальбумин - белок куриного яйца. Большое количество их содержится в ЦНС. Многие важные ферменты клетки активны только в фосфорилированной форме. Фосфопротеины являются источником энергетического и пластического материала.
4. Пример металлопротеинов:
- ферритин, трансферрин - Fe;
- алкогольдегидрогеназа - Zn;
- цитохромоксидаза - Cu;
- протеиназы - Mg, К;
- АТФ-аза - Na, К, Са, Мg.
Как правило, металлопротеины - ферменты. Ионы металлов выполняют следующие функции:
- являются активным центром фермента;
- служат мостиком между активным центром фермента и субстратом, сближают их;
- служат акцепторами электронов на определенной стадии ферментативной реакции.
13. Ферменты и их химические строение, основные коферменты. (НАД, НАДФ, КОА)
Ферменты- обычно белковые молекулы или молекулы РНК или их комплексы, ускоряющие химические реакции в живых системах. Реагенты в реакции, катализируемой ферментами, называются субстратами, а получающиеся вещества — продуктами.
Ферменты присутствуют во всех живых клетках и способствуют превращению одних веществ (субстратов) в другие (продукты). Ферменты выступают в роли катализаторов практически во всех биохимических реакциях, протекающих в живых организмах — ими катализируется более 4000 разных биохимических реакций[2]. Ферменты играют важнейшую роль во всех процессах жизнедеятельности, направляя и регулируя обмен веществ организма.
По строению ферменты могут быть однокомпонентными, простыми белками, и двухкомпонентными, сложными белками. Во втором случае в составе фермента обнаруживается добавочная группа небелковой природы.
Характерной особенностью двухкомпонентных ферментов является то, что ни белковая часть, ни добавочная группа в отдельности не обладают заметной каталитической активностью. Только их комплекс проявляет ферментативные свойства. При этом белок резко повышает каталитическую активность добавочной группы, присущую ей в свободном состоянии в очень малой степени; добавочная же группа стабилизирует белковую часть и делает ее менее уязвимой к денатурирующим агентам. Таким образом, хотя непосредственным исполнителем каталитической функции является простетическая группа, образующая каталитический центр, ее действие немыслимо без участия полипептидных фрагментов белковой части фермента. Более того, в апоферменте есть участок, характеризующийся специфической структурой, избирательно связывающий кофермент. Это так называемый кофермент связывающий домен; его структура у различных апоферментов, соединяющихся с одним и тем же коферментом, очень сходна. Таковы, например, пространственные структуры нуклеотидсвязывающих доменов ряда дегидрогеназ.
Иначе обстоит дело у однокомпонентных ферментов, не имеющих добавочной группы, которая могла бы входить в непосредственный контакт с преобразуемым соединением. Эту функцию выполняет часть белковой молекулы, называемая каталитическим центром. Предполагают, что каталитический центр однокомпонентного фермента представляет собой уникальное сочетание нескольких аминокислотных остатков, располагающихся в определенной части белковой молекулы.
КОФЕРМEНТЫ (от лат. со- - приставка, означающая совместность, и ферменты) (коэнзимы), орг. прир. соед., необходимые для осуществления каталитич. действия ферментов. Эти вещества, в отличие от белкового компонентафермента (апофермента), имеют сравнительно небольшую мол. массу и, как правило, термостабильны. Иногда под К. подразумевают любые низкомол. вещества, участие которых необходимо для проявления каталитич. Действия фермента, в т. ч. и ионы, например К+, Mg2+ и Мn2+.
Основные коферменты:
· Никотинамидадениндинуклеоти́д (НАД, NAD) — кофермент, присутствующий во всех живых клетках, входит в состав ферментов группы дегидрогеназ, катализирующих окислительно-восстановительные реакции; выполняет функцию переносчика электронов и водорода, которые принимает от окисляемых веществ.Представляет собой динуклеотид, молекула которого построена из амида никотиновой кислоты и аденина, соединённых между собой цепочкой, состоящей из двух остатков D-рибозы и двух остатков фосфорной кислоты; применяется в клинической биохимии при определении активности ферментов крови.
· Никотинамидадениндинуклеотидфосфа́т (НАДФ, NADP) — широко распространённый в природе кофермент некоторых дегидрогеназ — ферментов, катализирующих окислительно-восстановительные реакции в живых клетках. NADP принимает на себя водород и электроны окисляемого соединения и передаёт их на другие вещества. Вхлоропластах растительных клеток NADP восстанавливается при световых реакциях фотосинтеза и затем обеспечивает водородом синтез углеводов при темновых реакциях. NADP, — кофермент, отличающийся от NAD содержанием ещё одного остатка фосфорной кислоты, присоединённого к гидроксилу одного из остатков D-рибозы, обнаружен во всех типах клеток.
· Кофермент А (КоА) — кофермент ацетилирования; один из важнейших коферментов; принимает участие в реакциях переноса ацильных групп.Молекула КоА состоит из остатка адениловой кислоты, связанной пирофосфатной группой с остатком пантотеновой кислоты, соединённой пептидной связью с остатком β-меркаптоэтаноламина. С КоА связан ряд биохимических реакций, лежащих в основе окисления и синтеза жирных кислот, биосинтеза жиров, окислительных превращений продуктов распада углеводов. Во всех случаях КоА действует в качестве промежуточного звена, связывающего и переносящего кислотные остатки на другие вещества. При этом кислотные остатки в составе соединения с КоА подвергаются тем или иным превращениям, либо передаются без изменений на определённые метаболиты.
14. Механизм действия ферментов.
Скорость ферментативной реакции зависит от концентрации субстрата [S] и количества присутствующего фермента. Эти величины определяют, сколько молекул фермента соединится с субстратом, и именно от содержания фермент-субстратного комплекса зависит скорость реакции, катализируемой данным ферментом. В большинстве ситуаций, представляющих интерес для биохимиков, концентрация фермента очень мала, а субстрат присутствует в избытке.
Выяснение механизмов действия ферментов во всех деталях – дело будущего, однако некоторые важные их особенности уже установлены. Каждый фермент имеет один или несколько активных центров, с которыми и связывается субстрат. Эти центры высокоспецифичные, т.е. «узнают» только «свой» субстрат или близкородственные соединения.
15. Условия оптимального действия ферментов.
Температура. Ферменты теряют активность при нагревании; при температуре от 50 до 60° С большинство ферментов быстро инактивируются. Инактивация ферментов необратима, так как после охлаждения активность не восстанавливается. Этим можно объяснить, почему непродолжительное воздействие высокой температуры убивает большинство организмов: часть их ферментов инактивируется и обмен веществ продолжаться не может. Известно несколько исключений из этого правила. Некоторые виды примитивных растений — сине-зеленых водорослей — живут в горячих источниках, например в источниках Йеллоустонского национального парка, где температура воды достигает почти 100° С. Эти водоросли обусловливают яркую окраску травертиновых террас вокруг горячих источников. При температурах ниже той, при которой наступает инактивация ферментов (около 40° С), скорость большинства ферментативных реакций, как и скорость других химических реакций, примерно удваивается с повышением температуры на каждые 10° С.
Замораживание обычно не приводит к инактивации ферментов; при низких температурах ферментативные реакции идут очень медленно или не идут вовсе, но при повышении температуры до нормальной каталитическая активность возобновляется.
Кислотность. Ферменты чувствительны к изменениям pH, т. е. к изменению кислотности или щелочности среды. Пепсин — фермент, переваривающий белки, выделяемый слизистой оболочкой желудка, — замечателен тем, что он активен только в очень кислой среде и лучше всего действует при pH 2. Трипсин, расщепляющий белки и выделяемый поджелудочной железой, служит примером фермента, проявляющего оптимальную активность в щелочной среде, при pH около 8,5. Большинство внутриклеточных ферментов имеют оптимумы pH близ нейтральной точки, а в кислой или щелочной среде их активность значительно ниже; под действием сильных кислот и оснований они необратимо инактивируются.
16. Классификация ферментов.

• Гр 1: Оксидоредуктазы, катализирующие окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа
• Гр 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.
• Гр 3: Гидролазы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза
• Гр 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов.
• Гр 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата.
• Гр 6: Лигазы, катализирующие образование химических связей между субстратами за счет гидролиза АТФ. Пример: ДНК-полимераза
Будучи катализаторами, ферменты ускоряют как прямую, так и обратную реакции, поэтому, например, лиазы способны катализировать и обратную реакцию — присоединение по двойным связям.
17. Экстрактивные азотистые вещества.
Азотистые экстрактивные вещества — карнозин, креатин, ансерин, пу-риновые основания (гипоксантин) и др. Основное значение экстрактивных веществ заключается в их вкусовых свойствах и стимулирующем действии на секрецию пищеварительных желез.
Наличием азотистых экстрактивных веществ в. значительной степени обусловливается вкус мяса, особенно бульонов и корочки, образующейся при жарении мяса. Мясо взрослых животных богаче экстрактивными веществами и имеет более выраженный вкус, чем мясо молодых животных. Этим объясняется, что крепкие бульоны могут быть получены только из мяса взрослых животных. Экстрактивные вещества мяса являются энергичными возбудителями секреции желудочных желез, в связи с чем крепкие бульоны и жареное мясо в наибольшей степени возбуждают
отделение пищеварительных соков. Вываренное мясо этим свойством не обладает и поэтому оно широко используется в диетическом, химически щадящем рационе, при гастритах, язвенной болезни, заболеваниях печени ш других болезнях органов пищеварения.
18. Общая схема обмена белковых веществ.
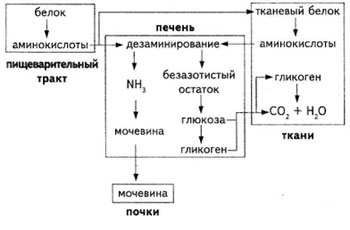
После расщепления белков в пищеварительном тракте образовавшиеся аминокислоты всасываются в кровь. В кровь всасывается также незначительное количество полипептидов — соединений, состоящих из нескольких аминокислот. Из аминокислот клетки нашего тела синтезируют белок, причем белок, который образуется в клетках человеческого организма, отличается от потребленного белка и характерен для человеческого организма.
Образование нового белка в организме человека и животных идет беспрерывно, так как в течении всей жизни взамен отмирающих клеток крови, кожи, слизистой оболочки, кишечника и т. д. создаются новые, молодые клетки. Для того чтобы клетки организма синтезировали белок, необходимо, чтобы белки поступали с пищей в пищеварительный канал, где они подвергаются расщеплению на аминокислоты, и уже из всосавшихся аминокислот будет образован белок.
19. Дезаминирование аминокислоты
Дезаминирование — процесс удаления аминогрупп от молекулы. Ферменты, катализирующие дезаминирование, называют деаминазами.
В организме человека дезаминирование в основном происходит в печени, однако, глютамат дезаминируется также и в почках. Аминогруппа, которая удаляется от аминокислот в ходе дезаминирования, превращается далее в аммиак. Остов аминокислоты, состоящий из атомов углерода и водорода, может далее использоваться в реакциях анаболизма или катаболизма. Аммиак является токсичным для человека, поэтому существуют ферменты, превращающие аммиак в мочевину или мочевую кислоту.
Деаминаза - фермент, катализирующий удаление аминогруппы (-NH2) из химического соединения (обычно аминокислоты или амина).
Существует несколько способов дезаминирования аминокислот:
· окислительное;
· непрямое (трансдезаминирование);
· неокислительное;
· внутримолекулярное.
Окислительно е: наиболее активно в тканях происходит дезаминирование глутаминовой кислоты. Реакцию катализирует фермент глутаматдегидрогеназа, коферментом глутаматдегидрогеназы является NAD+. Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование а-иминоглутарата, затем - неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется а-кетоглутарат.
Непрямое: непрямое дезаминирование аминокислот происходит при участии 2 ферментов: аминотрансферазы (кофермент ПФ) и глутаматдегидрогеназы (кофермент NAD+). Значение этих реакций в обмене аминокислот очень велико, так как непрямое дезаминирование - основной способ дезаминирования большинства аминокислот. Обе стадии непрямого дезаминирования обратимы, что обеспечивает как катаболизм аминокислот, так и возможность образования практически любой аминокислоты из соответствующей α-кетокислоты.
Этот путь дезаминирования преобладает в мышцах при интенсивной работе, в результате которой накапливается молочная кислота.
Неокислительное дезамитрование: в печени человека присутствуют специфические ферменты, катализирующие реакции дезаминирования аминокислот серина, треонина и гистидина неокислительным путём.
Реакция начинается с отщепления молекулы воды и образования метиленовой группы, затем происходит неферментативная перестройка молекулы, в результате которой образуется иминогруппа, слабо связанная с а-углеродным атомом. Далее в результате неферментативного гидролиза отщепляется молекула аммиака и образуется пируват.
 2015-04-30
2015-04-30 795
795








